
- •Экзаменационные вопросы по биохимии для студентов лечебного, педиатрического, медико-профилактического факультетов за 2010-2011 уч. Год
- •Электрохимические свойства белков как основа методов их исследования. Электрофорез белков крови.
- •Коллоидные свойства белков. Гидратация. Растворимость. Денатурация, роль шаперонов.
- •Углевод-белковые комплексы. Строение углеводных компонентов. Гликопротеины и протеогликаны.
- •Липид-белковые комплексы. Строение липидных компонентов. Структурные протеолипиды и липопротеины, их функции.
- •Ферменты, их химическая природа, структурная организация. Активный центр ферментов, его строение.
- •Коферменты и их функции в ферментативных реакциях. Витаминные коферменты. Примеры реакций с участием витаминных коферментов.
- •Свойства ферментов. Лабильность конформации, влияние температуры и рН среды. Специфичность действия ферментов, примеры реакций.
- •Номенклатура и классификация ферментов. Характеристика класса оксидоредуктаз. Примеры реакций с участием оксидоредуктаз.
- •Характеристика класса лиаз, изомераз и лигаз (синтетаз), примеры реакций.
- •Характеристика классов ферментов трансфераз и гидролаз. Примеры реакций с участием данных ферментов.
- •Современные представления о механизме действия ферментов. Стадии ферментативного катализа, молекулярные эффекты, примеры.
- •Ингибирование ферментов. Конкурентное и неконкурентное ингибирование, примеры реакций. Лекарственные вещества как ингибиторы ферментов.
- •Обмен веществ и энергии. Этапы обмена веществ. Общий путь катаболизма. Окислительное декарбоксилирование пирувата.
- •Цитратный цикл, химизм процесса, его биологическое значение.
- •С опряжение реакций цикла трикарбоновых кислот с дыхательной цепью ферментов. Написать эти реакции.
- •Реакции прямого и окислительного декарбоксилирования, примеры.
- •Современные представления о биологическом окислении. Над-зависимые дегидрогеназы. Строение окисленной и восстановленной форм над.
- •Компоненты дыхательной цепи и их характеристика. Фмн и фад-зависимые дегидрогеназы. Строение окисленной и восстановленной форм фмн.
- •Цитохромы электронтранспортной цепи. Их функционирование. Образование воды как конечного продукта обмена.
- •Пути синтеза атф. Субстратное фосфорилирование (примеры). Молекулярные механизмы окислительного фосфорилирования (теория Митчелла). Разобщение окисления и фосфорилирования.
- •Альтернативные пути биологического окисления, оксигеназный путь. Микросомальные монооксигеназы.
- •Свободнорадикальное окисление. Токсичность кислорода. Активные формы кислорода. Антиокислительная защита. Роль сро в патологии.
- •Потребность человека в белках. Строение незаменимых аминокислот. Биологическая ценность белков. Роль белков в питании.
- •Превращение белков в желудке. Роль соляной кислоты в переваривании белков. Показать действие пептидгидролаз. Качественный и количественный анализ желудочного содержимого.
- •Переваривание белков в кишечнике. Покажите действие трипсина, карбокси-и аминопептидазы на конкретных примерах.
- •Гниение белков и аминокислот в кишечнике. Пути образования продуктов гниения. Примеры.
- •Механизм обезвреживания продуктов гниения белков. Роль фафс и удф-гк в этом процессе (конкретные примеры).
- •Переаминирование и декарбоксилирование аминокислот. Химизм процессов, характеристика ферментов и коферментов. Образование амидов.
- •Дезаминирование аминокислот. Виды дезаминирования. Окислительное дезаминирование. Непрямое дезаминирование аминокислот на примере тирозина.
- •Орнитиновый цикл, последовательность реакций, биологическая роль.
- •Особенности катаболизма пуриновых нуклеотидов. Их строение и распад. Образование мочевой кислоты. Подагра.
- •Генетические дефекты обмена фенилаланина и тирозина.
- •Механизмы репликации днк (матричный принцип, полуконсервативный способ). Условия, необходимые для репликации. Основные этапы репликации.
- •Биосинтез рнк (транскрипция). Условия и этапы транскрипции. Процессинг рнк. Альтернативный сплайсинг.
- •Биосинтез белка. Этапы трансляции и их характеристика. Белковые факторы биосинтеза белка. Энергетическое обеспечение биосинтеза белка.
- •Посттрансляционный процессинг. Виды химической модификации, фолдинг и адресование белков. Шапероны, прионы.
- •Строение оперона. Регуляция биосинтеза белка у прокариотов. Функционирование лактозного и гистидинового оперонов.
- •Особенности и уровни регуляции биосинтеза белка у эукариотов. Амплификация генов, энхансерные и сайленсерные элементы.
- •Блокаторы белковых синтезов. Действие антибиотиков и токсинов. Биологическая роль теломер и теломераз.
- •Виды молекулярных мутаций и их биологические последствия.
- •Биохимический полиморфизм. Генотипическая гетерогенность популяций. Наследственная непереносимость пищевых веществ и лекарств.
- •Причины полиморфизма и динамичности протеома при определенной консервативности генома: роль особенностей транскрипции, трансляции, процессинга белка.
- •Роль углеводов в питании. Переваривание и всасывание углеводов в органах пищеварительной системы. Написать реакции.
- •Катаболизм глюкозы в анаэробных условиях. Химизм процесса, биологическая роль.
- •Катаболизм глюкозы в тканях в аэробных условиях. Гексозодифосфатный путь превращения глюкозы и его биологическая роль. Эффект Пастера.
- •Г ексозомонофосфатный путь превращения глюкозы в тканях и его биологическая роль. Реакции окислительной стадии.
- •Биосинтез и распад гликогена в тканях. Биологическая роль этих процессов. Гликогеновые болезни.
- •Пути образования глюкозы в организме. Глюконеогенез. Возможные предшественники, последовательность реакций, биологическая роль.
- •Характеристика основных липидов организма человека, их строение, классификация, суточная потребность и биологическая роль.
- •62. Фосфолипиды, их химическое строение и биологическая роль.
- •63. Биологическая роль липидов пищи. Переваривание, всасывание и ресинтез липидов в органах пищеварительной системы.
- •64. Желчные кислоты. Их строение и биологическая роль. Желчнокаменная болезнь.
- •65. Окисление высших жирных кислот в тканях. Особенности окисления высших жирных кислот с нечетным числом углеродных атомов, энергетический эффект.
- •66. Окисление глицерола в тканях. Энергетический эффект этого процесса.
- •67. Биосинтез высших жирных кислот в тканях. Биосинтез липидов в печени и жировой ткани.
- •6 8. Холестерол. Его химическое строение, биосинтез и биологическая роль. Причины
- •Витамины, их характеристика, отличительные признаки. Роль витаминов в обмене веществ. Коферментная функция витаминов (примеры).
- •С труктура и функции витамина а.
- •Витамин д, его строение, метаболизм и участие в обмене веществ. Признаки проявления гиповитаминоза.
- •Участие витаминов е и к в метаболических процессах.
- •С труктура витамина в1, его участие в метаболических процессах, примеры реакций.
- •Витамин в2. Строение, участие в обмене веществ.
- •В итамин в6 и pp. Роль в обмене аминокислот, примеры реакций, строение.
- •Характеристика витамина с, строение. Участие в обмене веществ, проявление гиповитаминоза. Витамин р.
- •Витамин в12 и фолиевая кислота. Их химическая природа, участие в метаболических процессах. Причины гиповитаминозов.
- •Витамины – антиоксиданты, их биологическая роль. Витаминоподобные вещества. Антивитамины.
- •Биотин, пантотеновая кислота, их роль в обмене веществ.М
- •Гормоны передней доли гипофиза, классификация, их химическая природа, участие в регуляции процессов метаболизма. Семейство пептидов проопиомеланокортина.
- •Гормоны задней доли гипофиза, место их образования, химическая природа, влияние на функции органов-мишеней.
- •Тиреоидные гормоны, место их образования, строение, транспорт и механизм действия на метаболические процессы.
- •Тиреокальцитонин, паратиреоидный гормон. Химическая природа, участие в регуляции обмена веществ.
- •Инсулин, схема строения, участие в регуляции метаболических процессов. Специфика в действии на рецепторы органов мишеней, инсулиноподобные факторы роста (ифр).
- •Глюкагон и соматостатин. Химическая природа. Влияние на обмен веществ.
- •У частие адреналина в регуляции обмена веществ. Место выработки. Структура адреналина, механизм его гормонального действия, метаболические эффекты.
- •К ортикостероидные гормоны. Структура кортизола, механизм действия. Участие глюкокортикоидов и минералокортикоидов в обмене веществ.
- •Гормоны половых желез: эстрадиол и тестостерон, их строение, механизм действия и биологическая роль.
- •Простаноиды - регуляторы обмена веществ. Биологические эффекты простаноидов и химическая природа.
- •Важнейшие функции печени. Роль печени в обмене веществ.
- •Обезвреживающая роль печени. Реакции микросомального окисления и реакции коньюгации токсических веществ в печени. Примеры обезвреживания (фенол, индол).
- •Биосинтез и распад гемоглобина в тканях. Механизм образования основных гематогенных пигментов.
- •Патология пигментного обмена. Виды желтух.
- •Окисление этанола в печени. Первичные эффекты этанола.
- •Основы клинической биохимии. Основные виды изменений биохимического состава крови.
- •Белки крови, их биологическая роль, функциональная характеристика, лабораторно – диагностическое значение показателей белкового состава крови.
- •Химический состав нервной ткани.
- •Особенности обмена веществ в нервной ткани (энергетический, углеводный обмен).
- •Роль глутамата в обмене веществ в нервной ткани. Написать реакции.
- •Биохимия передачи нервного импульса. Основные компоненты и этапы.
- •Образование нейромедиаторов – ацетилхолина, адреналина, дофамина, серотонина.
- •Особенности химического состава мышечной ткани.
- •Особенности энергетического обеспечения мышечного сокращения. Креатин, креатинфосфат и продукт их распада. Биохимические изменения при мышечных дистрофиях и денервации мышц. Креатинурия.
- •Роль атф в мышечном сокращении. Пути ресинтеза атф в мышечной ткани. Написать реакции ресинтеза атф в анаэробных условиях. Нарушение метаболизма при ишемической болезни сердца.
- •Межклеточный матрикс, его компоненты, функции. Характеристика коллагена, его строение. Полиморфизм коллагеновых белков.
- •Этапы синтеза и созревания коллагена. Роль ферментов и витаминов в этом процессе. Катаболизм коллагена.
- •Особенности строения и функции эластина. Неколлагеновые структурные белки: фибронектин и ламинин.
- •Гликозаминогликаны. Строение, функции.
- •Протеогликаны межклеточного матрикса, их состав, функции. Образование надмолекулярных комплексов. Метаболизм протеогликанов.
- •Функциональная биохимия почек. Физико-химические свойства мочи. Характеристика химических компонентов мочи по отношению к процессам мочеобразования.
- •Молекулярные основы онкогенеза. Онкогены, протоонкогены, гены-супрессоры опухолей (гсо).
- •Виды клеточной гибели: апоптоз и некроз. Биологическое значение.
- •Этапы апоптоза. Рецепторы, передача сигнала гибели клетки.
- •Каспазы: образование и биологическая роль.
- •Варианты индукции апоптоза. Роль митохондрий в развитии апоптоза.
64. Желчные кислоты. Их строение и биологическая роль. Желчнокаменная болезнь.
Желчь представляет собой сложную жидкость со щелочной реакцией. В ней выделяют сухой остаток – около 3% и воду – 97%. В сухом остатке обнаруживается две группы веществ:попавшие сюда путем фильтрации из крови натрий, калий, бикарбонат-ионы, креатинин, холестерол (ХС), фосфатидилхолин (ФХ); активно секретируемые гепатоцитами билирубин и желчные кислоты.
В сутки образуется около 10 мл желчи на кг массы тела, таким образом, у взрослого человека это составляет 500-700 мл. Желчеобразование идет непрерывно, хотя интенсивность на протяжении суток резко колеблется.
Роль желчи
1. Наряду с панкреатическим соком нейтрализация кислого химуса, поступающего из желудка. При этом карбонаты взаимодействуют с НСl, выделяется углекислый газ и происходит разрыхление химуса, что облегчает переваривание.
2. Усиливает перистальтику кишечника.
3. Обеспечивает переваривание жиров:эмульгирование для последующего воздействия липазой, необходима комбинация [желчные кислоты+жирные кислоты+моноацилглицеролы]; уменьшает поверхностное натяжение, что препятствует сливанию капель жира; образование мицелл, способных всасываться.
4. Благодаря п.п.1 и 2 обеспечивает всасывание жирорастворимых витаминов (витамин A,витамин D, витамин K, витамин E).
5. Экскреция избытка ХС, желчных пигментов, креатинина, металлов Zn, Cu, Hg, лекарств. Для холестерина желчь – единственный путь выведения, с ней может выводиться 1-2 г/сут.
Синтез желчных кислот идет в эндоплазматическом ретикулуме при участии цитохрома Р450, кислорода, НАДФН и аскорбиновой кислоты. 75% холестерина, образуемого в печени, участвует в синтезе желчных кислот.
В печени синтезируются первичные желчные кислоты – холевая (гидроксилирована по С3, С7, С12) и хенодезоксихолевая (гидроксилирована по С3, С7), затем они образуют конъюгаты с глицином – гликопроизводные и с таурином – тауропроизводные, в соотношении 3:1 соответственно.
В кишечнике под действием микрофлоры эти желчные кислоты теряют НО-группу при С7 и превращаются во вторичные желчные кислоты – дезоксихолевую (гидроксилирована по С3и С12) и литохолевую (гидроксилирована только по С3).
Кишечно-печеночная циркуляция - Это непрерывная секреция желчных кислот в просвет кишечника и реабсорбция их большей части в подвздошной кишке, что сберегает ресурсы холестерола. В сутки происходит 6-10 таких циклов. Таким образом, небольшое количество желчных кислот (всего 3-5 г) обеспечивает переваривание липидов, поступающих в течение суток. Потери в размере около 0,5 г/сут соответствуют суточному синтезу холестерола de novo.
65. Окисление высших жирных кислот в тканях. Особенности окисления высших жирных кислот с нечетным числом углеродных атомов, энергетический эффект.
Окисление жирных кислот (β-окисление) - Для преобразования энергии, заключенной в жирных кислотах, в энергию связей АТФ существует метаболический путь окисления жирных кислот до СО2 и воды, тесно связанный с циклом трикарбоновых кислот и дыхательной цепью. Этот путь называется β-окисление, т.к. происходит окисление 3-го углеродного атома жирной кислоты (β-положение) в карбоксильную группу, одновременно от кислоты отщепляется ацетильная группа, включающая С1 и С2 исходной жирной кислоты.
Р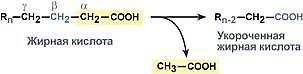 еакции
β-окисления происходят в митохондриях большинства
клеток организма (кроме нервных клеток).
Для окисления используются жирные
кислоты, поступающие в цитозоль из
крови или появляющиеся
при липолизе собственных
внутриклеточных ТАГ. Суммарное
уравнение окисления пальмитиновой
кислоты выглядит следующим образом:
еакции
β-окисления происходят в митохондриях большинства
клеток организма (кроме нервных клеток).
Для окисления используются жирные
кислоты, поступающие в цитозоль из
крови или появляющиеся
при липолизе собственных
внутриклеточных ТАГ. Суммарное
уравнение окисления пальмитиновой
кислоты выглядит следующим образом:
Пальмитоил-SКоА + 7ФАД + 7НАД+ + 7Н2O + 7HS-KoA → 8Ацетил-SКоА + 7ФАДН2 + 7НАДН
Этапы окисления жирных кислот
1![]() .
Прежде, чем проникнуть вматрикс
митохондрий и окислиться, жирная кислота
должна активироваться в цитозоле.
Это осуществляется присоединением к
ней коэнзима А с образованием ацил-S-КоА.
Ацил-S-КоА является высокоэнергетическим
соединением. Необратимость реакции
достигается гидролизом дифосфата на
две молекулы фосфорной кислоты.
.
Прежде, чем проникнуть вматрикс
митохондрий и окислиться, жирная кислота
должна активироваться в цитозоле.
Это осуществляется присоединением к
ней коэнзима А с образованием ацил-S-КоА.
Ацил-S-КоА является высокоэнергетическим
соединением. Необратимость реакции
достигается гидролизом дифосфата на
две молекулы фосфорной кислоты.
2. Ацил-S-КоА не способен проходить через митохондриальную мембрану, поэтому существует способ его переноса в комплексе с витаминоподобным веществом карнитином. На наружной мембране митохондрий имеется фермент карнитин-ацилтрансфераза I.
Карнитин синтезируется в печени и почках и затем транспортируется в остальные органы. Во внутриутробном периоде и в первые годы жизни значение карнитина для организма чрезвычайно важно. Энергообеспечение нервной системы детскогоорганизма и, в частности, головного мозга осуществляется за счет двух параллельных процессов: карнитин-зависимого окисления жирных кислот и аэробного окисления глюкозы. Карнитин необходим для роста головного и спинного мозга, для взаимодействия всех отделов нервной системы, ответственных за движение и взаимодействие мышц. Существуют исследования, связывающие с недостатком карнитина детский церебральный паралич и феномен "смерти в колыбели".
3. После связывания с карнитином жирная кислота переносится через мембранутранслоказой. Здесь на внутренней стороне мембраны фермент карнитин-ацилтрансфераза II вновь образует ацил-S-КоА который вступает на путь β-окисления.
4. Процесс собственно β-окисления состоит из 4-х реакций, повторяющихся циклически. В них последовательно происходит окисление (ацил-SКоА-дегидрогеназа), гидратирование(еноил-SКоА-гидратаза) и вновь окисление 3-го атома углерода (гидроксиацил-SКоА-дегидрогеназа). В последней, трансферазной, реакции от жирной кислоты отщепляетсяацетил-SКоА. К оставшейся (укороченной на два углерода) жирной кислоте присоединяется HS-КоА, и она возвращается к первой реакции. Все повторяется до тех пор, пока в последнем цикле не образуются два ацетил-SКоА.
Жирные кислоты с нечетным числом углеродов поступают в организм с растительной пищей и морепродуктами. Их окисление происходит по обычному пути до последней реакции, в которой образуется пропионил-SКоА. Суть превращений пропионил-SКоА сводится к его карбоксилированию, изомеризации и образованию сукцинил-SКоА. В этих реакциях участвуют биотин и витамин В12.
При окислении ненасыщенных жирных кислот возникает потребность клетки в дополнительных ферментах изомеразах. Эти изомеразы перемещают двойные связи в жирнокислотных остатках из γ- в β-положение и переводят природные двойные связи изцис- в транс-положение.Таким образом, уже имеющаяся двойная связь готовится к β-окислению и пропускается первая реакция цикла, в которой участвует ФАД.
