
- •1 Предмет і завдання хімі. Основні етапи розвитку хімії. Зв*язок хімії з іншими природничими ауками.
- •2 Роль хімії в народному господарстві, медицині. Хімія та екологія.
- •3 Основні поняття і закони в хімії. Хімічні та фізичні явища. Атомна і молекулярна маса.
- •Основні поняття і закони в хімії
- •7 Періодичний закон та періодична система елементів д.І. Мендєлєєва, структура періодичного хімічних елементів. Значення періодичного закону.
- •Значення періодичного закону:
- •8 Будова атома: ядро, енергетичні рівні. Електронні конфігурації атомів елементів в основному та збудженому стані.
- •Типи хімічних зв’язків:
- •11 Типи хімічних реакцій. Типи кристалічних граток.
- •Кристалічні гратки:
- •12 Оксиди.
- •Застосування
- •20 Сильні і слабкі електроліти. Дисоціація кислот, основ. Солей на іони.
- •21 Галогени. Хлор. Якісна реакція на хлорид – іон.
- •22 Сульфур. Алотропні модифікації сульфуру. Застосування.
- •23 Оксинен. Алотропні модифікації оксисену. Застосування.
- •24 Оксид Сульфуру (IV).
- •Хімічні властивості
- •25 Сульфур(VI) оксид
- •26 Сульфатна кислота.
- •27 Нітроген. Будова молекул
- •Якісна реакція
- •31 Фосфор. Алотропні модифікації.
- •Поширення в природі
- •32 Сполуки фосфору. Якісна реакція. Біологічне значення. Фосфатні добрива.
- •33 Карбон. Алотропні модифікації. Поняття про адсорбцію, застосування.
- •Фізичні властивості Алотропні модифікації
- •34 Оксиди карбону. Карбонатна кислота та її солі. Якісна реакція. Твердість води та способи її усунення. Кругообіг Карбону в природі.
- •36 Силіцій (4) оксид. Силікатна кислота. Силікати. Поняття про будівельні матеріали.
- •Хімічні властивості силіцій(IV) оксиду
- •37 Загальна характеристика металів.
- •Залежність швидкості реакцій від різних чинників
- •Хімічна рівновага
- •2 Теорія хімічної будови органічних сполук о. М. Бутлерова
- •3 Класифікація органічних сполук. Поняття про функціональні групи. Ізомерія
- •Класифікація
- •Найважливіші класи органічних сполук
- •4 Електронна будова атома Карбону. Основний і збуджений стан атома Карбону.
- •5 Алкани.
- •6 Фізичні і хімічні властивості насичених вуглеводнів. Добування, застосування
- •16 Одноатомні спирти
- •17 Фізичні та хімічні властивості одноатомних спиртів. Застосування. Отруйність спиртів та їх згубна дія на організм людини.
- •18 Багатоатомні спирти. Етиленгліколь і гліцерин
- •24 Одноосновні карбонові кислоти
- •Значення жирів
- •28 Мила
- •Класифікація
- •Добування:
- •30 Амінокислоти
- •Класифікація
- •Класифікація
- •Хімічні властивості
- •Рибосомний синтез
- •Нерибосомний синтез
- •33 Вуглеводи. Глюкоза. Сахароза
- •Класифікація
- •34 Полісахариди
- •35 Крохмаль і целюлоза
- •36 Синтетичні високомолекулярні речовини. Полімерні матеріали. Синтетичні волокна і синтетичні каучуки, утворення гуми. Застосування полімерних матеріалів
- •37 Генетичний зв*язок між органічними і неорганічними речовинами.
- •40 Хімія і екологія.
Класифікація
Прості і складні білки
За складом виділяють прості і складні білки. Прості білки містять тільки амінокислоти, зв'язані в ланцюжки. На відміну від них складні білки мають також неамінокислотні групи. Ці додаткові групи у складі складних білків називаються простетичними групами. Деякі простетичні групи служать кофакторами, необхідними для роботи ферментів. Інші, такі як полісахаридні ланцюжки, допомагають білку приймати потрібну конформацію і додають додаткову стабільність. Прикладами органічних простетичних груп в складі білків служать гем (в складі гемоглобіну), тіамін, біотин та інші. Неорганічні простетичні групи найчастіше складаються з іонів металів, найпоширенішими з яких є цинк, магній і молібден[14]. За типом простетичної групи складні білки поділяють на глікопротеїни, ліпопротеїни, хромопротеїни, нуклеопротеїни, фосфопротеїни, металопротеїни та деякі інші.
32 Властивості білків. Успіхи науки у вивченні та синтезі білків.
Хімічні властивості
1. Денатурація
Руйнування третинної і третинної структури білків під дією хімічних реагентів, нагрівання або радіації
2. Гідроліз
Руйнування первинної структури білків під дією хімічних реагентів (луги, кислоти, ферменти) з утворенням a-амінокислот
3. Якісні реакції білків
• біуретова реакція
При взаємодії білків з солями міді у лужному середовищі спостерігається поява фіолетового забарвлення. Дана реакція характеризує наявність пептидних зв'язків:
-CO - NH-
• ксантопротеїнова реакція
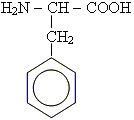
При дії нітратної кислоти на білки спостерігається поява жовтого забарвлення. Дана реакція характеризує наявність бензольних ядер, що входять до складу деяких амінокислот, наприклад, фенілаланіну:
Рибосомний синтез
Білки синтезуються живими організмами з амінокислот на основі інформації, закодованої в генах. Кожен білок складається з унікальної послідовності амінокислот, яка визначається нуклеотидною послідовністю гену, що кодує даний білок. Генетичний код складається з трибуквених «слів», які називаються кодонами. Кожен кодон відповідає за приєднання до білка однієї амінокислоти: наприклад, поєднання AUG (АУГ) відповідає метіоніну. Оскільки ДНК складається з чотирьох типів нуклеотидів, то загальне число можливих кодонів дорівнює 64; а оскільки в білках використовується 20 амінокислот, то багато амінокислот визначаються більш ніж одним кодоном. Гени, що кодують білки, спочатку транскрибуются в послідовність нуклеотидів матричної РНК (мРНК) білками РНК-полімеразами.
У прокаріотів мРНК може зчитуватися рибосомами в амінокислотну послідовність білків відразу після транскрипції, проте в більшості випадків у еукаріотів та інколи у бактерій вона оброблюється в процесі сплайсингу. Після цього еукаріоти повинні також транспортувати зрілу мРНК з ядра в цитоплазму, де знаходяться рибосоми.
Швидкість синтезу білків вища у прокаріотів і може досягати 20 амінокислот в секунду[16].
Процес синтезу білка з мРНК називається трансляцією. Під час початкової стадії трансляції — ініціації, кодон метионіну розпізнається малою субодиницею рибосоми, до якої за допомогою білкових факторів ініціації приєднана метионінова транспортна РНК (тРНК). Після розпізнавання стартового кодону до малої субодиниці приєднується велика субодиниця рибосоми, і починається друга стадія трансляції — елонгація. На кожному кроці рибосоми від 5' до 3' кінця мРНК прочитується один кодон шляхом утворення водневих зв'язків між трьома нуклеотидами (кодоном) мрРНК і комплементарним йому антикодоном транспортної РНК, до якої приєднана відповідна амінокислота. Синтез пептидного зв'язку каталізує рибосомна РНК (рРНК), що утворює пептиділтрансферазний центр рибосоми. Рибосомна РНК каталізує утворення пептидного зв'язку між останньою амінокислотою пептиду, і амінокислотою, приєднаною до тРНК, позиціонуючи атоми азоту і вуглецю в положенні, сприятливому для проходження реакції. Фермент аміноацил-тРНК-синтетаза приєднує амінокислоти до їхньої тРНК. Третя, і остання стадія трансляції, термінація, відбувається при досягненні рибосомою стоп-кодону, який не кодує амінокислот, після чого білкові фактори термінації гідролізують останню тРНК від білка, припиняючи синтез. В рибосомах білки завжди синтезуються від N- до C- кінця.
