
- •Дефекты кристаллического строения металлов.
- •4. Объёмные дефекты.
- •Фазовый состав сплавов.
- •Правило фаз (закон Гиббса) и правило определения состава и количества фаз (правило отрезков).
- •Р авновесная диаграмма состояния сплавов, образующих твердые растворы с неограниченной растворимостью.
- •Диаграмма состояния сплавов, компоненты которых ограниченно растворимы в твердом состоянии и образуют эвтектику.
- •Компоненты и фазы в системе железо-углерод.
- •Диаграмма Fе – Fе3с. Основные области и линии
- •Фазы и структуры углеродистых сталей в твердом состоянии.
- •Разновидности чугунов и их свойства.
- •Основные цели термической обработки металлических сплавов.
- •Отжиг 1 -го рода для уменьшения напряженней
- •Рекристаллизационный отжиг. Влияние нагрева на структуру и свойства деформируемого металла.
- •Отжиг 2-го рода. Фазовые превращения при нагреве сталей.
- •Аустенитное зерно.
- •Превращение (распад) аустенита при медленном охлаждении.
- •Диаграмма изотермического распада аустенита эвтектоидной стали.
- •Термокинетическая диаграмма распада аустенита (непрерывное охлаждение),
- •Отжиг 2-го рода доэвтектоидных сталей.
- •Сфероидизирующий отжиг заэвтектоидных сталей (инструментальный).
- •Закалка сталей. Условия проведения закалки.
- •Мартенсит. Изменение свойств при закалке на мартенсит.
- •Температуры мартенситного превращения
- •Изменение свойств стали при закалке на мартенсит
- •Способы закалки. Дефекты закалки
- •Бейнитное превращение. Механические свойства стали с бейнитной структурой.
- •Отпуск закаленных сталей, его параметры.
- •Структура и свойства отпущенной при разных температурах стали.
- •Прокаливаемость стали. Влияние прокаливаемости на свойства стали.
- •Химико-термическая обработка сталей и ее назначение. Основные методы насыщения и стадии хто.
- •Цементация сталей. Механизм образования, строение и свойства цементованного слоя.
- •Способы цементации.
- •Термическая обработка цементованных изделий.
- •Контроль качества цементованных изделий.
- •Нитроцементация и цианирование. Особенности совместной диффузии в стали с и n.
- •Структура и свойства нитроцементованного слоя. Дефекты нитроцементации.
- •Азотирование стали. Формирование диффузионного слоя и его строение.
- •Легированные стали. Цели легирования. Маркировка.
- •Влияние легирующих элементов на полиморфное превращение железа. Фазы в легированной стали.
- •В свободном состоянии.
- •В форме растворов в железе.
- •Влияние легирующих элементов на превращения в сталях.
- •Классификация легированных сталей.
- •Машиностроительные (конструкционные) стали.
- •Требования предъявляемые к подшипникам. Классификация подшипниковых сталей.
- •Улучшаемые конструкционные легированные стали.
- •Пружинные конструкционные стали.
- •Высокопрочные конструкционные стали.
- •Износостойкая аустенитная сталь.
- •С тали для строительных конструкций.
- •Дефекты легированных сталей.
- •Коррозионностойкие стали ферритного, мартенситного и аустенитного класса.
- •Инструментальные материалы. Стали для режущего инстумента.
- •Быстрорежущие стали. Термическая обработка быстрорежущих сталей.
- •Спеченные твердые сплавы.
- •Стали для измерительных инструментов.
- •Штамповые стали.
- •Полиморфизм металлов.
- •54.Постоянные примеси сталей
- •56. Обратимая и необратимая отпускная хрупкость.
- •57. Классификация алюминиевых сплавов.
- •58. Деформируемые алюминиевые сплавы и их термическая обработка.
- •59. Литейные и ковочные алюминиевые сплавы.
- •60. Спеченные алюминиевые сплавы.
- •61. Титан и его сплавы. Термическая обработка титановых сплавов.
- •62. Медь и её сплавы. Общая характеристика и классификация медных сплавов.
- •63. Бронзы – состав, свойства.
- •64. Латуни – состав, свойства.
- •65. Характеристика и классификация композиционных материалов.
Правило фаз (закон Гиббса) и правило определения состава и количества фаз (правило отрезков).
Процесс кристаллизации сплавов и связанные с ним многие закономерности строения описываются с помощью диаграммы состояния (ДГ) – графическое изображение состояния сплавов (фазовый состав и структура, в зависимости от элементов и температуры).
ДГ определяют устойчивые равновесные состояния сплавов, обладающие при данных условиях миниальной свободной энергией. Строят их экспериментальными методами, одним из которых является термический анализ, с помощью которого получают кривые охлаждения (кристаллизации) и точки перегиба кривых называют критическими точками. Они соответветвтсвуют температурам, при которых в сплавах начивают/заканчиваются какие-либо фазовые превращения.
Для построения диаграмм состояния и снятия кривых охлаждения берут большое количество сплавов с разной концентрацией компонентов.
Зависимость существования устойчивых фаз, отвечающая условиям равновесия, описывается условием Гиббса:
 ,
где с – число степеней свободы,
,
где с – число степеней свободы,
к – число компонент, ф – число фаз.
2 – число внешних факторов (Т, Р)
П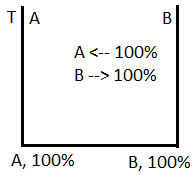 од
числом «с» (вариантностью системы),
понимается возможность изменения
температуры, давления и концентрации
без изменения числа фаз, находящихся в
равновесии.
од
числом «с» (вариантностью системы),
понимается возможность изменения
температуры, давления и концентрации
без изменения числа фаз, находящихся в
равновесии.
Применяя правило фаз Гиббса к металлам, можно во множестве случаев принять изменяющимся только один внешний фактор – температуру, так как давление мало влияет на фазовые превращения.
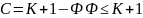
Если максимальное число фаз: с = 0 (при Т = константа).
Диаграмма состояния сплавов, имеющих неограниченную растворимость в жидком, твёрдом состоянии. Правило отрезков.
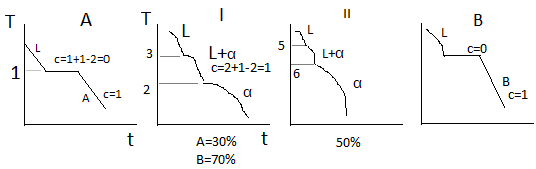
Верхняя линяя на диаграмме 1-3-5-6 – линия начала кристаллизации – Ликвидус. Линия 1-2-4-6 – линия окончания кристаллизации – линия Солидус. Выше линии Ликвидус существует только жидкая фаза L. Между линиями ликвидус и солиус идёт процесс кристаллизации и в равновесии находятся 2 фазы, т.е.число степеней свободы с=2+1-2=1. Ниже линии солидус – все сплавы однофазны и состоят из α-твёрдого раствора. Такую диаграмму состояния имеют следующие сплавы: Cu-Ni, Cu-Pt, Au-Ag, Fe-Va, Fe-Ni, Mo-W.
Р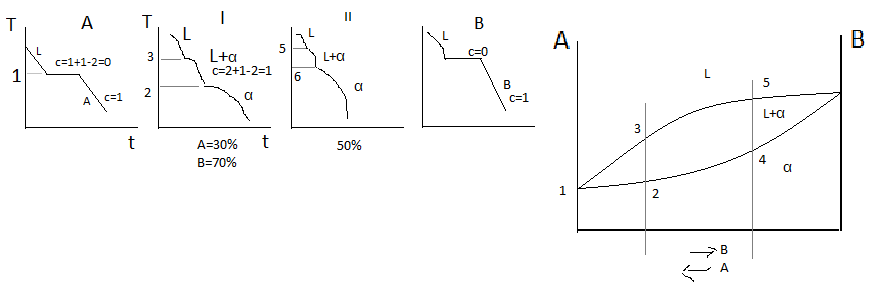 ассмотрим
более подробно процесс кристаллизации
сплава 50% А 50% В. Кристаллизация начинается
при температуре T1,
когда из жидкого раствора выделяются
первые кристаллы α-твёрдого раствора.
Ниже температуры T1
сплав 2х фазный (L+α).
В процессе кристаллизации твёрдых
растворов состав твёрдой и жидкой фазы
меняется. Каждой температуре соответствует
определённое количество и концентрация
фаз. В реальных условиях или при быстром
охлаждении не успевает произойти
выравнивание концентрации в твёрдом
растворе. Даже в пределах 1-го кристалла
будет наблюдаться неоднородный химический
состав. Первые кристаллы α-твёрдого
раствора обогащены компонентом В, а
далее всё время меняется соотношение
А и В. И последние кристаллы будут
содержать больше компонента А.
ассмотрим
более подробно процесс кристаллизации
сплава 50% А 50% В. Кристаллизация начинается
при температуре T1,
когда из жидкого раствора выделяются
первые кристаллы α-твёрдого раствора.
Ниже температуры T1
сплав 2х фазный (L+α).
В процессе кристаллизации твёрдых
растворов состав твёрдой и жидкой фазы
меняется. Каждой температуре соответствует
определённое количество и концентрация
фаз. В реальных условиях или при быстром
охлаждении не успевает произойти
выравнивание концентрации в твёрдом
растворе. Даже в пределах 1-го кристалла
будет наблюдаться неоднородный химический
состав. Первые кристаллы α-твёрдого
раствора обогащены компонентом В, а
далее всё время меняется соотношение
А и В. И последние кристаллы будут
содержать больше компонента А.
И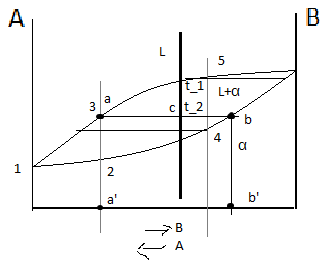 так,
для определения количественного
соотношения фаз, находящихся в равновесии
при данной температуре, пользуются
правилом
отрезков
(рычага).
так,
для определения количественного
соотношения фаз, находящихся в равновесии
при данной температуре, пользуются
правилом
отрезков
(рычага).
Правило
отрезков
позволяет определить:
Состав
фаз или концентрацию компонентов в
соответствующих фазах. Для этого точки
пересечения коноды с линиями диаграммы
переносятся на ось концентрации, т.е.
конода параллельна линии концентрации.
Конода – линия, соединяющая состав фаз,
находящихся в равновесии. a'
– состав жидкой фазы, b’
– состав α-твёрдого раствора. Количество
фаз:
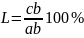
 .
Если точка, показывающая состав при
данной температуре, т.е. линия ниже линии
ликвидуса и выше линии солидуса, а её
состав соответствует исходному составу.
.
Если точка, показывающая состав при
данной температуре, т.е. линия ниже линии
ликвидуса и выше линии солидуса, а её
состав соответствует исходному составу.
