
- •Химический анализ
- •Часть 1. Качественный анализ неорганических веществ
- •Введение
- •1. Качественный анализ неорганических веществ
- •1.1. Методы и условия проведения качественного химического анализа
- •Классификация методов анализа в зависимости от количества исследуемого вещества
- •Методы разделения и концентрирования
- •1.2. Качественные аналитические реакции и аналитические признаки
- •1.3. Реактивы, применяемые в качественном анализе
- •Органические реактивы, используемые в качественном анализе
- •1.4. Аналитическая классификация ионов в качественном анализе
- •Аналитическая классификация анионов
- •Контрольные вопросы
- •2. Кислотно-основная аналитическая классификация катионов
- •2.1. Первая аналитическая группа катионов
- •2.1.1. Реакции катиона лития
- •4. Реакция с гексанитрокобальтатом(III) натрия Na3[Co(no2)6]:
- •2.1.3. Реакции катиона натрия
- •2.1.4. Реакции катиона калия
- •2. Реакция с гидротартратом натрия NaHc4h4o6.
- •3. Реакция с гексанитрокобальтатом(III) натрия Na3[Co(no2)6].
- •4. Реакция с гексанитрокупратом(II) свинца и натрия Na2Pb[Cu(no2)6].
- •Сводная таблица реакций катионов первой аналитической группы
- •2.2. Вторая аналитическая группа катионов
- •2.2.1. Реакции катиона серебра
- •2.2.3. Реакции катиона свинца(II)
- •Сводная таблица реакций катионов второй аналитической группы
- •2.3. Третья аналитическая группа катионов
- •2.3.1. Реакции катиона бария
- •2.3.2. Реакции катиона кальция
- •2.3.3. Реакции катиона стронция
- •Сводная таблица реакций катионов третьей аналитической группы
- •2.4. Четвёртая аналитическая группа катионов
- •2.4.1. Реакции катиона алюминия
- •2.4.2. Реакции катиона хрома (III)
- •2.4.3. Реакции катиона цинка
- •2.4.4. Реакции катионов олова(II) и (IV)
- •Сводная таблица реакций катионов четвертой аналитической группы
- •2.5. Пятая аналитическая группа катионов
- •2.5.3. Реакции катиона марганца (II)
- •2.5.4. Реакции катиона магния
- •2.5.5. Реакции катиона висмута (III)
- •2. Реакция с 8-оксихинолином c9h6n(он).
- •2.5.6. Реакции катиона сурьмы (III)
- •1. Реакция с тиосульфатом натрия Na2s2o3.
- •2.5.7. Реакции катиона сурьмы(V)
- •Сводная таблица реакций катионов пятой аналитической группы
- •2.6. Шестая аналитическая группа катионов
- •2.6.1. Реакции катиона меди (II)
- •2.6.2. Реакции катиона никеля(II)
- •2.6.3. Реакции катиона кобальта(II)
- •2.6.5. Реакции катиона ртути(II)
- •Сводная таблица реакций катионов шестой аналитической группы
- •Контрольные вопросы к разделу 2.1
- •Контрольные вопросы к разделу 2.2
- •Контрольные вопросы к разделу 2.3
- •Контрольные вопросы к разделу 2.4
- •Контрольные вопросы к разделу 2.5
- •Контрольные вопросы к разделу 2.6
- •3. Аналитическая классификация анионов
- •3.1. Анионы первой аналитической группы
- •3.1.1. Реакции хлорид - иона
- •3.1.2. Реакции бромид-иона
- •3.1.3. Реакции иодид-иона
- •3. Реакция окисления нитритом натрия:
- •3.1.4. Реакции сульфид-иона
- •5. Реакция с гидроксокомплексом свинца [Pb(oh)4 ]2-:
- •Качественные реакции анионов первой аналитической группы
- •3.2. Анионы второй аналитической группы
- •3.2.2. Реакции сульфит-иона
- •3.2.3. Реакции карбонат-иона
- •3.2.4. Реакции фосфат-иона
- •3.2.5. Реакции тиосульфат-иона
- •3.2.6. Реакции силикат-иона
- •3.2.7. Реакции борат-иона
- •Качественные реакции анионов второй аналитической группы
- •3.3. Анионы третьей аналитической группы
- •3.3.1. Реакции нитрат-иона
- •3.3.2. Реакции нитрит-иона
- •2. Реакция с иодидом калия ki.
- •Качественные реакции анионов третьей аналитической группы
- •Контрольные вопросы к разделу 3.1
- •Контрольные вопросы к разделу 3.2
- •Контрольные вопросы к разделу 3.3
- •4. Качественный анализ неизвестного вещества
- •4.1. Предварительные испытания
- •Предварительные испытания неизвестного вещества
- •4.2. Анализ индивидуальной соли
- •4.3. Систематический анализ смеси катионов
- •4.3.2. Систематический ход анализа (один из вариантов).
- •6. Анализ раствора 4 (V группа). Аммиакат меди – синий, никеля – сине-голубой, кобальта – желтый.
- •Контрольные вопросы
- •Список литературы
- •Химический анализ
- •Часть 1. Качественный анализ неорганических веществ
2.5.7. Реакции катиона сурьмы(V)
1. Реакция восстановления ионов Sb5+ до металлической сурьмы. В присутствии металлов, стоящих в ряду напряжений до сурьмы (Zn, Fe, Al и др.), катион Sb(III) восстанавливается до металлической сурьмы:
3Sb5+ + 5Al = 3Sb + 5Al3+.
Реакцию проводят на металлической пластинке в кислой среде. Пластинка чернеет вследствие выделения металлического висмута.
Методика проведения реакции. На очищенную металлическую пластинку (Zn, Fe, Al и др.) наносят каплю раствора соли Sb(III или V) и каплю раствора HCl . Пластинку оставляют на 2-3 минуты.
2. Реакция с родамином С. Родамин С и другие основные трифенилметановые красители в солянокислом растворе образуют с хлоридным комплексом сурьмы (V) малорастворимый в воде, окрашенный в фиолетовый цвет ионный ассоциат:
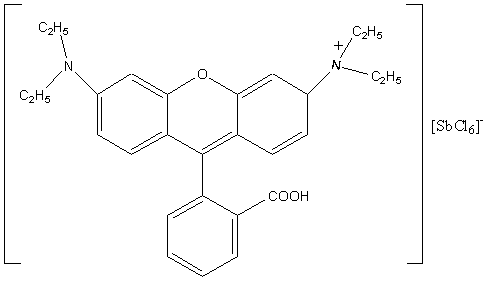 .
.
Методика проведения реакции. Реакцию одновременно проводят в двух пробирках. В одну пробирку помещают каплю раствора, содержащего ионы сурьмы (III или V), в другую - каплю 2 н. HCl. В обе пробирки добавляют по 2 капли концентрированной HCl, немного твердого нитрита натрия для окисления сурьмы (III) до сурьмы (V), по капле раствора родамина С и по 5-7 капель бензола. Пробирки закрывают пробками и встряхивают 2-3 минуты. В присутствии сурьмы органическая фаза окрашивается в красно-фиолетовый цвет. В пробирке с контрольным опытом окраска бензольного слоя бледно-розовая.
Некоторые реакции катионов пятой аналитической группы приведены в табл. 9.
Таблица 9
Сводная таблица реакций катионов пятой аналитической группы
Реагент |
Катионы
|
||||||
Fe 2+ |
Fe 3+ |
Mn 2+ |
Mg 2+ |
Bi 3+ |
Sb 3+ |
Sb 5+
|
|
NaOH |
Fe(OH)2 зеленый осадок, на воздухе буреет |
Fe(OH)3 бурый осадок |
Mn(OH)2 белый осадок, буреет |
Mg(OH)2 белый осадок, растворим в растворе NH4Cl
|
Bi(OH)3 белый осадок |
Sb(OH)3 белый осадок |
SbO(OH)3 белый осадок
|
Растворимы в кислотах
|
|||||||
H2S |
FeS↓ черный |
Fe2S3↓ чёрный |
MnS↓ телесный |
--- |
Bi2S3↓ черный |
Sb2S3↓ крас-ный |
Sb2S5↓ оранж.- красный
|
H2O |
---- |
---- |
---- |
---- |
BiOCl ↓ белый, нераст-ворим в винной кислоте |
SbOCl ↓ |
SbO2Cl ↓ |
Белые, растворимы в винной кислоте |
|||||||
8-окси-хинолин |
---- |
желтый осадок |
зеленый осадок |
зеленовато-желтый осадок |
зеле-ный осадок
|
желтый осадок |
---- |
Окислители |
Fe3+ желтый раствор |
--- |
MnO4 – фиолетово-красный раствор
|
--- |
--- |
соли Sb 5+ |
--- |
Восстанови- тели
|
-- |
--- |
--- |
--- |
Bi ↓ черный |
Sb ↓ черный |
Sb ↓ черный |
