
- •Химический анализ
- •Часть 1. Качественный анализ неорганических веществ
- •Введение
- •1. Качественный анализ неорганических веществ
- •1.1. Методы и условия проведения качественного химического анализа
- •Классификация методов анализа в зависимости от количества исследуемого вещества
- •Методы разделения и концентрирования
- •1.2. Качественные аналитические реакции и аналитические признаки
- •1.3. Реактивы, применяемые в качественном анализе
- •Органические реактивы, используемые в качественном анализе
- •1.4. Аналитическая классификация ионов в качественном анализе
- •Аналитическая классификация анионов
- •Контрольные вопросы
- •2. Кислотно-основная аналитическая классификация катионов
- •2.1. Первая аналитическая группа катионов
- •2.1.1. Реакции катиона лития
- •4. Реакция с гексанитрокобальтатом(III) натрия Na3[Co(no2)6]:
- •2.1.3. Реакции катиона натрия
- •2.1.4. Реакции катиона калия
- •2. Реакция с гидротартратом натрия NaHc4h4o6.
- •3. Реакция с гексанитрокобальтатом(III) натрия Na3[Co(no2)6].
- •4. Реакция с гексанитрокупратом(II) свинца и натрия Na2Pb[Cu(no2)6].
- •Сводная таблица реакций катионов первой аналитической группы
- •2.2. Вторая аналитическая группа катионов
- •2.2.1. Реакции катиона серебра
- •2.2.3. Реакции катиона свинца(II)
- •Сводная таблица реакций катионов второй аналитической группы
- •2.3. Третья аналитическая группа катионов
- •2.3.1. Реакции катиона бария
- •2.3.2. Реакции катиона кальция
- •2.3.3. Реакции катиона стронция
- •Сводная таблица реакций катионов третьей аналитической группы
- •2.4. Четвёртая аналитическая группа катионов
- •2.4.1. Реакции катиона алюминия
- •2.4.2. Реакции катиона хрома (III)
- •2.4.3. Реакции катиона цинка
- •2.4.4. Реакции катионов олова(II) и (IV)
- •Сводная таблица реакций катионов четвертой аналитической группы
- •2.5. Пятая аналитическая группа катионов
- •2.5.3. Реакции катиона марганца (II)
- •2.5.4. Реакции катиона магния
- •2.5.5. Реакции катиона висмута (III)
- •2. Реакция с 8-оксихинолином c9h6n(он).
- •2.5.6. Реакции катиона сурьмы (III)
- •1. Реакция с тиосульфатом натрия Na2s2o3.
- •2.5.7. Реакции катиона сурьмы(V)
- •Сводная таблица реакций катионов пятой аналитической группы
- •2.6. Шестая аналитическая группа катионов
- •2.6.1. Реакции катиона меди (II)
- •2.6.2. Реакции катиона никеля(II)
- •2.6.3. Реакции катиона кобальта(II)
- •2.6.5. Реакции катиона ртути(II)
- •Сводная таблица реакций катионов шестой аналитической группы
- •Контрольные вопросы к разделу 2.1
- •Контрольные вопросы к разделу 2.2
- •Контрольные вопросы к разделу 2.3
- •Контрольные вопросы к разделу 2.4
- •Контрольные вопросы к разделу 2.5
- •Контрольные вопросы к разделу 2.6
- •3. Аналитическая классификация анионов
- •3.1. Анионы первой аналитической группы
- •3.1.1. Реакции хлорид - иона
- •3.1.2. Реакции бромид-иона
- •3.1.3. Реакции иодид-иона
- •3. Реакция окисления нитритом натрия:
- •3.1.4. Реакции сульфид-иона
- •5. Реакция с гидроксокомплексом свинца [Pb(oh)4 ]2-:
- •Качественные реакции анионов первой аналитической группы
- •3.2. Анионы второй аналитической группы
- •3.2.2. Реакции сульфит-иона
- •3.2.3. Реакции карбонат-иона
- •3.2.4. Реакции фосфат-иона
- •3.2.5. Реакции тиосульфат-иона
- •3.2.6. Реакции силикат-иона
- •3.2.7. Реакции борат-иона
- •Качественные реакции анионов второй аналитической группы
- •3.3. Анионы третьей аналитической группы
- •3.3.1. Реакции нитрат-иона
- •3.3.2. Реакции нитрит-иона
- •2. Реакция с иодидом калия ki.
- •Качественные реакции анионов третьей аналитической группы
- •Контрольные вопросы к разделу 3.1
- •Контрольные вопросы к разделу 3.2
- •Контрольные вопросы к разделу 3.3
- •4. Качественный анализ неизвестного вещества
- •4.1. Предварительные испытания
- •Предварительные испытания неизвестного вещества
- •4.2. Анализ индивидуальной соли
- •4.3. Систематический анализ смеси катионов
- •4.3.2. Систематический ход анализа (один из вариантов).
- •6. Анализ раствора 4 (V группа). Аммиакат меди – синий, никеля – сине-голубой, кобальта – желтый.
- •Контрольные вопросы
- •Список литературы
- •Химический анализ
- •Часть 1. Качественный анализ неорганических веществ
2.2. Вторая аналитическая группа катионов
Ко второй аналитической группе относятся катионы, дающие малорастворимые соединения при взаимодействии с соляной кислотой и ее солями. К ним относятся ионы Ag+, Hg22+, Pb2+. Катионы этой группы с сульфат-, сульфит-, сульфид-, фосфат-, хромат-, карбонат- и галогенид-анионами образуют нерастворимые соли. При взаимодействии со щелочами также образуются нерастворимые вещества. Гидроксиды, образуемые данными катионами, обладают слабоосновными свойствами, поэтому при растворении в воде их соли легко гидролизуются и имеют кислую реакцию.
Групповым реактивом является соляная кислота HCl. При взаимодействии катионов второй группы с разбавленной соляной кислотой или ее солями образуются осадки хлоридов, малорастворимые в холодной воде и кислотах согласно реакциям:
Ag+ + Cl- = AgCl (тв);
Hg22+ + 2Cl- = Hg2Cl2 (тв);
Pb2+ + 2Cl- = PbCl2 (тв).
Растворимость хлоридов в воде различна:
ПР![]() =
1,6∙10-5;
ПР
=
1,6∙10-5;
ПР![]() =
1,7∙10-10,
ПР
=
1,7∙10-10,
ПР![]() =
2,0∙10-18.
=
2,0∙10-18.
Растворимость хлорида свинца с повышением температуры заметно растет, растворимость же остальных хлоридов при этом практически не меняется, что используется для отделения Pb2+ от остальных катионов первой группы.
Осадок хлорида серебра легко растворяется в растворах аммиака с образованием растворимого в воде комплексного соединения - хлорида диаминсеребра:
+++AgCl(тв ) + 2NH4OH = [Ag(NH3)2]Cl + 2H2O.
Хлорид ртути взаимодействует с раствором аммиака, образуя хлорид меркуроаммония [Hg(NH2)]Cl и металлическую ртуть, вследствие чего осадок чернеет:
Hg2Cl2(тв ) + 2NH4OH = [Hg(NH2)]Cl(тв) + Hg + NH4Cl + 2H2O.
2.2.1. Реакции катиона серебра
+++1. Реакции с галогенидами щелочных металлов.
Ag+ + Cl- = AgCl(тв) (белый осадок),
Ag+ + Br- = AgBr(тв) (бледно-желтый осадок),
Ag+ + I- = AgI(тв) (светло-желтый осадок).
С увеличением концентрации галогенид-ионов увеличивается растворимость галогенидов серебра в аммиаке из-за образования хорошо растворимых комплексных ионов [AgX2]- и [AgX4]3-. Причем, растворимость в водном растворе аммиака уменьшается в ряду AgCl, AgBr, AgI, что соответствует уменьшению величины произведения растворимости.
Методика проведения реакции. В три пробирки помещают по 3-4 капли раствора, содержащего ионы Ag+, добавляют по 2-3 капли 2 н. раствора HNO3. В первую пробирку добавляют 3-4 капли 2 н. HCl, во вторую - 3-4 капли раствора KBr, в третью - 3-4 капли раствора KI. Отмечают цвет образовавшихся осадков. Проверяют растворимость осадков в растворе гидроксида аммония.
2. Растворение галогенидов серебра в растворах KCN или Na2S2O3 за счет образования цианидных или тиосульфатных комплексов, более устойчивых по сравнению с аммиачными комплексами.
AgI + S2O32- = [AgS2O3]- + I-,
AgBr + 3CN- = [Ag(CN)3]2- + Br-.
+++3. Реакция с хроматом калия K2CrO4.
2Ag+ + CrO42- = Ag2CrO4(тв.).
Образуется кирпично-красный осадок хромата серебра, растворимый в азотной кислоте и гидроксиде аммония.
Методика проведения реакции. К 3 каплям раствора, содержащего ионы серебра, добавляют 3 капли раствора хромата калия. Наблюдают цвет образовавшегося осадка.
4. Реакция восстановления до металлического серебра при действии формальдегида на аммиачный раствор соли серебра. Ионы серебра в присутствии восстановителей (формальдегид, Mn2+, Sn2+) легко восстанавливаются до металлического серебра:
2[Ag(NH3)2]+ + НСНО + H2O = 2Ag + 3NH4+ + НСОО- + NH3.
При проведении реакции с формальдегидом на стенках пробирки образуется блестящий налет металлического серебра (реакция "серебряного зеркала").
Методика проведения реакции. В пробирки помещают 3 капли раствора, содержащего ионы Ag+, 3 капли раствора NH4OH, добавляют 3 капли 10%-ного раствора формальдегида и погружают пробирку в теплую воду. Наблюдают образование зеркала металлического серебра.
5. Реакция с дитизоном (С6H5)2CSN4H2. Дитизон образует с ионом Ag+ внутрикомплексное соединение, окрашенное в желтый цвет и экстрагируемое хлороформом или четыреххлористым углеродом:
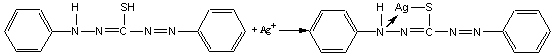 .
.
Методика проведения реакции. К 1-2 каплям анализируемого раствора добавляют 2-3 капли 2 н. раствора H2SO4 и экстрагируют 0,002%-ным раствором дитизона в CCl4. В присутствии ионов серебра органический слой окрашивается в желтый цвет. Определению мешают ионы Hg2+ и Cu2+, которые можно замаскировать, прибавив перед началом выполнения реакции раствор ЭДТА.
2.2.2. Реакции катиона диртути 2+
1. Реакции восстановления [Hg2]2+ до металлической ртути. Катион диртути 2+ способен восстанавливаться в присутствии восстановителей (SnCl2, Cu) до металлической ртути.
Hg22+ + Sn2+ = 2Hg (тв) + Sn4+;
Hg22+ + Cu = 2Hg (тв) + Cu2+.
Методика проведения реакций. а) К 2 каплям анализируемого раствора добавляют 2 капли раствора хлорида олова (II). Через минуту добавляют еще 2 капли реагента. Наблюдают выпадение осадка черного цвета. б) На медную пластинку наносят 2 капли раствора, содержащего ионы Hg22+. Через несколько минут пластинку промывают водой, протирают и наблюдают блестящее пятно ртути.
2. Реакция с иодидом калия KI.
Hg22+ + 2I- = Hg2I2 (тв).
Образуется грязно-зеленый осадок Hg2I2, растворимый в избытке реагента с образованием тетраиодомеркурата(II) калия и черного осадка металлической ртути:
Hg2I2 + 2KI = K2[HgI4] + Hg(тв).
Методика проведения реакции. К 3 каплям анализируемого раствора добавляют 3 капли раствора иодида калия. После образования грязно-зеленого осадка добавляют еще 5 капель иодида калия и наблюдают растворение зеленого и появление черного осадка.
3. Реакция со щелочами.
Hg22+ + 2OH- = HgO + Hg + H2O.
В результате реакции катион Hg22+ диспропорционирует на оксид ртути(II) и дисперсную ртуть черного цвета.
Методика проведения реакции. К 3 каплям раствора, содержащего ионы Hg22+, добавляют 3 капли раствора щелочи и наблюдают выпадение черного осадка.
4. Реакция с хроматом калия K2CrO4 .
Hg22+ + CrO42- = Hg2CrO4(тв).
Образуется осадок хромата ртути красного цвета, растворимый в азотной кислоте.
5. Реакция с соляной кислотой (люминесцентная реакция). Для обнаружения ртути (I) можно использовать реакцию образования каломели Hg2Cl2, способной люминесцировать оранжево-красным светом в ультрафиолетовом свете.
Методика проведения реакции. На предметное стекло наносят каплю раствора, содержащего ионы ртути (I), и каплю 2 н. HCl. Наблюдают оранжево-красное свечение в ультрафиолетовом свете.
