
- •Химический анализ
- •Часть 1. Качественный анализ неорганических веществ
- •Введение
- •1. Качественный анализ неорганических веществ
- •1.1. Методы и условия проведения качественного химического анализа
- •Классификация методов анализа в зависимости от количества исследуемого вещества
- •Методы разделения и концентрирования
- •1.2. Качественные аналитические реакции и аналитические признаки
- •1.3. Реактивы, применяемые в качественном анализе
- •Органические реактивы, используемые в качественном анализе
- •1.4. Аналитическая классификация ионов в качественном анализе
- •Аналитическая классификация анионов
- •Контрольные вопросы
- •2. Кислотно-основная аналитическая классификация катионов
- •2.1. Первая аналитическая группа катионов
- •2.1.1. Реакции катиона лития
- •4. Реакция с гексанитрокобальтатом(III) натрия Na3[Co(no2)6]:
- •2.1.3. Реакции катиона натрия
- •2.1.4. Реакции катиона калия
- •2. Реакция с гидротартратом натрия NaHc4h4o6.
- •3. Реакция с гексанитрокобальтатом(III) натрия Na3[Co(no2)6].
- •4. Реакция с гексанитрокупратом(II) свинца и натрия Na2Pb[Cu(no2)6].
- •Сводная таблица реакций катионов первой аналитической группы
- •2.2. Вторая аналитическая группа катионов
- •2.2.1. Реакции катиона серебра
- •2.2.3. Реакции катиона свинца(II)
- •Сводная таблица реакций катионов второй аналитической группы
- •2.3. Третья аналитическая группа катионов
- •2.3.1. Реакции катиона бария
- •2.3.2. Реакции катиона кальция
- •2.3.3. Реакции катиона стронция
- •Сводная таблица реакций катионов третьей аналитической группы
- •2.4. Четвёртая аналитическая группа катионов
- •2.4.1. Реакции катиона алюминия
- •2.4.2. Реакции катиона хрома (III)
- •2.4.3. Реакции катиона цинка
- •2.4.4. Реакции катионов олова(II) и (IV)
- •Сводная таблица реакций катионов четвертой аналитической группы
- •2.5. Пятая аналитическая группа катионов
- •2.5.3. Реакции катиона марганца (II)
- •2.5.4. Реакции катиона магния
- •2.5.5. Реакции катиона висмута (III)
- •2. Реакция с 8-оксихинолином c9h6n(он).
- •2.5.6. Реакции катиона сурьмы (III)
- •1. Реакция с тиосульфатом натрия Na2s2o3.
- •2.5.7. Реакции катиона сурьмы(V)
- •Сводная таблица реакций катионов пятой аналитической группы
- •2.6. Шестая аналитическая группа катионов
- •2.6.1. Реакции катиона меди (II)
- •2.6.2. Реакции катиона никеля(II)
- •2.6.3. Реакции катиона кобальта(II)
- •2.6.5. Реакции катиона ртути(II)
- •Сводная таблица реакций катионов шестой аналитической группы
- •Контрольные вопросы к разделу 2.1
- •Контрольные вопросы к разделу 2.2
- •Контрольные вопросы к разделу 2.3
- •Контрольные вопросы к разделу 2.4
- •Контрольные вопросы к разделу 2.5
- •Контрольные вопросы к разделу 2.6
- •3. Аналитическая классификация анионов
- •3.1. Анионы первой аналитической группы
- •3.1.1. Реакции хлорид - иона
- •3.1.2. Реакции бромид-иона
- •3.1.3. Реакции иодид-иона
- •3. Реакция окисления нитритом натрия:
- •3.1.4. Реакции сульфид-иона
- •5. Реакция с гидроксокомплексом свинца [Pb(oh)4 ]2-:
- •Качественные реакции анионов первой аналитической группы
- •3.2. Анионы второй аналитической группы
- •3.2.2. Реакции сульфит-иона
- •3.2.3. Реакции карбонат-иона
- •3.2.4. Реакции фосфат-иона
- •3.2.5. Реакции тиосульфат-иона
- •3.2.6. Реакции силикат-иона
- •3.2.7. Реакции борат-иона
- •Качественные реакции анионов второй аналитической группы
- •3.3. Анионы третьей аналитической группы
- •3.3.1. Реакции нитрат-иона
- •3.3.2. Реакции нитрит-иона
- •2. Реакция с иодидом калия ki.
- •Качественные реакции анионов третьей аналитической группы
- •Контрольные вопросы к разделу 3.1
- •Контрольные вопросы к разделу 3.2
- •Контрольные вопросы к разделу 3.3
- •4. Качественный анализ неизвестного вещества
- •4.1. Предварительные испытания
- •Предварительные испытания неизвестного вещества
- •4.2. Анализ индивидуальной соли
- •4.3. Систематический анализ смеси катионов
- •4.3.2. Систематический ход анализа (один из вариантов).
- •6. Анализ раствора 4 (V группа). Аммиакат меди – синий, никеля – сине-голубой, кобальта – желтый.
- •Контрольные вопросы
- •Список литературы
- •Химический анализ
- •Часть 1. Качественный анализ неорганических веществ
2.5.3. Реакции катиона марганца (II)
1. Реакция окисления висмутатом натрия NaBiO3:
2Mn2+ + 5BiO3- + 14H+ = 2MnO4- + 5Bi3+ + 7H2O.
Висмутат натрия окисляет ионы Mn2+ до MnO4- фиолетово-красного цвета. Определению мешают восстановители (в том числе и хлорид-ионы) и большие количества Mn2+, поэтому перед выполнением реакции исследуемый раствор разбавляют водой.
Методика проведения реакции. К капле раствора марганца (II) прибавляют каплю концентрированной азотной кислоты, 3-4 капли воды и немного твердого висмутата натрия. Раствор окрашивается в фиолетово-красный цвет.
2. Реакция окисления пероксодисульфатом аммония (NH4)2S2O8. Окисление пероксодисульфатом аммония проводят в кислой среде в присутствии катализатора AgNO3.
2Mn2+ + 5S2O82- + 8H2O = 2MnO4- + 10SO42- + 16H+.
Методика проведения реакции. К 5-6 каплям раствора (NH4)2S2O8 прибавляют каплю 2 М H2SO4, 1-2 капли концентрированной H3PO4, 1-2 капли AgNO3 и нагревают. В нагретую окислительную смесь вносят с помощью стеклянной палочки минимальное количество раствора, содержащего ионы Mn2+ и не содержащего хлорид-ионы. Наблюдают появление фиолетовой окраски раствора.
2.5.4. Реакции катиона магния
1. Реакция с гидрофосфатом натрия Na2HPO4. Реакцию проводят в присутствии NH4Cl, который препятствует образованию аморфного осадка Mg(OH)2, растворяющегося в присутствии NH4Cl. В результате реакции образуется белый кристаллический осадок двойной соли фосфата магния-аммония. Осадок имеет характерное строение.
Mg2+ + HPO42- + NH4OH = MgNH4PO4(тв)+ H2O.
Методика проведения реакции. К 3 каплям раствора соли магния добавляют 4 капли раствора Na2HPO4, 3 капли раствора HCl и по каплям медленно добавляют раствор гидроксида аммония до образования кристаллического осадка. Реакцию можно проводить на предметном стекле и наблюдать в микроскоп форму образовавшихся кристаллов.
2. Реакция с 8-оксихинолином C9H6N(ОН). В присутствии аммиака образуется зеленовато-желтый кристаллический осадок оксихинолята магния. Реакция выполняется при нагревании. Мешают катионы других групп, кроме II и III.
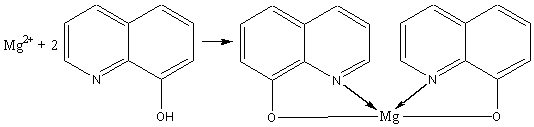 .
.
Методика проведения реакции. К 3 каплям раствора соли магния добавляют каплю раствора фенолфталеина и по каплям 2 н. раствора NH4OH до появления розовой окраски, затем нагревают до кипения и добавляют 3-4 капли раствора 8-оксихинолина.
3. Реакция с магнезоном I C12H7N2NO2(OH)2. Магнезон I (п-нитробензолазорезорцин) способен адсорбироваться на осадке гидроксида магния, меняя при этом красную окраску на синюю. Осадок гидроксида магния окрашивается в синий цвет (в случае малых количеств магния синюю окраску приобретает раствор). Реакции мешают катионы Ni2+, Cd2+, Co2+, гидроксиды которых также окрашиваются магнезоном.
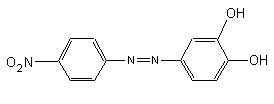
Методика проведения реакции. На предметное стекло наносят каплю раствора соли магния и каплю щелочного раствора магнезона. Появляется синяя окраска или синий осадок.
