
- •Химический анализ
- •Часть 1. Качественный анализ неорганических веществ
- •Введение
- •1. Качественный анализ неорганических веществ
- •1.1. Методы и условия проведения качественного химического анализа
- •Классификация методов анализа в зависимости от количества исследуемого вещества
- •Методы разделения и концентрирования
- •1.2. Качественные аналитические реакции и аналитические признаки
- •1.3. Реактивы, применяемые в качественном анализе
- •Органические реактивы, используемые в качественном анализе
- •1.4. Аналитическая классификация ионов в качественном анализе
- •Аналитическая классификация анионов
- •Контрольные вопросы
- •2. Кислотно-основная аналитическая классификация катионов
- •2.1. Первая аналитическая группа катионов
- •2.1.1. Реакции катиона лития
- •4. Реакция с гексанитрокобальтатом(III) натрия Na3[Co(no2)6]:
- •2.1.3. Реакции катиона натрия
- •2.1.4. Реакции катиона калия
- •2. Реакция с гидротартратом натрия NaHc4h4o6.
- •3. Реакция с гексанитрокобальтатом(III) натрия Na3[Co(no2)6].
- •4. Реакция с гексанитрокупратом(II) свинца и натрия Na2Pb[Cu(no2)6].
- •Сводная таблица реакций катионов первой аналитической группы
- •2.2. Вторая аналитическая группа катионов
- •2.2.1. Реакции катиона серебра
- •2.2.3. Реакции катиона свинца(II)
- •Сводная таблица реакций катионов второй аналитической группы
- •2.3. Третья аналитическая группа катионов
- •2.3.1. Реакции катиона бария
- •2.3.2. Реакции катиона кальция
- •2.3.3. Реакции катиона стронция
- •Сводная таблица реакций катионов третьей аналитической группы
- •2.4. Четвёртая аналитическая группа катионов
- •2.4.1. Реакции катиона алюминия
- •2.4.2. Реакции катиона хрома (III)
- •2.4.3. Реакции катиона цинка
- •2.4.4. Реакции катионов олова(II) и (IV)
- •Сводная таблица реакций катионов четвертой аналитической группы
- •2.5. Пятая аналитическая группа катионов
- •2.5.3. Реакции катиона марганца (II)
- •2.5.4. Реакции катиона магния
- •2.5.5. Реакции катиона висмута (III)
- •2. Реакция с 8-оксихинолином c9h6n(он).
- •2.5.6. Реакции катиона сурьмы (III)
- •1. Реакция с тиосульфатом натрия Na2s2o3.
- •2.5.7. Реакции катиона сурьмы(V)
- •Сводная таблица реакций катионов пятой аналитической группы
- •2.6. Шестая аналитическая группа катионов
- •2.6.1. Реакции катиона меди (II)
- •2.6.2. Реакции катиона никеля(II)
- •2.6.3. Реакции катиона кобальта(II)
- •2.6.5. Реакции катиона ртути(II)
- •Сводная таблица реакций катионов шестой аналитической группы
- •Контрольные вопросы к разделу 2.1
- •Контрольные вопросы к разделу 2.2
- •Контрольные вопросы к разделу 2.3
- •Контрольные вопросы к разделу 2.4
- •Контрольные вопросы к разделу 2.5
- •Контрольные вопросы к разделу 2.6
- •3. Аналитическая классификация анионов
- •3.1. Анионы первой аналитической группы
- •3.1.1. Реакции хлорид - иона
- •3.1.2. Реакции бромид-иона
- •3.1.3. Реакции иодид-иона
- •3. Реакция окисления нитритом натрия:
- •3.1.4. Реакции сульфид-иона
- •5. Реакция с гидроксокомплексом свинца [Pb(oh)4 ]2-:
- •Качественные реакции анионов первой аналитической группы
- •3.2. Анионы второй аналитической группы
- •3.2.2. Реакции сульфит-иона
- •3.2.3. Реакции карбонат-иона
- •3.2.4. Реакции фосфат-иона
- •3.2.5. Реакции тиосульфат-иона
- •3.2.6. Реакции силикат-иона
- •3.2.7. Реакции борат-иона
- •Качественные реакции анионов второй аналитической группы
- •3.3. Анионы третьей аналитической группы
- •3.3.1. Реакции нитрат-иона
- •3.3.2. Реакции нитрит-иона
- •2. Реакция с иодидом калия ki.
- •Качественные реакции анионов третьей аналитической группы
- •Контрольные вопросы к разделу 3.1
- •Контрольные вопросы к разделу 3.2
- •Контрольные вопросы к разделу 3.3
- •4. Качественный анализ неизвестного вещества
- •4.1. Предварительные испытания
- •Предварительные испытания неизвестного вещества
- •4.2. Анализ индивидуальной соли
- •4.3. Систематический анализ смеси катионов
- •4.3.2. Систематический ход анализа (один из вариантов).
- •6. Анализ раствора 4 (V группа). Аммиакат меди – синий, никеля – сине-голубой, кобальта – желтый.
- •Контрольные вопросы
- •Список литературы
- •Химический анализ
- •Часть 1. Качественный анализ неорганических веществ
2.3.2. Реакции катиона кальция
1. Окрашивание пламени. Пламя горелки при внесении солей кальция окрашивается в кирпично-красный цвет.
2. Реакция с оксалатом аммония (NH4)2C2O4.
Ca2+ + C2O42- = CaC2O4(тв).
Оксалат аммония образует с ионами кальция кристаллический осадок CaC2O4 ∙5H2O. Осадок растворяется в сильных кислотах, но нерастворим в уксусной кислоте (в отличие от оксалатов стронция и бария).
Методика проведения реакции. К 2-3 каплям раствора, содержащего ионы кальция, добавляют 2-3 капли раствора оксалата аммония. Выпадает белый кристаллический осадок. Растворимость осадка проверяют в уксусной, а затем в соляной кислотах.
+++3. Реакция с гексацианоферратом(II) калия K4[Fe(CN)6].
Ca2+ + [Fe(CN)6]4- + 2NH4OH = Ca(NH4)2[Fe(CN)6] (тв) + 2OH-.
В слабощелочной
среде (рН![]() 9)
образуется белый кристаллический
осадок смешанной кальций-аммонийной
соли, растворимой в минеральных кислотах,
но нерастворимой в уксусной кислоте.
Реакцию проводят в присутствии аммиачной
буферной смеси. Ионы Sr2+
этим реактивом не осаждаются. Ионы Ba2+
должны быть предварительно удалены.
9)
образуется белый кристаллический
осадок смешанной кальций-аммонийной
соли, растворимой в минеральных кислотах,
но нерастворимой в уксусной кислоте.
Реакцию проводят в присутствии аммиачной
буферной смеси. Ионы Sr2+
этим реактивом не осаждаются. Ионы Ba2+
должны быть предварительно удалены.
Методика проведения реакции. На предметном стекле перемешивают 2-3 капли раствора, содержащего ионы кальция, с 2-3 каплями раствора NH4OH, нагревают до 60-700С и добавляют 3 капли раствора гексацианоферрата(II) калия.
4. Микрокристаллоскопическая реакция с серной кислотой H2SO4. В разбавленных растворах ион кальция образует с серной кислотой характерные игольчатые кристаллы CaSO4.2H2O. Мешают проведению реакции ионы Pb2+, Ba2+, Sr2+, если они присутствуют в 10-кратном по отношению к ионам кальция избытке.
Методика проведения реакции. На предметное стекло помещают каплю раствора соли кальция, рядом помещают каплю H2SO4 (1:4). Стеклянной палочкой соединяют капли, дают постоять и рассматривают под микроскопом кристаллы, образовавшиеся по краям капли.
2.3.3. Реакции катиона стронция
1. Окрашивание пламени. Летучие соли стронция окрашивают пламя горелки в карминово-красный цвет.
2. Реакция с родизонатом натрия Na2C6O6.
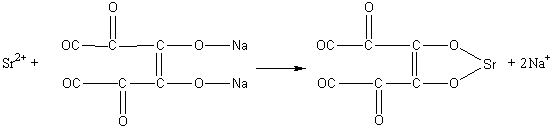
При проведении этой реакции на фильтровальной бумаге образуется красно-бурое окрашивание осадка родизоната стронция, исчезающее в присутствии соляной кислоты. Если в растворе присутствуют ионы бария, то реакцию проводят, предварительно добавляя хромат-ионы.
Методика проведения реакции. На фильтровальную бумагу наносят каплю раствора хромата калия, затем каплю исследуемого раствора, содержащего ионы стронция. Выдерживают бумагу в течение 2-3 минут и добавляют каплю раствора родизоната натрия. В присутствии ионов стронция бумага окрашивается в буро-красный цвет, при их отсутствии остается желтой.
Некоторые реакции катионов третьей аналитической группы приведены в табл. 7.
Таблица 7
Сводная таблица реакций катионов третьей аналитической группы
Реактив |
Ca2+ |
Sr2+ |
Ba2+ |
H2SO4 |
CaSO4 ↓ белый осадок, растворим в (NH4)2SO4 |
SrSO4 ↓ белый осадок, растворим в конц. H2SO4 |
BaSO4 ↓ белый осадок, растворим в конц. H2SO4 |
K2CrO4 |
- |
SrCrO4 ↓ желтый осадок, растворим в HCl, HNO3, CH3COOH |
BaCrO4 ↓ желтый осадок, растворим в HNO3, HCl, нерастворим в CH3COOH |
K2Cr2O7 |
- |
- |
BaCrO4 ↓ желтый осадок, растворим в HNO3, HCl |
(NH4)2C2O4 |
CaC2O4 ↓ белый осадок, растворим в HCl, HNO3 ,нераств. в CH3COOH (гор.) |
SrC2O4 ↓ белый осадок, растворим в HCl, HNO3, CH3COOH (гор.) |
BaC2O4 ↓ белый осадок, растворим в HCl, HNO3, CH3COOH (гор.) |
Na2HPO4 |
CaHPO4 ↓ белый осадок, растворим в HCl, HNO3, CH3COOH |
SrHPO4 ↓ белый осадок, растворим в HCl, HNO3, CH3COOH |
BaHPO4 ↓ белый осадок, растворим в HCl, HNO3, CH3COOH |
(NH4)2CO3 |
CaCO3 ↓ белый осадок, растворим в HCl, HNO3, CH3COOH |
SrCO3 ↓ белый осадок, растворим в HCl, HNO3, CH3COOH |
BaCO3 ↓ белый осадок, растворим в HCl, HNO3, CH3COOH |
CaSO4 |
- |
SrSO4 ↓ белый осадок |
BaSO4 ↓ белый осадок |
K4[Fe(CN)6] |
CaK2[Fe(CN)6] ↓ белый осадок, растворим в HCl, HNO3 |
- |
BaK2[Fe(CN)6] ↓ белый осадок, растворим в HCl, HNO3 |
Родизонат натрия |
CaC6O6.Ca(OH)2 ↓ фиолетовый осадок, растворим в HCl |
SrC6O6 ↓ красно-бурый осадок, растворим в HCl |
BaC6O6 ↓ красно-бурый осадок, краснеет в HCl |
Окрашивание пламени |
Кирпично-красный цвет |
Карминово-красный цвет |
Желто-зеленый цвет |
