
- •Часть 1
- •Введение
- •Лекция 1 единицы и размерности физических величин
- •Системы единиц измерения. Элементы теории ошибок
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 2 основы механики.
- •2.1 Кинематика точки
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 3 динамика
- •3.1 Законы Ньютона
- •3.2 Физическая природа сил
- •3.3 Масса и импульс
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 4 законы сохранения. Работа и мощность.Энергия.
- •4.1 Закон сохранения импульса и центра масс
- •4.2 Работа и мощность
- •4.3 Виды энергии
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция № 5 твердое тело в механике.Вращательное движение.
- •5.1 Вращательное движение
- •5.2 Момент инерции. Момент импульса
- •5.3 Уравнение динамики вращательного движения
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 6. Колебания
- •Кинематика гармонических колебаний. Механические волны.
- •(Уравнения гармонического колебания)
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция № 7 Гидростатика и гидродинамика
- •7.1.Давление в жидкости. Законы Паскаля и Архимеда
- •Уравнения течения жидкости
- •Формулировка уравнения Бернулли:
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция № 8 Молекулярно-кинетическая теория строения вещества.
- •8.1 Основные положения мкт
- •8.2 Внутренняя энергия молекул.
- •Вопросы для самоконтроля.
- •Список литературы Основная
- •Дополнительная
- •Лекция 9
- •9.1 Плавление, кристаллизация, парообразование, конденсация.
- •9.2 Свойства жидкости
- •Список литературы Основная
- •Дополнительная
- •Лекция 10 идеальные и реальные газы.
- •1 Уравнение идеального газа. Экспериментальные газовые законы
- •10.2 Уравнение Ван-дер-Ваальса
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция №11 явления переноса
- •Теплопроводность.
- •Диффузия
- •Внутреннее трение (вязкость)
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 12 основы термодинамики.
- •12.1 Общие понятия. Первое начало термодинамики
- •12.2 Работа, совершаемая при изменении объема
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 13 обратимые и необратимые тепловые процессы.
- •13.1 Второе начало термодинамики
- •13.2 Цикл Карно
- •13.3 Энтропия
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 14 электростатика.
- •14.1 Взаимодействие электрических зарядов. Закон кулона
- •14.2 Напряженность поля
- •14.3 Теорема Остроградского-Гаусса
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 15 потенциал электрического поля. Электроемкость.
- •15.1 Потенциал и работа электрического поля.
- •15.2 Проводники и диэлектрики в электрическом поле
- •15.3 Вектор электрической индукции
- •15.4 Электрическая емкость. Энергия электрического поля
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 16 постоянный электрический ток
- •16.1.Электрический ток. Сила тока, э.Д.С., напряжение
- •16.2 Сопротивление проводников
- •16.3 Законы Ома и Джоуля-Ленца
- •16.4 Правила Кирхгофа
- •Список литературы Основная
- •Дополнительная
- •Лекция 17 ток в жидкостях и газах
- •17.1Электролиз.
- •17.2 Самостоятельный и несамостоятельный газовые разряды
- •Вопросы для самоконтроля.
- •Список литературы Основная
- •Дополнительная
- •Лекция 18 термоэлектрические явления.
- •18.1 Электронная лампа диод и ее применение
- •18.2 Электронная лампа триод
- •18.3 Контактная разность потенциалов. Термоэлектричество
- •Контактная разность потенциалов двух металлов зависит только от их химического состава и температуры.
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Библиографический список
- •Содержание
12.2 Работа, совершаемая при изменении объема
Определим работу, совершаемую газом при изменении объема. Пусть газ расширяется под поршнем от V1 при давлении P1, до объема V2 при давлении P2.(см.рис.36).
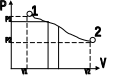 Этот
процесс на графике изображается кривой
1-2. Рассмотрим малый интервал расширения,
Этот
процесс на графике изображается кривой
1-2. Рассмотрим малый интервал расширения,
![]() для которого давление P
можно считать постоянным. Элементарная
работа при малом перемещении поршня
будет равна A=p*V.
для которого давление P
можно считать постоянным. Элементарная
работа при малом перемещении поршня
будет равна A=p*V.
Очевидно, что полная работа A, совершаемая при изменении объема газа, численно равна сумме площадей всех «n» полосок, т.е. работа графически изображена площадью фигуры, ограниченной снизу осью абсцисс, сверху кривой 1-2, а слева и справа ординатами P1 и P2. При переходе к бесконечно малым интервалам dA=pdV(3).
Интегрируя в пределах от V1 до V2 получим полную работу при изменении объема.
![]() .(4).
.(4).
Рисунок 36
Рассмотрим работу, совершаемую при изотермическом, изобарическом, изохорическом и адиабатическом процессах:
Изохорический процесс. Объем газа остается постоянным(V=const),следовательно газ не совершает работы А=0. и согласно 1 началу термодинамики Q=U. Вся сообщенная газу теплота затрачивается на U, т.е. на нагревание газа. График его изображен в виде прямой на рис.4
Изотермический процесс. T=const.Когда моль идеального газа изменяет свой объем. Из уравнения Клапейрона-Менделеева pV=RT отсюда
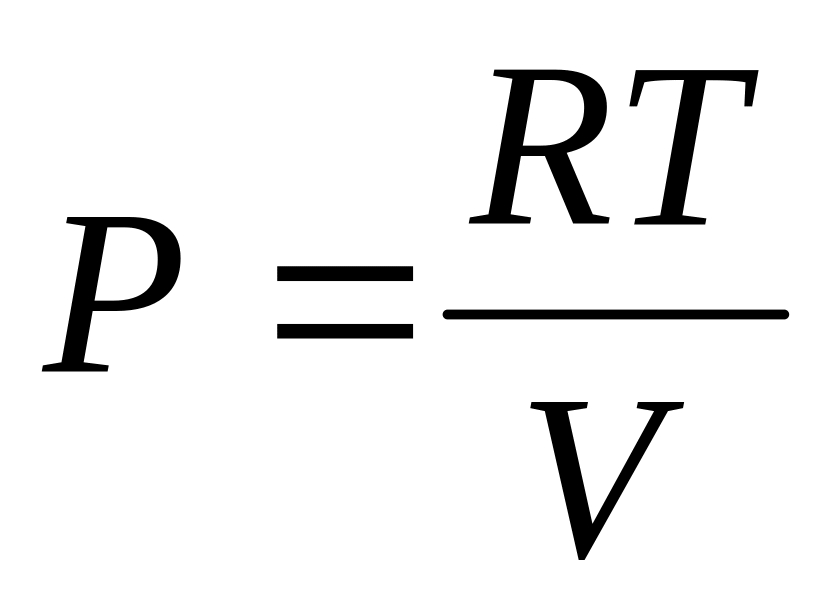 ,которое подставим в формулу(4), получим
,которое подставим в формулу(4), получим
![]() ,
,![]() -
работа 1 моль газа.
-
работа 1 моль газа.
Для
любой массы газа
![]()
3). Изобарический процесс. P=const. Газ нагревается и совершает работу против внешних сил. Q=U+A=U+pV. т.е. сообщаемая газу теплота затрачивается на увеличение внутренней энергии объема от V1 до V2 равна
![]() .
.
4) Адиабатический процесс, наз. Процесс, происходящий при отсутствии теплообмена
между системой и окружающей средой.Q=0. Следовательно «–U=A» система совершает работу за счет своей внутренней энергии. Расширение газа вызывает его охлаждение, сжатие (внешними силами)-нагревание. Выведем уравнение, связывающие параметры газа при адиабатических процессах. Рассмотрим адиабатический процесс в системе:1 моля идеального газа помещен в цилиндр, стенки и поршень которого абсолютно нетеплопроводные. Известно, что внутренняя dU=Cv*dT(9), тогда первое начало термодинамики можно записать так CvdT+pdV=0(10),
Определив из
уравнения Клапейрона-Менделеева давление
p
и подставив в равенство (10), получим
![]() .
Разделим обе части данного равенства
на СvT
имеем
.
Разделим обе части данного равенства
на СvT
имеем
![]() .
Интегрируя последние равенство в
пределах от V1
до V2
и соответственно от T1
до T2
получим
.
Интегрируя последние равенство в
пределах от V1
до V2
и соответственно от T1
до T2
получим
![]() ,откуда
,откуда
![]() или
или
![]() учитывая ,что Ср=Сv+R
и
учитывая ,что Ср=Сv+R
и
![]() имеем
имеем
![]() .
Проинтегрируя, получим
.
Проинтегрируя, получим
![]() или T1*
или T1*![]()
![]() или
или
![]() .
Уравнение выражает закон Пуассона из
него следует, что при адиабатическом
расширение газа его температура
понижается, а при сжатии-повышается.
.
Уравнение выражает закон Пуассона из
него следует, что при адиабатическом
расширение газа его температура
понижается, а при сжатии-повышается.
Адиабатический процесс в больших массах - это образование кучевых облаков.
Закон Пуассона
примет другой вид, если выразить
температуру через давление согласно
уравнению Клайперона-Менделеева имеем
![]() подставив последнее в формулу получим
подставив последнее в формулу получим
![]() =const
так как R
=const
так как R![]() const=const.
const=const.

![]()
 - закон Пуассона.
- закон Пуассона.
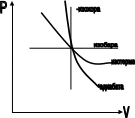
Рисунок 37
Уравнение Пуассона связывает между собой изменения объема и давления газа. График процесса представлен на рис.37. Адиабата идет круче изотермы,т.к. при изотермическом расширении давления газа уменьшается за счет увеличения объема, так и за
счет понижения температуры. При адиабатическом процессе температура газа изменится от Т1 до Т2. Газ совершает работу. Зная, что при адиабатическом процессе dA=-dU и внутренняя энергия моля идеального газа равна dU=Cv*dT где Сv-малярная
теплоемкость при
объеме. Объединив эти формулы, получим
dA=-CvdT,интегрируя
найдем
![]() или
A=Cv(T1-T2).
Работа совершаемая газом при адиабатическом
процессе, пропорциональна изменению
температуры газа.
или
A=Cv(T1-T2).
Работа совершаемая газом при адиабатическом
процессе, пропорциональна изменению
температуры газа.
