
- •Часть 1
- •Введение
- •Лекция 1 единицы и размерности физических величин
- •Системы единиц измерения. Элементы теории ошибок
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 2 основы механики.
- •2.1 Кинематика точки
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 3 динамика
- •3.1 Законы Ньютона
- •3.2 Физическая природа сил
- •3.3 Масса и импульс
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 4 законы сохранения. Работа и мощность.Энергия.
- •4.1 Закон сохранения импульса и центра масс
- •4.2 Работа и мощность
- •4.3 Виды энергии
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция № 5 твердое тело в механике.Вращательное движение.
- •5.1 Вращательное движение
- •5.2 Момент инерции. Момент импульса
- •5.3 Уравнение динамики вращательного движения
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 6. Колебания
- •Кинематика гармонических колебаний. Механические волны.
- •(Уравнения гармонического колебания)
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция № 7 Гидростатика и гидродинамика
- •7.1.Давление в жидкости. Законы Паскаля и Архимеда
- •Уравнения течения жидкости
- •Формулировка уравнения Бернулли:
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция № 8 Молекулярно-кинетическая теория строения вещества.
- •8.1 Основные положения мкт
- •8.2 Внутренняя энергия молекул.
- •Вопросы для самоконтроля.
- •Список литературы Основная
- •Дополнительная
- •Лекция 9
- •9.1 Плавление, кристаллизация, парообразование, конденсация.
- •9.2 Свойства жидкости
- •Список литературы Основная
- •Дополнительная
- •Лекция 10 идеальные и реальные газы.
- •1 Уравнение идеального газа. Экспериментальные газовые законы
- •10.2 Уравнение Ван-дер-Ваальса
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция №11 явления переноса
- •Теплопроводность.
- •Диффузия
- •Внутреннее трение (вязкость)
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 12 основы термодинамики.
- •12.1 Общие понятия. Первое начало термодинамики
- •12.2 Работа, совершаемая при изменении объема
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 13 обратимые и необратимые тепловые процессы.
- •13.1 Второе начало термодинамики
- •13.2 Цикл Карно
- •13.3 Энтропия
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 14 электростатика.
- •14.1 Взаимодействие электрических зарядов. Закон кулона
- •14.2 Напряженность поля
- •14.3 Теорема Остроградского-Гаусса
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 15 потенциал электрического поля. Электроемкость.
- •15.1 Потенциал и работа электрического поля.
- •15.2 Проводники и диэлектрики в электрическом поле
- •15.3 Вектор электрической индукции
- •15.4 Электрическая емкость. Энергия электрического поля
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Лекция 16 постоянный электрический ток
- •16.1.Электрический ток. Сила тока, э.Д.С., напряжение
- •16.2 Сопротивление проводников
- •16.3 Законы Ома и Джоуля-Ленца
- •16.4 Правила Кирхгофа
- •Список литературы Основная
- •Дополнительная
- •Лекция 17 ток в жидкостях и газах
- •17.1Электролиз.
- •17.2 Самостоятельный и несамостоятельный газовые разряды
- •Вопросы для самоконтроля.
- •Список литературы Основная
- •Дополнительная
- •Лекция 18 термоэлектрические явления.
- •18.1 Электронная лампа диод и ее применение
- •18.2 Электронная лампа триод
- •18.3 Контактная разность потенциалов. Термоэлектричество
- •Контактная разность потенциалов двух металлов зависит только от их химического состава и температуры.
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Дополнительная
- •Библиографический список
- •Содержание
Вопросы для самоконтроля
Что такое термодинамическая система, термодинамический процесс?
Сформулируйте первое начало термодинамики и его уравнение .
Напишите общие выражение работы А при изменении объема газа (от V1 до V2).
Какие процессы называются адиабатическими? Напишите уравнение Пуассона.
Чему равна работа, совершаемая газом при изохорическом, изотермическом, изобарическом и адиабатическом процессах?
Почему на графике с координатными осями Р и V адиабата идет круче изотермы?
Список литературы Основная
1. Грабовский Р.И. Курс физики / Р. И. Грабовский. – СПб.; Издательство «Лань», 2002.-608 с.
2. Пронин В.П. Краткий курс физики / В.П. Пронин. – Саратов: ФГОУ ВПО «Саратовский ГАУ», 2007 г. – 200 с.
3. Трофимова Т.И. Курс физики / Т.И. Трофимова. – М.: «Высшая школа». 2003 г. – 350с.
Дополнительная
1.Матвеев А.Н. Механика и теория относительности. Учебное пособие/ С.-Петербург: Издательство «Лань», 2009г. 500экз.
2.Рогачев Н.М. Курс физики. Учебное пособие// С.-Петербург: Издательство «Лань», 2010г.- 448с. 1000 экз.
3.Трофимова Т.И.Физика в таблицах.. М.: «Высшая школа». 2008г
Лекция 13 обратимые и необратимые тепловые процессы.
13.1 Второе начало термодинамики
Важное значение в термодинамике имеют так называемые круговые процессы (циклы).Круговым процессом (циклом) называется процесс , в результате которого, система пройдя ряд состояний возвращается в исходное состояние. Круговой процесс является обратимым, если все его части обратимы. Если же какая-либо часть кругового процесса является необратимой, то и весь процесс необратим.
Термодинамикой называется раздел физики, в котором изучаются закономерности тепловой формы движения материи.
Термодинамической системой называется совокупность тел, которые могут обмениваться между собой и с внешней средой и веществом и энергией.
Изолированная термодинамическая система – такая, в которой обмен с окружающей средой не происходит.
Открытая система – обмен с окружающей средой и энергией и веществом.(живой организм).
Состояние системы определяется совокупностью ее параметров: V, Т, р и т.д. При взаимодействии системы с внешними телами ее параметры изменяются.
Равновесным состоянием (термическое равновесие) называется такое состояние системы, в которое она самопроизвольно (спонтанно) переходит через достаточно большой промежуток времени при условии изоляции от окружающей среды.
В состоянии равновесия параметры системы не меняются со временем. Процесс установления термического равновесия носит название релаксации. Примером неравновесной системы является газ в цилиндре при быстром сжатии. При отсутствии внешних воздействий изолированная система не может самопроизвольно выйти из равновесного состояния.
![]()
Теплота, сообщаемая системе, расходуется на изменение внутренней энергии и на работу, совершаемую силами, приложенными со стороны системы к внешним телам.
Н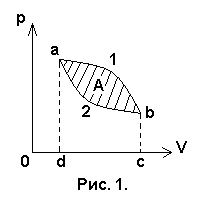 а
графике равновесный процесс изображается
замкнутой кривой (рис. 38). Совершаемая
за цикл работа равна разности работ,
совершенных по часовой стрелке (при
расширении) – А1
и против часовой стрелки (при сжатии) –
А2.
Работа А1
численно равна площади фигуры da1bc
(положительна). А работа А2
(отрицательна) – площади фигуры da2bc:
а
графике равновесный процесс изображается
замкнутой кривой (рис. 38). Совершаемая
за цикл работа равна разности работ,
совершенных по часовой стрелке (при
расширении) – А1
и против часовой стрелки (при сжатии) –
А2.
Работа А1
численно равна площади фигуры da1bc
(положительна). А работа А2
(отрицательна) – площади фигуры da2bc:
А=А1-А2
Рисунок 38
