
- •«Вятский государственный университет»
- •Биоорганическая химия в технологии защиты биосферы
- •Оглавление
- •3. Реакция присоединения галогенов за счёт двойных связей в остатках непредельных кислот. 80
- •Биоорганическая химия Предмет биоорганической химии
- •Углеводы
- •Моносахариды
- •Генетический d-ряд альдотриоз, тетроз, пентоз
- •Пентозы с5н10о5
- •Получение моносахаридов
- •Физические свойства моносахаридов
- •Химические свойства моносахаридов
- •Дисахариды (биозы)
- •Общие химические свойства дисахаридов
- •Собственно полисахариды
- •Крахмал
- •Химические свойства
- •Целлюлоза (клетчатка)
- •Химические свойства
- •Химическая переработка целлюлозы
- •Аминокислоты
- •Изомерия
- •Получение
- •Физические свойства
- •Химические свойства
- •Пептиды, белки
- •Химические свойства
- •Ферменты
- •Понятие о нуклеиновых кислотах
- •Моноглицериды
- •Диглицериды
- •Триглицериды
- •Предельные жирные кислоты
- •Непредельные жирные кислоты
- •Физические свойства
- •Химические свойства
- •Сложные жиры
- •Стерины
- •Гормоны и медиаторы
- •Лабораторный практикум Моносахариды Реакции на гидроксильные группы в моносахаридах
- •Реакции на карбонильные группы в моносахаридах
- •Осмоление моносахаридов
- •Цветные реакции на моносахариды
- •Дисахариды Реакции на гидроксильные группы дисахаридов
- •Реакции дисахаридов по карбонильным группам (сравнение свойств восстанавливающих и невосстанавливающих дисахаридов)
- •Гидролиз (инверсия) сахарозы
- •Реакции сахарозы с сульфатами никеля и кобальта
- •Высшие полисахариды Качественные реакции на углеводы
- •Кислотный гидролиз крахмала
- •Свойства целлюлозы
- •Некоторые свойства хлопкового и искусственных волокон
- •Аминокислоты Свойства аминокислот
- •Свойства шерсти и синтетических волокон
- •Цветные рекции на белки
- •Биуретовая реакция
- •Ксантопротеиновая реакция
- •Реакция на триптофан (реакция Шульце-Распайля)
- •Реакция Адамкевича
- •Реакция на серусодержащие аминокислоты
- •Реакция Фоля на серусодержащие аминокислоты
- •Библиографический список
- •Биоорганическая химия в технологии защиты биосферы
Пентозы с5н10о5
К наиболее важным в природе представителям пентоз С5Н10О5 можно отнести D-ксилозу, D-рибозу, D-арабинозу, 2-дезокси-D-рибозу.

D-ксилоза
D-рибоза
D-арабиноза
2-дезокси-
D-рибоза
D-ксилоза в большом количестве входит в состав полисахаридов древесины. Гидролизаты, содержащие ксилозу, используются для выращивания кормовых дрожжей. При нагревании в присутствие минеральных кислот ксилоза превращается в фурфурол, при гидрировании – в ксилит.
D-рибоза входит в состав рибонуклеиновых кислот, витаминов, энзимов.
2-дезокси-D-рибоза входит в состав дезоксирибонуклеиновых кислот ДНК, которые играют основную роль в передаче наследственных признаков.
Получение моносахаридов
В свободном виде в природе встречается преимущественно глюкоза. Она же является структурной единицей большинства полисахаридов. Другие моносахариды в свободном состоянии встречаются редко и в основном известны как компоненты олиго- и полисахаридов. В природе глюкоза получается в результате реакции фотосинтеза:
hν
6 CO2
+ 6H2O
C6H12O6(глюкоза)
+ 6O2
CO2
+ 6H2O
C6H12O6(глюкоза)
+ 6O2
Впервые глюкоза получена в 1811 году русским химиком Г.Э. Кирхгофом при гидролизе крахмала. Позже её синтез из формальдегида в щелочной среде был предложен А.М. Бутлеровым:
O II Ca(OH)2
6 I H |
В промышленности глюкозу получают гидролизом крахмала в присутствии серной кислоты:
Н2 SO4, tº
(C6H10O5)n (крахмал) + nH2O → nC6H12O6 (глюкоза)
Физические свойства моносахаридов
Моносахариды – бесцветные кристаллические вещества, хорошо растворимые в воде, плохо – в спирте и совсем не растворимые в эфире и других малополярных растворителях. Оптически активны. Плавятся с разложением, не перегоняются даже в глубоком вакууме. Водные растворы имеют нейтральную реакцию на лакмус. Большинство моносахаридов обладает сладким вкусом, однако меньшим, чем свекловичный сахар.
Химические свойства моносахаридов
Моносахариды проявляют свойства и спиртов, и карбонильных соединений. Реакции, обусловленные наличием карбонильной группы, – это окисление, восстановление, присоединение синильной кислоты, образование оксимов, образование озазонов при взаимодействии с фенилгидразином, взаимодействие с щёлочью.
Окисление. Очень слабые окислители затрагивают только альдегидную группу и превращают альдозы в альдоновые кислоты. При окислении глюкозы аммиачным раствором гидроксида серебра образуется глюконовая кислота (реакция «серебряного зеркала»):

Реакции моносахаридов с гидроксидом меди при нагревании также приводят к альдоновым кислотам.
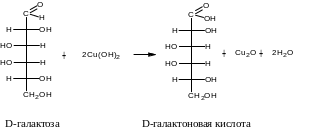

фруктоза
гликолевая
кислота
триоксимасляная
кислота
Более сильные окислительные средства окисляют в карбоксильную группу не только альдегидную, но и первичную спиртовую группы, приводя к образованию двухосновных сахарных (альдаровых) кислот. Обычно для такого окисления используют концентрированную азотную кислоту:


Восстановление. При восстановлении моноз получаются полиолы, называемые сахарными спиртами. Так, из глюкозы и фруктозы получают шестиатомный спирт сорбит, из маннозы – маннит, из галактозы – дульцит, из ксилозы – пятиатомный спирт ксилит и т. д.

Для восстановления используют амальгаму натрия в водной, водно-спиртовой или спиртовой среде, а также водород в присутствии катализаторов (Ni, Pt, Pd) и гидриды металлов (особенно NaBH4).
При восстановлении альдоз образуется один спирт, а при восстановлении кетоз – два стереоизомерных полиола:

Присоединение синильной кислоты. Эта реакция используется для синтеза моносахаридов с большим числом атомов углерода, чем в исходном моносахариде. При этом образуется смесь двух оптических изомеров, которые отличаются конфигурацией Н и ОН у вновь образовавшегося асимметрического атома углерода. Однако при этом конфигурация асимметрических атомов исходного моносахарида сохраняется. Таким образом, из соединения D ряда образуется также D-изомер, из L-изомера –
L-изомер, но с большим числом атомов углерода.

Образование оксимов. Реакцию образования оксимов можно использовать для укорочения углеродной цепи моноз.

Образование озазонов при взаимодействии с фенилгидразином. Озазоны – хорошо кристаллизуемые вещества с характерной температурой плавления. Реакция используется для идентификации сахаров.

D-глюкоза, D-манноза и D-фруктоза образуют озазоны с одинаковыми физическими и химическими свойствами и одним углом вращения, т.е. озазоны одинакового химического и пространственного строения. Это говорит о том, что расположение групп Н и ОН у трёх асимметрических атомов углерода (3, 4, 5) у всех этих моноз одинаково. Такие оптические изомеры называются эпимерами.
Взаимодействие с щелочами. Под действием сильных щёлочей при нагревании происходит побурение раствора вследствие протекания реакций конденсации, полимеризации и расщепления (с разрушением С-С связей), в результате чего образуется диоксиацетон, глицериновый и гликолевый альдегиды, а также формальдегид.
Реакции, обусловленные наличием гидроксильных групп, – это алкилирование, ацилирование, дегидратация, образование сахаратов. Они осуществляются, как правило, в полуацетальной (циклической) форме.
Алкилирование (образование простых эфиров). При действии метилового спирта в присутствии газообразного хлористого водорода атом водорода гликозидного гидроксила замещается на метильную группу:

При использовании более сильных алкилирующих средств, каковыми являются, например, иодистый метил или диметилсульфат, подобное превращение затрагивает все гидроксильные группы моносахарида:

Интересно, что если полностью алкилированный продукт подвегнуть гидролизу, то гидролизуется только глюкозидная группа:

тетраметилглюкоза
Эта реакция подтверждает повышенную реакционную способность полуацетального гидроксила. Образование глюкозидов может идти также за счёт реакции с аминами.
Ацилирование (образование сложных эфиров). При действии на глюкозу уксусного ангидрида образуется сложный эфир – пентаацетил- глюкоза:
При мягком действии таких минеральных кислот, как фосфорная, моносахариды образуют фосфаты, например монофосфат глюкозы (с участием полуацетальной группы). Такие эфиры часто встречаются в природных соединениях (ДНК, липиды, протеиды и др.).
Реакции дегидратации протекают при нагревании моносахаридов в присутствии минеральных кислот (H2SO4, HCl), при этом образуется фурфурол. Легче всего реакция протекает у пентоз:

Гексозы реагируют с образованием 5-оксиметилфурфурола. Реакция с ними идёт труднее и может привести к более глубоким изменениям вплоть до образования левулиновой кислоты
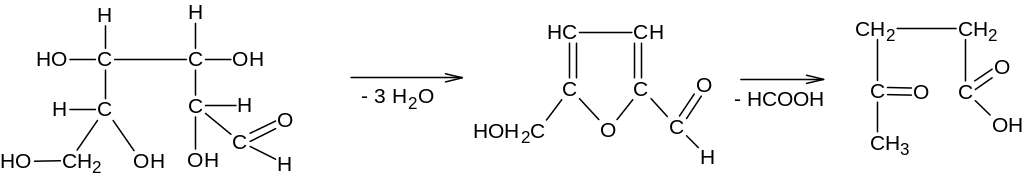
Образование сахаратов. Моносахариды, имеющие в составе молекулы несколько групп ОН, проявляют свойства многоатомных спиртов, они дают качественную реакцию с гидроксидом меди (II) (растворение осадка с образованием комплексного сахарата интенсивной синей окраски).
Кроме приведенных выше реакций, глюкоза характеризуется и некоторыми специфическими свойствами – процессами брожения. Брожением называется расщепление молекул сахаров под воздействием ферментов (энзимов). Брожению подвергаются сахара с числом углеродных атомов, кратным трём. Существует много видов брожения, среди которых наиболее известны следующие: спиртовое, молочнокислое, маслянокислое и уксуснокислое). Наиболее эффективен процесс брожения глицеринового альдегида, диоксиацетона и гексозы. Из двух оптических антиподов (D и L) легче подвергаются брожению монозы D-ряда, которые встречаются в природе. В результате брожения удалось выделить из многих синтетических оптически недеятельных моноз неизвестные ранее оптические антиподы природных соединений:.
a) спиртовое брожение
дрожжи
 C6H12O6
2CH3–CH2OH
(этиловый спирт) + 2CO2
C6H12O6
2CH3–CH2OH
(этиловый спирт) + 2CO2
б) молочнокислое брожение
молочнокислые
бактерии
C |
2CH3CH–СОOH I OH молочная кислота |
в) маслянокислое брожение
 C6H12O6
CH3–CH2–СН2–СОOH
(масляная кислота) + 2Н2
+ 2CO2
C6H12O6
CH3–CH2–СН2–СОOH
(масляная кислота) + 2Н2
+ 2CO2
г) уксуснокислое брожение
уксуснокислые
бактерии
 С6H12O6
3CH3СООН
С6H12O6
3CH3СООН
д) лимонокислое брожение
лимонокислые
бактерии
С6H12O6 + H2O C6H8О7 + 3H2
е) ацетонобутиловое брожение
 2С6H12O6
C4H9ОH
+ CH3COCH3
+ 5CO2
+ 4H2
2С6H12O6
C4H9ОH
+ CH3COCH3
+ 5CO2
+ 4H2
Все эти виды брожения, вызываемые микроорганизмами, имеют широкое практическое значение. Например, спиртовое брожение используется для получения этилового спирта, в виноделии, пивоварении и т.д., а молочнокислое – для получения молочной кислоты и кисломолочных продуктов.

 C–H
C6H12O6
C–H
C6H12O6
 6H12O6
6H12O6