
- •«Вятский государственный университет»
- •Биоорганическая химия в технологии защиты биосферы
- •Оглавление
- •3. Реакция присоединения галогенов за счёт двойных связей в остатках непредельных кислот. 80
- •Биоорганическая химия Предмет биоорганической химии
- •Углеводы
- •Моносахариды
- •Генетический d-ряд альдотриоз, тетроз, пентоз
- •Пентозы с5н10о5
- •Получение моносахаридов
- •Физические свойства моносахаридов
- •Химические свойства моносахаридов
- •Дисахариды (биозы)
- •Общие химические свойства дисахаридов
- •Собственно полисахариды
- •Крахмал
- •Химические свойства
- •Целлюлоза (клетчатка)
- •Химические свойства
- •Химическая переработка целлюлозы
- •Аминокислоты
- •Изомерия
- •Получение
- •Физические свойства
- •Химические свойства
- •Пептиды, белки
- •Химические свойства
- •Ферменты
- •Понятие о нуклеиновых кислотах
- •Моноглицериды
- •Диглицериды
- •Триглицериды
- •Предельные жирные кислоты
- •Непредельные жирные кислоты
- •Физические свойства
- •Химические свойства
- •Сложные жиры
- •Стерины
- •Гормоны и медиаторы
- •Лабораторный практикум Моносахариды Реакции на гидроксильные группы в моносахаридах
- •Реакции на карбонильные группы в моносахаридах
- •Осмоление моносахаридов
- •Цветные реакции на моносахариды
- •Дисахариды Реакции на гидроксильные группы дисахаридов
- •Реакции дисахаридов по карбонильным группам (сравнение свойств восстанавливающих и невосстанавливающих дисахаридов)
- •Гидролиз (инверсия) сахарозы
- •Реакции сахарозы с сульфатами никеля и кобальта
- •Высшие полисахариды Качественные реакции на углеводы
- •Кислотный гидролиз крахмала
- •Свойства целлюлозы
- •Некоторые свойства хлопкового и искусственных волокон
- •Аминокислоты Свойства аминокислот
- •Свойства шерсти и синтетических волокон
- •Цветные рекции на белки
- •Биуретовая реакция
- •Ксантопротеиновая реакция
- •Реакция на триптофан (реакция Шульце-Распайля)
- •Реакция Адамкевича
- •Реакция на серусодержащие аминокислоты
- •Реакция Фоля на серусодержащие аминокислоты
- •Библиографический список
- •Биоорганическая химия в технологии защиты биосферы
Свойства целлюлозы
Растворение целлюлозы в медно-аммиачном растворе (реактиве Швейцера). В пробирку наливают 5 мл медно-аммиачного раствора (реактива Швейцера), опускают в него очень маленький кусочек гигроскопической ваты (целлюлозы) и тщательно перемешивают содержимое пробирки стеклянной палочкой до полного растворения ваты. Получается вязкая прозрачная жидкость ярко-синего цвета. Её выливают тонкой струей в стакан, содержащий около 100 мл тёплой воды, подкислённой 2 – 3 мл концентрированной серной кислоты. Целлюлоза выделяется из раствора в виде хлопьев. Способность целлюлозы растворяться в реактиве Швейцера используется при производстве медно-аммиачного искусственного шёлка.
Растворение и гидролиз клетчатки кислотами. В пробирку с
7 мл холодной серной кислоты помещают кусок свёрнутой жгутом фильтровальной бумаги или ваты. При встряхивании в течение 1– 2 мин волокна клетчатки разъединяются и вскоре почти полностью исчезают; образуется бесцветный густой раствор.
Половину этого раствора выливают в пятикратный объём воды; при этом выделяются хлопья не растворимых в воде продуктов частичного гидролиза клетчатки. Другую половину раствора нагревают в горячей воде до появления светло-коричневой окраски, после чего охлаждают и также выливают в пятикратный объём воды; в этом случае хлопья уже не выпадают.
В отдельные пробирки наливают по 2 мл полученных водных растворов, нейтрализуют их щёлочью и проводят пробы на присутствие восстанавливающих сахаров. Раствор, полученный в результате гидролиза клетчатки при нагревании, восстанавливает окисную медь гораздо быстрее и энергичнее.
Некоторые свойства хлопкового и искусственных волокон
В четыре пробирки наливают по 2 мл концентрированной азотной кислоты, 25%-ного раствора серной кислоты, 10%-ного раствора гидроксида натрия, ацетона. В каждую пробирку опускают небольшой кусочек вискозного волокна (или ткани). Размешивают содержимое пробирки стеклянной палочкой в течение 2 – 3 мин. Результаты опыта записывают в таблицу.
Аминокислоты Свойства аминокислот
Реактивы: 2%-ный раствор аминоуксусной кислоты (глицина),
10%-ный раствор аминоуксусной кислоты, 1%-ный раствор аминоуксусной кислоты, растворы индикаторов в капельницах: метиловый оранжевый, метиловый красный, лакмус, 40%-ный раствор формальдегида (формалин) – нейтрализованный, оксид меди (II), 10%-ный раствор гидроксида натрия, 10%-ный раствор нитрита натрия, ледяная уксусная кислота, 0,1%-ный раствор нингидрина, натрий металлический, -капролактам.
Оборудование: химические стаканы (100 мл), лёд, фильтровальная бумага, пинцеты, скальпели, бани песчаные, термометры (300 °С).
Отношение моноаминомонокарбоновых кислот к индикаторам. В три пробирки наливают по 1 мл 2%-ного раствора аминоуксусной кислоты (глицина) и добавляют по 2 капли растворов индикаторов: в одну пробирку – метилового оранжевого, в другую – метилового красного, в третью – лакмуса.
Меняется ли окраска индикаторов? Объясните результаты опыта.
Реакция аминоуксусной кислоты с формальдегидом. В пробирку к 2 мл 2%-ного раствора аминоуксусной кислоты прибавляют 1 каплю индикатора метилового красного. Раствор окрашивается в жёлтый цвет. Этот индикатор применяют для обнаружения в растворах кислот: в кислой среде в интервале рН 4,2 – 6,2 жёлтая окраска индикатора меняется на красную. Водный раствор аминоуксусной кислоты имеет нейтральную реакцию.
К раствору аминоуксусной кислоты добавляют 1 мл нейтрализованного формалина. Жёлтая окраска раствора превращается в красную, следовательно, реакция раствора стала кислой. Формальдегид присоединяется к аминогруппам, связывает их, карбоксильные группы при этом освобождаются и обусловливают кислую реакцию раствора.
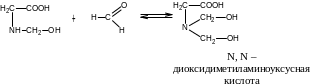
Уравнения реакций аминоуксусной кислоты с 1 моль формальдегида (образование N-монооксиметиламиноуксусной кислоты) и с 2 моль формальдегида (образование N, N-диоксидиметиламиноуксусной кислоты):

Образование медной соли аминоуксусной кислоты. В пробирке нагревают при встряхивании смесь 0,5 г оксида меди (II) и 2 – 3 мл 2%-ного раствора аминоуксусной кислоты. Через 2 – 3 мин пробирку ставят в штатив. После отстаивания хорошо видна синяя окраска раствора. Отливают примерно 0,5 мл раствора и добавляют к нему 1 – 2 капли
10%-ного раствора гидроксида натрия.
Выпадает ли осадок гидроксида меди (II)?
Остальную жидкость сливают с осадка оксида меди (II) в пробирку и охлаждают в стакане с ледяной водой. Постепенно выпадают кристаллы труднорастворимой медной соли аминоуксусной кислоты. Образование комплексных окрашенных в синий цвет медных солей характерно для
-аминокислот.
Уравнение реакции образования комплексной медной соли аминоуксусной кислоты следующее:

Реакция аминокислот с азотистой кислотой. Аминокислоты, как и первичные амины, реагируют с азотистой кислотой с выделением азота. Эту реакцию используют для количественного определения аминокислот.
К 2 мл 10%-ного раствора аминоуксусной кислоты приливают 2 мл
10%-ного раствора нитрита натрия и 2 капли ледяной уксусной кислоты. При встряхивании содержимого пробирки обильно выделяются пузырьки газа (азота).
Уравнение реакции аминоуксусной кислоты c азотистой кислотой следующее:

Реакция -аминокислот с нингидрином. Реакцию с нингидрином применяют для качественного и количественного анализа -аминокислот. Нингидрин разлагает -аминокислоты на альдегиды, оксид углерода (IV) и аммиак. Аммиак конденсируется с избытком нингндрина и с продуктами его восстановления. Продукты конденсации окрашены в розово-фиолетовый цвет. Различные -аминокислоты образуют окрашенные соединения, отличающиеся оттенком.
К 2 мл 1%-ного раствора аминоуксусной кислоты приливают 2 – 3 капли 0,1%-ного раствора нингидрина. Содержимое пробирки встряхивают и ставят в штатив. Через некоторое время раствор приобретают фиолетовый цвет с синеватым оттенком.

нингидрин
