
Учебник Органическая химия Щеголев 2016
.pdf
Прямое окисление алкенов протекает по схеме:
R' |
R'' |
[O] |
R' O |
R'' |
||
|
C = C |
|
C |
|
C |
|
|
|
|
|
|||
|
|
|
|
|||
R |
R"' |
|
R |
R"' |
||
Например, эпоксиэтан образуется при окислении этена кислородом воздуха на серебряном катализаторе при 250 С:
CH2=CH2 O2/Ag CH2 - CH2
O
Эта реакция имеет большое промышленное значение. Мировое производство этиленоксида составляет 5 млн т в год.
Эпоксипроизводные других алкенов можно получить применением органических пероксикислот (RCOOOH) в качестве окислителя — это реакция Прилежаева* (гл. 4.1.4.3, 6.4.6).
3.4.4.3. Краун-эфиры
Краун-эфиры — циклические полиэфиры, содержащие 9 60 атомов в цикле, в том числе от 3 до 20 эфирных атомов кислорода. Они открыты Чарльзом Педерсеном в 1960-х годах, за что ему в 1987 году (совместно с Дональдом Крамом и Жан-Мари Лѐном) была присуждена Нобелевская премия.
Эти макроэфиры представляют собой бесцветные кристаллические или маслообразные вещества, устойчивые к действию кислот и оснований.
Ч. Педерсеном была предложена также и номенклатура краун-эфиров, общие правила которой заключаются в следующем. Название краун-эфира включает: 1) общее число атомов макроцикла, 2) термин «краун», 3) число атомов кислорода, то есть число эфирных звеньев в кольце краунсоединения. Имеющиеся в этой молекуле ароматические или циклогексановые кольца обозначают приставками бензо- и циклогексил-. Например:
O
O O
O O
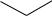
O
дибензо-18-краун-6
151
Эти номенклатурные правила не всегда точно могут описать тип связей в соединении и положение заместителей, однако они очень удобны для обычных краун-эфиров с симметричными и сравнительно простыми структурами.
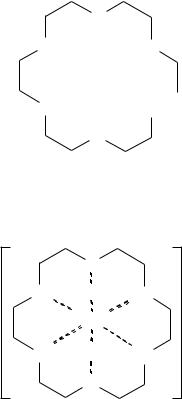
Самое важное свойство краун-эфиров — образование комплексов с металлами. Полость внутренней части, например, такой молекулы:
O
O O
O O 
O
достаточна по размеру для того, чтобы там разместился ион калия, а наличие шести атомов кислорода обеспечивает возможность образования прочной системы координационных связей:
+
O
O

 O
O

 K
K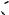

O


 O
O
O
Чем ближе ионный диаметр металла к диаметру полости макроцикла, тем устойчивее комплекс. Так, 18-краун-6 больше подходит для ионов калия, а 15-краун-5 — для ионов натрия. Поэтому комплексы такого типа достаточно хорошо растворимы в органических растворителях.
В общем случае наличие полости в центре макроциклической полиэфирной системы обусловливает способность таких соединений поглощать неорганический катион, размер которого соответствует размеру этой полости, и удерживать его там за счѐт сильных ион-дипольных взаимодействий положительного заряда иона с неподелѐнными электронными парами шести атомов кислорода, обрамляющих полость.
Применение краун-эфиров в органических реакциях связано с образованием таких катионных комплексов, что делает возможным растворение неорганических солей в неполярных растворителях и способствует образованию несольватированного аниона. Это приводит к возрастанию основности аниона и, кроме того, за счѐт малого размера несольватированный анион в качестве нуклеофила способен атаковать пространственно затруднѐнные реакционные центры.
152
В определѐнной степени краун-эфиры моделируют действие некоторых природных веществ (например, антибиотика пептидной природы валиномицина), облегчающих транспорт ионов через клеточные мембраны.
Синтезируют краун-эфиры алкилированием этиленгликоля, диэтиленгликоля НОСН2СН2ОСН2СН2ОН,
триэтиленгликоля НОCН2СН2ОСН2СН2ОСН2СН2ОН подходящими реагентами, например, 2,2 -дихлордиэтиловым эфиром O(CH2CH2Cl)2.
3.4.5. ФИЗИОЛОГИЧЕСКАЯ РОЛЬ И ВАЖНЕЙШИЕ ПРЕДСТАВИТЕЛИ
Простые эфиры применяются для ингаляционного наркоза. Как анестетики, они во многом похожи на галогенопроизводные алифатического ряда. С увеличением длины углеродной цепи в алкильных группах эфиров наркотическое действие их на организм и токсичность возрастают. Из простых эфиров в медицинской практике применяется только этиловый эфир.
Природные соединения типа краун-эфиров играют большую роль в биологических системах — они осуществляют транспорт ионов через биологические мембраны.
Метаболическое отщепление О-алкильных групп из молекул эфиров (О-дезалкилирование) — не простая замена алкоксигруппы гидроксилом, а процесс окисления. Под действием ферментов образуется -оксид, который и распадается спонтанно до альдегида (в случае первичной алкоксигруппы) или кетона (в случае вторичной алкоксигруппы):
R CH-O R" |
|
|
|
R C |
O-R" |
|
|
|
R C=O + H-O-R" |
|||
|
|
|
|
|
|
|
||||||
R' |
|
|
R' |
|
|
|
|
|
|
|
R' |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
O: |
H |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
В эфирах с более длинными алкильными группами, чем этильные, вначале окисляется алкильная цепь ( -гидроксилирование) как в случае метаболизма алканов (гл. 2.6), а процессы дезалкилирования для них вторичны.
Диэтиловый эфир — бесцветная жидкость со своеобразным эфирным запахом, очень летуч, его пары тяжелее воздуха. Плохо растворим в воде, а вода плохо растворима в эфире.
Диэтиловый эфир хорошо растворяет различные органические вещества, поэтому его широко применяют в качестве растворителя для экстракции и для металлорганического синтеза. В медицине диэтиловый эфир применяют для общего наркоза.
Целлозольвы — моноалкиловые эфиры гликоля, являются хорошими растворителями, особенно для растворения сложных эфиров целлюлозы.
1,2-Диметоксиэтан (диметиловый эфир этиленгликоля) и
153
Диглим (диметиловый эфир диэтиленгликоля) — хорошие растворите-
ли, растворяют также некоторые неорганические соли за счѐт сильной сольватации ионов металлов.
Этиленоксид — бесцветный газ с эфирным запахом, хорошо растворимый в воде и в органических растворителях; температура кипения 11 С.
Широко применяется в органическом синтезе, особенно для получения ценных растворителей и поверхностно-активных веществ.
Тетрагидрофуран (1,4-эпоксибутан, тетраметиленоксид) — бесцвет-
ная жидкость с запахом эфира, растворима в воде и органических растворителях; температура кипения 66 С. Хорошо сольватирует ионы различных металлов. Широко применяется в качестве растворителя.
3.5. ЭФИРЫ МИНЕРАЛЬНЫХ КИСЛОТ
Это такие, как эфиры неорганических кислот (серной, фосфорной и др.), которые имеют общую формулу R–O–Z, где Z в отличие от углеводородного радикала простых эфиров — остаток минеральной кислоты, обладающий сильным акцепторным эффектом.
3.5.1. ЭФИРЫ СЕРНОЙ КИСЛОТЫ
Серная кислота может образовывать как кислые, так и полные эфиры. При этом кислые эфиры могут быть названы и как замещѐнная серная кислота.
O |
O |
||
R-O S OH |
R-O S OR |
||
|
|
|
|
O |
O |
||
алкилгидросульфат (алкилсерная кислота) |
диалкилсульфат |
||
Связь С–О в молекулах этих соединений в значительной степени поляризована, в связи с чем атом углерода является высоко реакционноспособным электрофильным центром:
+  O
O
R'-CH2  O S
O S OH
OH  O
O
Поэтому эфиры серной кислоты легко вступают в различные реакции нуклеофильного замещения сульфатной группы, превращаясь в другие производные алканов. На этом основано их применение в качестве эффективных
154
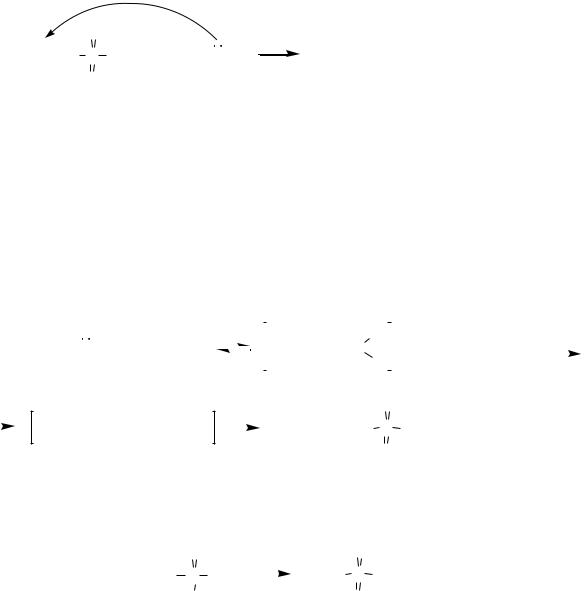
алкилирующих агентов (главным образом для алкилирования спиртов, фенолов):
+ |
O |
- |
R'-O-CH2-R + H2O + HSO4- |
|
OH |
||
R-CH2-O S OH + R'-OH |
|||
|
O |
|
, |
вчастности, диметилсульфат применяется для метилирования, диэтилсульфат — для этилирования.
Образование кислых эфиров протекает легко при растворении спиртов
вконцентрированной серной кислоте. Механизм реакции здесь близок к SN1 или пограничный между SN1 и SN2 даже в случае первичных спиртов, так как диссоциации субстрата способствуют эффективное протонирование и дегидратация, осуществляющиеся концентрированной серной кислотой, а нуклеофильность гидросульфат-иона крайне низка. Все эти факторы свидетельствуют о преобладании мономолекулярного механизма данной реакции.
|
|
|
|
|
|
|
|
|
|
|
|
|
+ H |
|
|
- |
|
H2SO4 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3-CH2-O |
|
HSO4 |
|
||||
|
CH3-CH2-OH |
+ |
H2SO4 |
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
.H O |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
-H SO |
||
|
+ |
|
HSO4- |
|
|
|
|
|
|
|
O |
|
|
|
2 |
4 |
2 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
CH3CH2-O S OH |
|
|
|
|
|
||||||
|
|
CH3-CH2 |
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
Диалкилсульфаты образуются при взаимодействии спиртов с хлорсульфоновой кислотой или с олеумом, например:
O |
|
O |
||
2 R-OH + Cl S OH |
|
|
R-O S OR + H2O + HCl |
|
|
|
|||
|
|
|
||
O |
|
O |
||
Диметилсульфат — бесцветная жидкость, малорастворим в воде, но хорошо — в органических растворителях; температура кипения 189 С. Очень ядовит, проникает в организм через кожу и через дыхательные пути.
Получают диметилсульфат из метанола и олеума. Широко применяется в качестве метилирующего агента, в частности, для получения целого ряда лекарственных препаратов (триметина, анальгина, метилкофеина и т.д.).
Диэтилсульфат — бесцветная жидкость, нерастворим в воде; температура кипения 210 С. Очень ядовит.
Получают диэтилсульфат из этанола и олеума или при насыщении концентрированной серной кислоты этиленом. Широко применяется в качестве этилирующего агента.
155

3.5.2.ЭФИРЫ ФОСФОРНОЙ КИСЛОТЫ
Всоответствии со структурой ортофосфорной кислоты возможно образование и существование еѐ алкиловых эфиров:
R-O |
R-O |
R-O |
||||||
HO P |
|
O |
R-O P |
|
O |
R-O P |
|
O |
|
|
|
||||||
|
|
|
||||||
HO |
HO |
R-O |
||||||
алкилдигидрофосфат |
диалкилгидрофосфат |
триалкилфосфат |
||||||
Эфиры фосфорной кислоты в обычных условиях — достаточно стабильные соединения, но в кислой или щелочной среде могут подвергаться гидролизу. Эти реакции являются типичным нуклеофильным замещением у атома углерода эфирной связи, причѐм гидролиз кислых фосфатов обычно ускоряется в кислой, а полных — в щелочной среде:
|
|
O |
OH |
H2O / H+ |
|||
H C-H C-O |
|
P |
OH |
|
|
CH3-CH2OH + H3PO4 |
|
|
|
|
|||||
3 2 |
|
|
|
|
|
||
+ |
|
|
|
|
|
||
H3C-H2C-O |
|
|
OH- |
||||
+ |
|
|
|||||
H3C-H2C-O |
P O |
|
|
|
3 CH3-CH2OH + PO43- |
||
|
|
|
|||||
+ |
|
|
|
|
|
||
H3C-H2C-O |
|
|
|
|
|
||
Это, по-видимому, связано со способностью кислых эфиров к диссоциации с образованием соответствующего аниона, который не взаимодействует с гидроксид-ионом.
Но в целом в щелочной среде гидролиз протекает необратимо вследствие стабильности аниона уходящей группы (фосфат-анион) и невозможности осуществления по нему нуклеофильной атаки.
Эфиры фосфорной кислоты получают главным образом из галогенидов фосфора и спиртов. Например:
POCl3 + 3 C2H5OH O=P(OC2H5)3 + 3 HCl
триэтилфосфат
Кислые фосфаты получают также взаимодействием спиртов с оксидом фосфора (V).
Эфиры фосфорной кислоты в живых организмах играют две ключевые роли. Во-первых, они служат структурными компонентами клеточных мембран и нуклеиновых кислот. Основу клеточных мембран составляют фосфолипиды (гл. 6.5.6). Остов нуклеиновых кислот состоит из рибозо- и дезокси-
156

рибозофосфатных цепей (гл. 12.5.5). Во-вторых, эфиры фосфорной кислоты, точнее полифосфорных кислот, в организме аккумулируют и переносят энергию (гл. 7.1.3).
3.6. ТИОСПИРТЫ И ТИОЭФИРЫ
Названия этих классов соединений означают, что они являются тиоаналогами соответственно спиртов и эфиров. С другой стороны, их можно рассматривать как органические производные сероводорода, в которых один или два атома водорода замещены предельными углеводородными радикалами: R-SH и R-S-R соответственно.
Сами соединения называют обычно по заместительной и радикалофункциональной номенклатурам ИЮПАК. Например:
CH3-SH |
CH3-CH-CH2-CH3 |
CH3-S- |
CH-CH2-CH3 |
|
|
||||
SH |
CH3 |
|||
|
||||
метантиол, |
бутан-2-тиол, |
2-метилтиобутан, |
||
метилмеркаптан |
втор-бутилмеркаптан |
метил-втор-бутилсульфид |
||
Тиоспирты (меркаптаны, алкантиолы, или просто тиолы) во многом отличаются от своих кислородных аналогов. Так, их первые представители, в отличие от спиртов, плохо растворяются в воде и кипят при значительно более низких температурах. Например, метилмеркаптан при обычных условиях
— газ (температура кипения 6 С), а метиловый спирт — жидкость (температура кипения 64 С). Эти различия определяются способностью к образованию водородных связей за счѐт ОН-групп в спиртах и SH-групп в меркаптанах.
Меркаптаны обладают неприятным запахом, который обнаруживается в чрезвычайно малых концентрациях. Например, запах метилмеркаптана чувствуется уже при содержании его в воздухе 2.5 10-7%.
Тиоэфиры (сульфиды) — это также бесцветные соединения с неприятным запахом. Их температуры кипения выше, чем у аналогичных простых эфиров. Низшие представители являются жидкостями.
Тиоспирты обладают слабокислыми свойствами (для этантиола рКа = 10.6), и кислотность их выражена сильнее, чем спиртов (на 4 5 порядков) за счѐт большей поляризуемости атома серы по сравнению с кислородом (подобно тому, что H2S является более сильной кислотой, чем H2O). Поэтому с водными растворами щелочей они образуют соли, например:
С2Н5-SH + NaOH С2Н5-S Na+ + H2O
этантиол, |
этантиолят натрия, |
этилмеркаптан |
этилмеркаптид натрия |
|
157 |

Тиоляты являются сильными нуклеофилами и легко алкилируются. Это типичная реакция нуклеофильного замещения, в которой субстратом обычно является галогеналкан:
R-S Na+ + R -X R-S-R + NaX
Образующиеся тиоэфиры могут алкилироваться дальше. Продуктом исчерпывающего алкилирования является соль триалкилсульфония:
|
|
|
+ |
- |
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
||||
R |
S |
|
R' + R" X |
|
|
|
R S |
|
R' |
-- |
||
|
|
|
||||||||||
|
|
|
|
|
|
|
|
X |
||||
|
|
|
|
|
|
|
|
R" |
|
|||
Например, горчичный газ (или иприт), ClCН2CН2SCН2CН2Cl может само-
произвольно превращаться с образованием хлорида тризамещѐнного сульфония. Это внутримолекулярная SN2-реакция:
|
|
|
|
|
CH2 |
|
Cl- |
|
Cl-H2C-H2C CH2 Cl |
|
+ |
|
|||||
|
|
|
ClCH2-CH2-S |
|
|
|||
|
|
|
||||||
S |
CH2 |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
Наличие трѐхчленного малого цикла придаѐт ему высокую реакционную способность. Он легко подвергается нуклеофильной атаке аминогруппами, входящими в состав белковых молекул, что приводит к алкилированию белка. В этом состоит причина кожно-нарывного действия горчичного газа и поражения слизистых оболочек.
Как тиоспирты, так и тиоэфиры являются очень слабыми основаниями, значительно слабее, чем их соответствующие кислородные аналоги.
Тиолы и сульфиды легко окисляются до различных продуктов. Тиоспирты при окислении йодом образуют дисульфиды R-S-S-R, более энергичные окислители могут их окислить до алкансульфоновых кислот R-SO3H:
|
|
I2 |
R-S-S-R |
R-SH |
|
|
|
|
|
|
|
|
|
|
|
|
|
KMnO4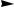 R-SO3H
R-SO3H
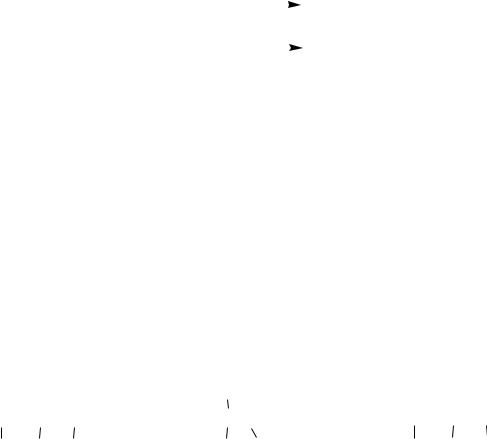
Тиоэфиры окисляются до сульфоксидов и сульфонов (например, пероксикислотами R-COOOH — гл. 6.4.6):
|
|
O |
|
O |
|||||
R-S-R' |
[O] |
|
|
|
[O] |
|
|
|
|
R-S-R' |
R-S-R' |
||||||||
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||
158
Тиоспирты и тиоэфиры могут быть получены взаимодействием галогеналканов с кислыми и средними солями сероводородной кислоты:
Na+ SH + R-X R-SH + NaX
Na2+ S 2- + R-X R-S-R + 2NaX
Это типичные реакции нуклеофильного замещения галогеналканов. Тиоэфиры могут быть получены также из тиоспиртов, как было пока-
зано выше.
В промышленности для получения меркаптанов и сульфидов используют каталитическое алкилирование сероводорода спиртами в газовой фазе
(при 330 400 С):
|
|
|
ThO2, to |
||
R-OH + H2S |
|
|
|
|
R-SH + H2O |
|
|
|
|||
|
|
|
|||
|
|
Al2O3, to |
|||
|
|||||
|
|
|
|||
|
|
|
|
|
R-S-R + H2O |
|
|
|
|
|
|
Диметилсульфид — бесцветная летучая жидкость с неприятым запахом. Получают каталитически из метанола и сероводорода. Используют для производства диметилсульфоксида.
Горчичный газ, иприт — бесцветная жидкость; температура кипения 215 С. Очень токсичное вещество кожно-нарывного действия. Получают взаимодействием этилена с хлоридами серы.
Некоторые поли- и гетерофункциональные тиолы образуют прочные комплексы с ионами тяжѐлых металлов, на чѐм основано их использование в качестве противоядий (антидотов) при отравлении соединениями ртути, свинца, кадмия, сурьмы, мышьяка. Одним из первых антидотов был 2,3-димеркаптопропан-1-ол (британский антилюизит, БАЛ). Позже нашли применение такие тиолы, как 2-амино-3-меркапто-3-метилбутановая кислота (пеницилламин) и 2,3-димеркаптопропансульфонат натрия (унитиол).
|
CH3 |
|
CH2-CH-CH2 |
CH3-C-CH-COOH |
CH2-CH-CH2 |
SH SH OH |
SH NH2 |
SH SH SO3Na |
БАЛ |
пеницилламин |
унитиол |
3.7. НАСЫЩЕННЫЕ АМИНЫ
Насыщенные амины можно рассматривать как производные предельных углеводородов, то есть это продукты замещения одного или нескольких
159

атомов водорода в молекуле алкана одной или несколькими аминогруппами (-NН2) или же — как производные аммиака, в молекуле которого один, два или три атома водорода замещены углеводородными радикалами.
3.7.1. КЛАССИФИКАЦИЯ, НОМЕНКЛАТУРА, ИЗОМЕРИЯ
Если рассматривать амины как производные аммиака, то в зависимости от числа углеводородных радикалов у атома азота их можно разделить на первичные, вторичные и третичные:
|
|
R" |
|
|
R-NН-R |
|
|
R-NН2 |
R-N-R' |
||
первичный |
вторичный |
третичный |
|
По количеству аминогрупп в молекуле можно выделить моноамины
(например, C2H5-NН2), диамины (например, NН2-CH2CH2-NН2) и т.д.
Для названия аминов применяются как радикало-функциональная, так и заместительная номенклатуры ИЮПАК, однако могут применяться и другие виды номенклатур (например, «а»-номенклатура).
По радикало-функциональной номенклатуре перечисляются названия углеводородных радикалов и добавляется слово «амин». Например:
CH3-NН2 |
— |
метиламин, |
C2H5-NH-СН3 |
— |
метилэтиламин, |
CH3-N-C2H5 |
— |
метилдиэтиламин. |
C2H5 |
|
|
Однако по радикало-функциональной номенклатуре удобно называть только моноамины или другие несложные по структуре соединения. Для веществ, молекулы которых содержат несколько функциональных групп, применение радикало-функциональной номенклатуры часто бывает затруднительно, но в отдельных случаях она может использоваться, например:
NH2-CH2CH2CH2-NH2 — триметилендиамин
Заместительная номенклатура более универсальна. При названии первичных аминов функциональная группа (-NH2) называется суффиксом «-амин», добавляемым к названию углеводорода, а в присутствии старших групп — приставкой «амино». Например:
NH2-CH2CH2CH2-NH2 |
— пропан-1,3-диамин, |
СН3CH2-NHCН3 |
— N-метилэтанамин, |
|
160 |
