
- •Помогаев а.И.
- •Оглавление
- •1. Способы получения
- •1.1.5. Гидрогалогенирование сопряженных диенов
- •1.1.6. Замещение гидроксильной группы в спиртах на галоген
- •1.2. Способы получения винил- и арилгалогенидов
- •1.3. Способы получения дигалогенопроизводных
- •2. Химические свойства
- •2.1. Реакции нуклеофильного замещения (sn) в алкилгалогенидах
- •2.1.1. Механизм мономолекулярного нуклеофильного замещения (sn1)
- •2.1.2. Механизм бимолекулярного нуклеофильного замещения (sn2)
- •2.2. Особенности нуклеофильного замещения галогена в арилгалогенидах
- •2.2.1. Нуклеофильное замещение в неактивированных арилгалогенидах
- •2.2.2. Нуклеофильное замещение в активированных арилгалогенидах
- •2.3. Реакция дегидрогалогенирования
- •2.4. Восстановление галогенопроизводных
- •2.5. Реакции галогенопроизводных с металлами
- •3. Задачи и упражнения
- •1. Способы получения
- •1.1. Гидратация алкенов
- •1.2. Гидролиз галогенопроизводных
- •1.3. Восстановление карбонильных соединений
- •1.4. Получение спиртов реакцией Гриньяра
- •1.5. Получение диолов и триолов
- •2. Химические свойства
- •2.1. Кислотно-основные свойства
- •2.2. Реакции спиртов с разрывом связи о-н
- •2.2.1. Алкилирование спиртов
- •2.2.2. Ацилирование спиртов
- •2.3. Реакции спиртов с разрывом связи с-о
- •2.3.1. Замещение гидроксильной группы на галоген
- •2.3.2. Образование простых эфиров (межмолекулярная дегидратация)
- •2.3.3. Внутримолекулярная дегидратация спиртов до алкенов
- •2.4. Окисление и дегидрирование спиртов
- •3. Задачи и упражнения
- •1. Способы получения
- •1.1. Щелочной гидролиз арилгалогенидов
- •1.2. Щелочное плавление солей ароматических сульфокислот
- •1.3. «Кумольный» метод получения фенола
- •2. Химические свойства
- •2.1. Кислотно-основные свойства фенолов
- •2.2. Фенолы как нуклеофилы
- •2.2.1. Алкилирование и ацилирование фенолов по атому кислорода
- •2.2.2. Реакции электрофильного замещения
- •3. Задачи и упражнения
- •Альдегиды и кетоны
- •1. Способы получения
- •1.1. Окисление алкенов
- •1.1.1. Озонолиз алкенов
- •1.1.2. Окисление алкенов в присутствии хлорида палладия
- •1.2. Гидратация алкинов
- •1.3. Получение ароматических альдегидов и кетонов ацилированием аренов
- •1.4. Гидролиз геминальных дигалогенидов
- •1.6.3. Синтез кетонов из нитрилов карбоновых кислот реакцией Гриньяра
- •2. Химические свойства
- •2.1. Кислотно-основные свойства и кето-енольная таутомерия
- •2.2. Реакции нуклеофильного присоединения
- •2.2.1. Реакции с о-нуклеофилами
- •2.2.2. Реакции с s-нуклеофилами
- •2.2.3. Реакции с n-нуклеофилами
- •2.2.4. Реакции с с-нуклеофилами
- •2.3. Реакции енолизующихся альдегидов и кетонов с галогенами
- •2.4. Окисление и восстановление альдегидов и кетонов
- •2.4.1. Окисление альдегидов и кетонов
- •2.4.2. Восстановление альдегидов и кетонов
- •2.4.3. Реакция Канниццаро
- •3. Задачи и упражнения
- •Помогаев Александр Ильич
- •Часть 3
2. Химические свойства
Все реакции, характерные для спиртов, можно формально разделить на реакции, протекающие с разрывом связи О-Н, и реакции, в которых происходит разрыв связи С-О. В первом случае, т.е. при разрыве связи О-Н молекула спирта проявляет нуклеофильные или кислотные свойства, во втором случае – электрофильные или основные свойства.
2.1. Кислотно-основные свойства
Подобно воде, спирты являются амфотерными соединениями. Они проявляют кислотные свойства, реагируя как О-Н-кислоты с достаточно сильными основаниями.
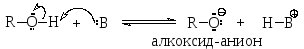
По кислотным свойствам спирты немного уступают воде (рКа 16-18), поскольку их сопряженные основания – алкоксид-анионы – менее устойчивы в растворе, чем гидроксид-анион, из-за меньшей сольватации. При этом кислотные свойства спиртов уменьшаются в ряду метанол – первичные спирты – вторичные спирты – третичные спирты по этой же причине: более объемные третичные алкоксид-анионы менее сольватированы, чем вторичные или, тем более, первичные. Введение электроноакцепторных заместителей в молекулу спирта приводит к усилению кислотных свойств, т.к. такие заместители стабилизируют алкоксид-анион, уменьшая отрицательный заряд атома кислорода. Так, например, 2-хлорэтанол является более сильной кислотой, чем этанол, поскольку атом хлора в 2-хлорэтоксид-анионе за счет своего отрицательного индуктивного эффекта уменьшает заряд на атоме кислорода и этот анион становится более устойчивым, чем незамещенный этоксид-анион.
![]()
Как кислоты, спирты могут образовывать соли – алкоголяты металлов, реагируя только с сильными основаниями или с активными металлами. Водные растворы щелочей не могут эффективно депротонировать спирты, поскольку вода является более сильной кислотой. Ниже приведены некоторые уравнения реакций, в которых спирты превращаются в соли:


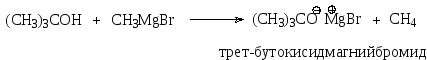
Как основания, спирты могут реагировать только с очень сильными кислотами, поскольку основные свойства выражены не сильно.
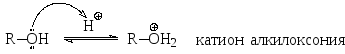
2.2. Реакции спиртов с разрывом связи о-н
2.2.1. Алкилирование спиртов
Как нуклеофилы спирты могут взаимодействовать с алкилгалогенидами. При этом в результате нуклеофильного замещения происходит образование простых эфиров. Поскольку атом водорода в гидроксильной группе замещается на алкильную группу, этот процесс обозначают как алкилирование спиртов.
![]()
Однако из-за высокой электроотрицательности атома кислорода нуклеофильность спиртов мала, поэтому алкилированию подвергают не сами спирты, а их алкоголяты, в которых атом кислорода, имеющий отрицательный заряд, естественно, является более нуклеофильным. Так, пропиловый спирт можно метилировать действием на него натрия и последующим взаимодействием пропилата натрия с метилиодидом.

2.2.2. Ацилирование спиртов
Замещение атома водорода в гидроксильной группе молекулы спирта на ацильную группу приводит к ацилированию спирта и превращению его в сложный эфир карбоновой кислоты. Эту процедуру можно осуществить с помощью различных ацилирующих агентов. Одной из реакций ацилирования является этерификация – взаимодействие спирта и карбоновой кислоты в присутствии более сильной кислоты как катализатора. Например, при нагревании бутилового спирта с уксусной кислотой в присутствии серной кислоты образуется бутиловый эфир уксусной кислоты (бутилацетат).
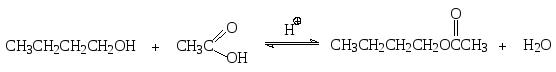
Ацилировать бутиловый спирт можно также производными уксусной кислоты, такими как ее хлорангидрид (ацетилхлорид) или ангидрид (уксусный ангидрид) в соответствии с уравнениями:
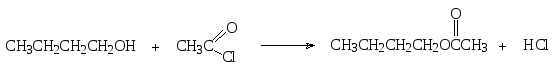
ацетилхлорид
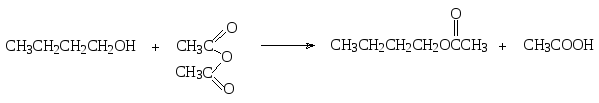
уксусный ангидрид
Ацилирование можно также осуществить после предварительного депротонирования спирта, т.е. взаимодействием алкоголята с хлорангидридом или ангидридом карбоновой кислоты:
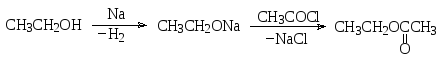
этилат натрия этилацетат
