
- •Помогаев а.И.
- •Оглавление
- •1. Способы получения
- •1.1.5. Гидрогалогенирование сопряженных диенов
- •1.1.6. Замещение гидроксильной группы в спиртах на галоген
- •1.2. Способы получения винил- и арилгалогенидов
- •1.3. Способы получения дигалогенопроизводных
- •2. Химические свойства
- •2.1. Реакции нуклеофильного замещения (sn) в алкилгалогенидах
- •2.1.1. Механизм мономолекулярного нуклеофильного замещения (sn1)
- •2.1.2. Механизм бимолекулярного нуклеофильного замещения (sn2)
- •2.2. Особенности нуклеофильного замещения галогена в арилгалогенидах
- •2.2.1. Нуклеофильное замещение в неактивированных арилгалогенидах
- •2.2.2. Нуклеофильное замещение в активированных арилгалогенидах
- •2.3. Реакция дегидрогалогенирования
- •2.4. Восстановление галогенопроизводных
- •2.5. Реакции галогенопроизводных с металлами
- •3. Задачи и упражнения
- •1. Способы получения
- •1.1. Гидратация алкенов
- •1.2. Гидролиз галогенопроизводных
- •1.3. Восстановление карбонильных соединений
- •1.4. Получение спиртов реакцией Гриньяра
- •1.5. Получение диолов и триолов
- •2. Химические свойства
- •2.1. Кислотно-основные свойства
- •2.2. Реакции спиртов с разрывом связи о-н
- •2.2.1. Алкилирование спиртов
- •2.2.2. Ацилирование спиртов
- •2.3. Реакции спиртов с разрывом связи с-о
- •2.3.1. Замещение гидроксильной группы на галоген
- •2.3.2. Образование простых эфиров (межмолекулярная дегидратация)
- •2.3.3. Внутримолекулярная дегидратация спиртов до алкенов
- •2.4. Окисление и дегидрирование спиртов
- •3. Задачи и упражнения
- •1. Способы получения
- •1.1. Щелочной гидролиз арилгалогенидов
- •1.2. Щелочное плавление солей ароматических сульфокислот
- •1.3. «Кумольный» метод получения фенола
- •2. Химические свойства
- •2.1. Кислотно-основные свойства фенолов
- •2.2. Фенолы как нуклеофилы
- •2.2.1. Алкилирование и ацилирование фенолов по атому кислорода
- •2.2.2. Реакции электрофильного замещения
- •3. Задачи и упражнения
- •Альдегиды и кетоны
- •1. Способы получения
- •1.1. Окисление алкенов
- •1.1.1. Озонолиз алкенов
- •1.1.2. Окисление алкенов в присутствии хлорида палладия
- •1.2. Гидратация алкинов
- •1.3. Получение ароматических альдегидов и кетонов ацилированием аренов
- •1.4. Гидролиз геминальных дигалогенидов
- •1.6.3. Синтез кетонов из нитрилов карбоновых кислот реакцией Гриньяра
- •2. Химические свойства
- •2.1. Кислотно-основные свойства и кето-енольная таутомерия
- •2.2. Реакции нуклеофильного присоединения
- •2.2.1. Реакции с о-нуклеофилами
- •2.2.2. Реакции с s-нуклеофилами
- •2.2.3. Реакции с n-нуклеофилами
- •2.2.4. Реакции с с-нуклеофилами
- •2.3. Реакции енолизующихся альдегидов и кетонов с галогенами
- •2.4. Окисление и восстановление альдегидов и кетонов
- •2.4.1. Окисление альдегидов и кетонов
- •2.4.2. Восстановление альдегидов и кетонов
- •2.4.3. Реакция Канниццаро
- •3. Задачи и упражнения
- •Помогаев Александр Ильич
- •Часть 3
2.2.2. Нуклеофильное замещение в активированных арилгалогенидах
Если в ароматическом ядре арилгалогенида присутствуют электроноакцепторные заместители, процесс замещения атома галогена на нуклеофил значительно облегчается. При этом реакция протекает по механизму бимолекулярного ароматического нуклеофильного замещения, включающего стадию образования отрицательно заряженного σ-комплекса в результате присоединения нуклеофила и стадию отщепления галогенид-аниона. По такому механизму происходит, например, щелочной гидролиз пара-нитрохлорбензола до пара-нитрофенолята натрия (образующийся при замещении пара-нитрофенол проявляет достаточно сильные кислотные свойства, превращаясь в щелочной среде в пара-нитрофенолят).
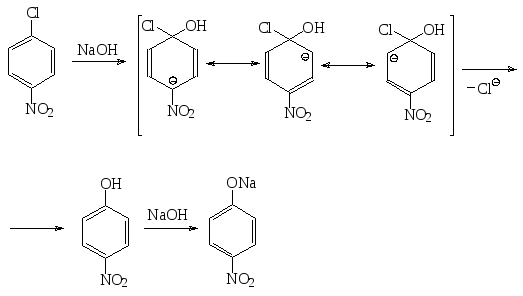
σ-комплекс
2.3. Реакция дегидрогалогенирования
Отщепление галогеноводорода от молекулы галогенопроизводного происходит региоселективно с образованием наиболее термодинамически устойчивого алкена в соответствии с правилом Зайцева. Так, при нагревании 2-хлорпентана в спиртовом растворе КОН главным продуктом оказывается 2-пентен:
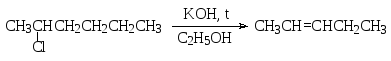
Механизмы, по которым может протекать элиминирование, имеют ту же кинетическую основу, что и механизмы нуклеофильного замещения. Действительно, процесс отщепления заключается в разрыве двух связей в молекуле галогенопроизводного: связи углерод-галоген и связи углерод-водород, причем галоген уходит как анион, а водород – в виде протона, который отрывает основание. Разрывы связей могут происходить либо последовательно, т.е. постадийно, либо синхронно. В первом случае реализуется механизм мономолекулярного элиминирования (Е1), во втором – механизм бимолекулярного элиминирования (Е2).
Третичные галогенопроизводные, способные образовать стабильные карбокатионы, подвергаются дегидрогалогенированию по механизму мономолекулярного элиминирования Е1. Так, например, при нагревании трет-бутилхлорида с гидроксидом калия в этаноле происходит сначала ионизация, а затем уже депротонирование образовавшегося на первой стадии карбокатиона:
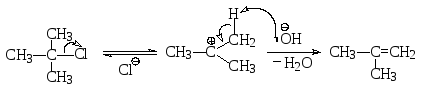
Для вторичных и первичных галогенопроизводных характерен механизм бимолекулярного элиминирования Е2:
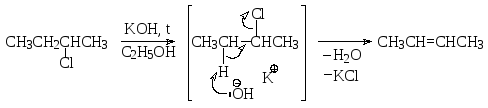
переходное состояние
2.4. Восстановление галогенопроизводных
Восстановление галогенопроизводных до соответствующих углеводородов можно осуществить различными способами:
восстановление водородом в момент выделения
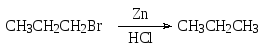
каталитическое гидрирование
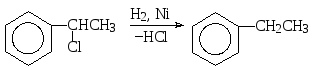
восстановление комплексными гидридами, например, алюмогидридом лития
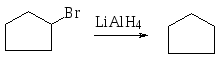
2.5. Реакции галогенопроизводных с металлами
В зависимости от природы металлы реагируют с галогенопроизводными по-разному. При воздействии металлического натрия галогенопроизводные по реакции Вюрца превращаются в алканы, например, из этилхлорида образуется бутан.
![]()
С менее реакционноспособным литием образуются литийорганические соединения, например:

фениллитий
При нагревании с магнием в диэтиловом эфире алкил- и арилгалогениды превращаются в магнийорганические соединения – так называемые реактивы Гриньяра:
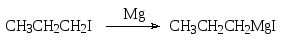
пропилмагнийиодид
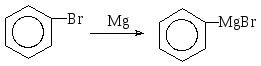
фенилмагнийбромид
Металлорганические соединения, такие как литий- и магнийпроизводные углеводородов, являются чрезвычайно реакционноспособными соединениями, которые из-за высокой полярности связи углерод-металл представляют собой сильные С-нуклеофилы.
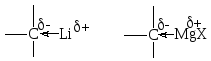
Реактивы Гриньяра и литийорганические соединения являются также сильными основаниями и реагируют с соединениями, проявляющими кислотные свойства. Поэтому их синтез проводят только в безводных растворителях, поскольку вода, как кислота, реагирует с этими соединениями, гидролизуя их.
![]()
Подобным же образом реактивы Гриньяра реагируют и с другими более или менее сильными кислотами, например, с карбоновыми кислотами или спиртами:
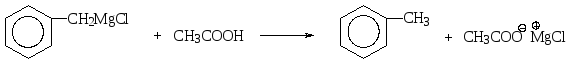
![]()
