
- •Государственное бюджетное образовательное учреждение
- •Предисловие
- •Тематические разделы дисциплины «Химия»
- •1. 1. Растворы. Способы выражения концентрации растворов
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.2. Введение в титриметрический анализ. Метод нейтрализации
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.3. Оксидиметрия. Перманганатометрия.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.4. Элементы химической термодинамики
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.5. Энергетика химических процессов
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.6. Коллигативные свойства растворов. Осмос.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.7. Водородный показатель среды растворов – pH.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.8. Буферные системы
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.9. Электрохимия. Потенциометрия.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.10. Окислительно-восстановительные потенциалы и электроды
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.11. Комплексные соединения
- •Контрольные вопрросы
- •Типовые задачи
- •Тестовые задания
- •Контрольные задания
- •Литература
- •1.12. Поверхностные явления. Способы получения и свойства коллоидных растворов.
- •Контрольные вопросы
- •Тестовые задания
- •Контрольные задания
- •Литература
- •1.13. Свойства растворов высокомолекулярных веществ (вмв)
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания
- •Контрольные задания
- •Литература
- •1.14. Биогенные элементы
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания
- •Темы рефератов
- •Литература
- •2. Инструкция по охране труда и пожарной безопасности для студентов при работе в лабораториях кафедры химии
- •2.1. Общие требования безопасности
- •2.2. Требования безопасности перед началом работы
- •2.3. Требования безопасности во время работы
- •2.4. Требования безопасности в аварийных ситуациях
- •2.5. Требования безопасности по окончании работы
- •3. Кодификатор зачетной работы дисциплины «Химия» для студентов I курса специальностей
- •060101- Лечебное дело; 060103-педиатрия
- •Характеристика зачетной работы и инструкция по ее выполнению
- •Часть 2
- •Часть 3
- •Заключение
- •Глоссарий
- •Ответы на тестовые задания
- •Приложения
- •1. Основные физико-химические константы
- •2. Важнейшие единицы си и их соотношение с единицами других систем
- •3. Приставки для дольных и кратных единиц си
Контрольные задания
07. Рассчитайте величину о/в потенциала при температуре 25 0С для системы Со3+/Со2+, если Е0(Со3+/Со2+) = + 1,84 В, а (Со3+) = 0,001 моль/дм3, а (Со2+) = 0,01 моль/дм3.
08. Рассчитайте величину о/в потенциала для о/в электрода Fe+3/Fe+2 , если при Т = 298 К активные концентрации ионов Fe+3 и Fe+2 соответственно составляют 0,02 моль·дм– 3 и 0,006 моль·дм– 3; Е0 (Fe+3/ Fe+2) = +0,77 В.
09. Даны о/в системы
а) SO42– + H2O + 2ē ↔ SO32– + 2OH-; Е0SO42–/ SO32– = – 0,93 В
б) MnО4– + 4H+ + 3ē ↔ MnO2 + 2 H2O; Е0MnO4–/ MnO2 = + 1,695 В
Составить схему гальванического элемента на основе данных о-в систем. Привести уравнение о/в реакции элемента, рассчитать ЭДС цепи.
10. Составьте уравнения реакций диспропорционирования с участием следующих веществ: а) пероксида водорода; б) хлора; в) серы.
11. Из заданных о/в систем (приложение 3.5.) составить гальваническую цепь, рассчитать ЭДС цепи и написать ионное уравнение суммарного о/в процесса:
1) 10 и 13; 2) 1 и 18; 3) 5 и 14.
Литература
1. Общая химия. Биофизическая химия. Химия биогенных элементов: Учеб. для вузов / Ю. А. Ершов, В.А. Попков, А.С. Берлянд и др.; Под ред. Ю.А. Ершова. – 5-е изд., стер. – М.: Высш.шк., 2005. – С. 479 – 484.
2. Практикум по общей химии. Биофизическая химия. Химия биогенных элементов: Учеб. пособие для студентов медицинских спец. вузов / Ю.А. Ершов, А.М. Кононов, С.А. Пузаков и др.; Под ред. Ю.А. Ершова, В.А. Попкова. – М. : Высш. шк., 2008. – С.179-189.
1.11. Комплексные соединения
Строение и номенклатура комплексных соединений
В XIX веке был накоплен экспериментальный материал, показывающий, что многие молекулы с уже реализованными химическими свойствами способны вступать в дальнейшие взаимодействия с образованием более сложных соединении второго порядка. К таким соединениям относятся комплексные соединения.
В 1893 г. швейцарским химиком-неоргаником Альфредом Вернером (1866–1919) была сформулирована теория, позволившая понять строение и некоторые свойства комплексных соединений и названная координационной теорией. Поэтому комплексные соединения часто называют координационными соединениями.
Соединения, в состав которых входят сложные ионы, существующие как в кристалле, так и в растворе, называются комплексными, или координационными.
Основные положения теории Вернера:
1. В составе комплексных соединений выделяют внутреннюю сферу, включающую центральный атом или ион комплексообразователя, вокруг которого находятся связанные с ним лиганды.
Внешнюю сферу комплексных соединений образуют ионы, непосредственно не связанные с комплексообразователем. Эти ионы удерживаются около внутренней сферы за счет сил электростатического взаимодействия.
3. Типичными комплексообразователями являются: атомы или ионы d-элементов, имеющие свободные орбитали (Сu+, Сu2+ ,Zn2+, Ni2+ ,Со3+, Fе2+, Fе3+, Mn2+, Pt2+ и др.). Комплексообразователи являются акцепторами электронов.
4. Лиганды - атомы, ионы, молекулы, имеющие избыток электронов или неподелённые электронные пары. Ими могут быть кислотные остатки (SO42-, CI-, NO3-), гидроксогруппы (ОН-) и нейтральные молекулы (Н2O, NН3, СО, органические вещества). Лиганды являются донорами электронов.
5. Механизмы комплексообразования связаны с возникновением межионного и межмолекулярного взаимодействий комплексообразователя с лигандами, но основной вклад в формирование внутренней сферы вносят донорно-акцепторные (координационные) взаимодействия.

|
Координация цианид-ионов вокруг иона железа |
6. Количество лигандов, связанных с комплексообразователем, определяется его координационным числом. Величина координационного числа зависит от природы комплексообразователя, лигандов и условий комплексообразования (концентрации, рН, температуры и др.)
Координационные числа наиболее распространенных комплексообразователей:
|
Kоординационное число |
Комплексообразователь |
|
2 |
Cu+, Ag+, Au+ |
|
4 |
Cu2+, Hg2+, Sn2+, Pt2+, Pb2+, Ni2+, Co2+, Zn2+, Au3+, Al3+ |
|
6 |
Fe2+, Fe3+, Co2+, Co3+, Ni2+, Cr3+, Sn4+, Pt4+ |
Разберите состав комплексных соединений с помощью следующих примеров:
K4[Fe(CN)6] – гексацианоферрат(II) калия,

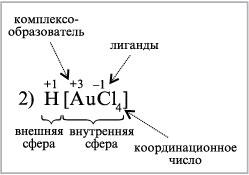
H[AuCl4] – тетрахлорозолотая кислота
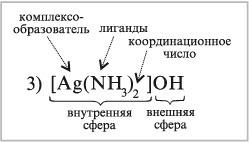
3) [Ag(NH3)2]OH – диамминсеребро(I) гидроксид
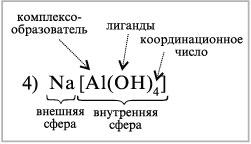
4) Na[Al(OH)4] – тетрагидроксоалюминат (III) натрия
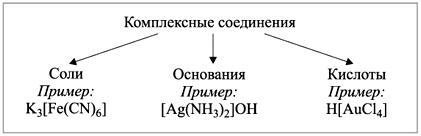
Классификация комплексных соединений
Большое многообразие комплексных соединений и их свойств не позволяет создать единую классификацию. Однако можно группировать вещества по некоторым отдельным признакам.
1) По составу.
2) По типу координируемых лигандов.
а) Аквакомплексы – это комплексные катионы, в которых лигандами являются молекулы H2O. Их образуют катионы металлов со степенью окисления +2 и больше, причем способность к образованию аквакомплексов у металлов одной группы периодической системы уменьшается сверху вниз.
Например: [Al(H2O)6]Cl3, [Cr(H2O)6](NO3)3.
б) Гидроксокомплексы – это комплексные анионы, в которых лигандами являются гидроксид-ионы OH–. Комплексообразователями являются металлы, склонные к проявлению амфотерных свойств – Be, Zn, Al, Cr.
Например: Na[Al(OH)4], Ba[Zn(OH)4].
в) Аммиакаты – это комплексные катионы, в которых лигандами являются молекулы NH3. Комплексообразователями являются d-элементы.
Например: [Cu(NH3)4]SO4, [Ag(NH3)2]Cl.
г) Ацидокомплексы – это комплексные анионы, в которых лигандами являются анионы неорганических и органических кислот.
Например: K3[Al(C2O4)3], Na2[Zn(CN)4], K4[Fe(CN)6].
3) По характеру заряда внутренней сферы различают катионные, анионные и нейтральные комплексы.
Например:
1) [Cu+( NН3)4]+ - катионный комплекс
2) [Zn2+(SCN)4]2– - анионный комплекс
3) [ Pt2+(CI)2(Н 2 О)2]0 - нейтральный комплекс
При составлении названия комплексного соединения учитывают знак заряда внутренней сферы комплекса.
Греческим числительным указывают число лигандов и называют нейтральные лиганды:

Лиганды-анионы называют с окончанием «-о»
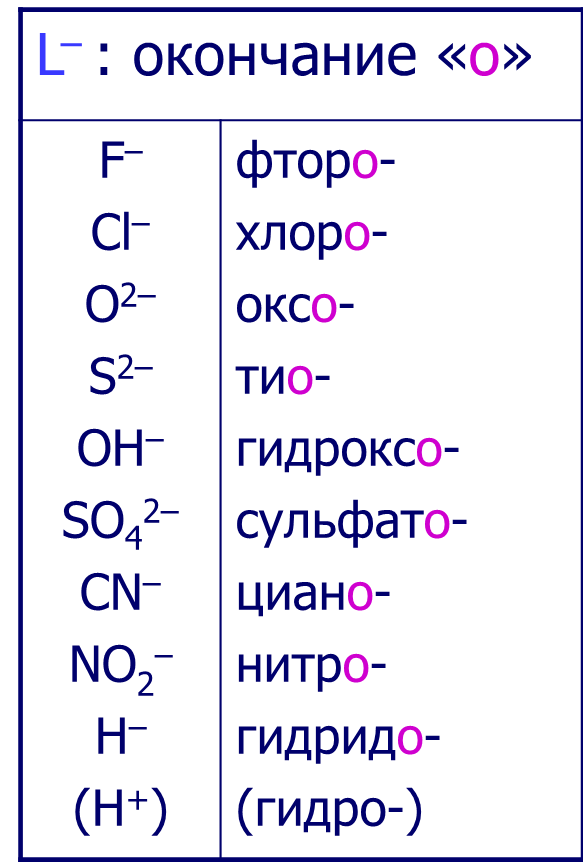
Комплексообразователь в катионных и нейтральных комплексах называют русским наименованием, а в анионных комлексах-латинским наименованием с окончанием «-ат».
Степень окисления комплексообразователя указывают римской цифрой в круглых скобках, за исключением нейтральных комплексов.
Например:
1) катионные комплексы:
[Cu2+(NH3)4]SO4 – сульфат тетраамминмедь(II);
[Al3+(H2O)6]Cl3 – хлорид гексаакваалюминий (III).
2) анионные комплексы:
[Fe3+(CN)6]3– – гексацианоферрат(III)-ион;
K2[Hg2+(I)4] – тетраиодомеркурат(II) калия;
3) нейтральные комплексы:
[Zn2+(Cl)2(H2O)2] – диаквадихлороцинк
[Pt4+(OH)2(NO2)2(NH3)2] – диамминдинитродигидроксоплатина
Значение комплексных соединений
Координационные соединения имеют исключительно большое значение в природе. Достаточно сказать, что почти все ферменты, многие гормоны, лекарства, биологически активные вещества представляют собой комплексные соединения.
Комплексы белков с катионами металлов играют роль металлоферментов, катализирующих большинство химических превращений. В качестве центрального иона металлофермента выступают катионы Mn2+,Cr2+,Fe3+, Zn2+ и др. К комплексным соединениям относятся гормон инсулин – комплекс ионов цинка с белками; витамин В12 - комплекс кобальта с порфирином.
Гемоглобин крови, благодаря которому осуществляется перенос кислорода от легких к клеткам ткани, является комплексным соединением, содержащим железо Fе2+ с порфирином, а хлорофилл, ответственный за фотосинтез в растениях, – комплексным соединением магния с тем же лигандом.
-

Гем-группа в молекуле гемоглобина
Значительную часть природных минералов, в том числе полиметаллических руд и силикатов, также составляют координационные соединения. Более того, химические методы извлечения металлов из руд, в частности меди, вольфрама, серебра, алюминия, платины, железа, золота и других, также связаны с образованием легкорастворимых, легкоплавких или летучих комплексов. Например: Na3[AlF6] – криолит, KNa3[AlSiO4]4 – нефелин.
Комплексные соединения находят широкое применение:
- для выведения из организма камней, которые образуются в почках, мочевом пузыре, желчных протоках;
- для маскировки нежелательных примесных элементов в составе лекарственных препаратов;
- для очистки организма от ядов, радиоактивных элементов, тяжелых металлов;
- в аналитической химии для определения ионов, т.к. яркая окраска многих внутрикомплексных соединений позволяет использовать реакции их образования для обнаружения катионов металлов в анализируемом растворе;
- для разделения некоторых металлов и получения металлов высокой степени чистоты; - для устранения жесткости воды;
- в качестве катализаторов важных биохимических процессов.
