
- •Государственное бюджетное образовательное учреждение
- •Предисловие
- •Тематические разделы дисциплины «Химия»
- •1. 1. Растворы. Способы выражения концентрации растворов
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.2. Введение в титриметрический анализ. Метод нейтрализации
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.3. Оксидиметрия. Перманганатометрия.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.4. Элементы химической термодинамики
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.5. Энергетика химических процессов
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.6. Коллигативные свойства растворов. Осмос.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.7. Водородный показатель среды растворов – pH.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.8. Буферные системы
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.9. Электрохимия. Потенциометрия.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.10. Окислительно-восстановительные потенциалы и электроды
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.11. Комплексные соединения
- •Контрольные вопрросы
- •Типовые задачи
- •Тестовые задания
- •Контрольные задания
- •Литература
- •1.12. Поверхностные явления. Способы получения и свойства коллоидных растворов.
- •Контрольные вопросы
- •Тестовые задания
- •Контрольные задания
- •Литература
- •1.13. Свойства растворов высокомолекулярных веществ (вмв)
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания
- •Контрольные задания
- •Литература
- •1.14. Биогенные элементы
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания
- •Темы рефератов
- •Литература
- •2. Инструкция по охране труда и пожарной безопасности для студентов при работе в лабораториях кафедры химии
- •2.1. Общие требования безопасности
- •2.2. Требования безопасности перед началом работы
- •2.3. Требования безопасности во время работы
- •2.4. Требования безопасности в аварийных ситуациях
- •2.5. Требования безопасности по окончании работы
- •3. Кодификатор зачетной работы дисциплины «Химия» для студентов I курса специальностей
- •060101- Лечебное дело; 060103-педиатрия
- •Характеристика зачетной работы и инструкция по ее выполнению
- •Часть 2
- •Часть 3
- •Заключение
- •Глоссарий
- •Ответы на тестовые задания
- •Приложения
- •1. Основные физико-химические константы
- •2. Важнейшие единицы си и их соотношение с единицами других систем
- •3. Приставки для дольных и кратных единиц си
Контрольные вопросы
Уравнение ионного произведения воды, его анализ.
Водородный и гидроксильный показатели среды.
Характеристика кислотности сред по величине pH.
Биологическое значение водородного показателя.
Типовые задачи
Задача 1. Рассчитать рН раствора соляной кислоты с молярной концентрацией вещества в растворе С(НСl) = 0,001 моль·дм-3.
Дано: Решение:
С (HCl)
= 0,001 моль·дм-3
HCl
H+
+ Cl-,
т.к.
= 1, то
(HCl)
= 0,001 моль·дм-3
HCl
H+
+ Cl-,
т.к.
= 1, то
 [H+]
= [HCl]
= 10-3
моль·дм-3
[H+]
= [HCl]
= 10-3
моль·дм-3
рН - ? pH = -lg [H+]
pH = -lg10-3 = 3
Ответ: pH = 3.
Задача 2. Рассчитать pH раствора гидроксида калия с молярной концентрацией вещества в растворе C(KOH) = 1,5·10-2 моль·дм-3.
Дано: Решение:
С (KOH)
= 1,5·10-2
моль·дм-3
KOH
K+
+ OH-,
т.к.
= 1, то
(KOH)
= 1,5·10-2
моль·дм-3
KOH
K+
+ OH-,
т.к.
= 1, то
 [OH-]
= [KOH]
= 1,5·10-2
моль·дм-3
[OH-]
= [KOH]
= 1,5·10-2
моль·дм-3
рН -? pOH = –lg[OH-]
pOH = –lg1,5·10-2 = 1,82
pH + pOH = 14 pH = 14 – pOH
pH = 14 – 1,82 = 12,18.
Ответ: pH = 12,18.
Задача 3. pH желудочного сока равен 1,65. Определить концентрации ионов [H+] и [OH-] в желудочном соке.
Дано: Решение:
p H
= 1,65 pH
= –lg
[H+]
H
= 1,65 pH
= –lg
[H+]
 lg
[H+]
= –pH
[H+]
= 10–pH
lg
[H+]
= –pH
[H+]
= 10–pH
[H+] - ? [H+] = 10–1,65 = 0,0224 моль·дм–3 = 2,24·10–2 моль·дм–3
[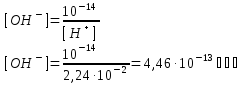 OH-]
- ? [H+]
· [OH-]
= 10–14
OH-]
- ? [H+]
· [OH-]
= 10–14
Ответ: [H+] = 2,24·10–2 мольˑдм–3; [OH–] = 4,46·10–13 мольˑдм–3 .
Тестовые задания для самоконтроля
Выберите правильный вариант ответа
01. КОНЦЕНТРАЦИЯ ИОНОВ ОН— (МОЛЬ/ДМ3) В РАСТВОРЕ ПРИ рН = 2,00 РАВНА ________МОЛЬ/ДМ3
1) 10–10
2) 10–2
3) 10–12
4) 10–4
02. ЗНАЧЕНИЯ С(ОН—) И С(Н+ ) В РАСТВОРЕ ПРИ рН = 5,0 СОСТАВЛЯЮТ______ МОЛЬ/ДМ3
1) 10–5 и 10 –9
2) 10–4 и 10 –10
3) 10–10 и 10 –4
4) 10–9 и 10 –5
03. ЗНАЧЕНИЯ С(ОН—) И С(Н+ ) В РАСТВОРЕ ПРИ рОН = 6,0 СОСТАВЛЯЮТ ______ МОЛЬ/ДМ3
1) 10–8 и 10–6
2) 10–4 и 10–10
3) 10–6 и 10–8
4) 10–7 и 10–7
04. УКАЖИТЕ рН СОЛЯНОЙ КИСЛОТЫ С КОНЦЕНТРАЦИЕЙ 0,1 МОЛЬ/Л И ВОДНОГО РАСТВОРА ГИДРОКСИДА КАЛИЯ С КОНЦЕНТРАЦИЕЙ 1,0 МОЛЬ/Л, СЧИТАЯ, ЧТО УКАЗАННЫЕ ВЕЩЕСТВА ДИССОЦИИРУЮТ ПОЛНОСТЬЮ
1) 1 и 14
2) 7 и 7
3) 14 и 0
4) 2 и 12
05. В РАСТВОРЕ АЗОТНОЙ КИСЛОТЫ С рН = 2 КОНЦЕНТРАЦИЯ ВЕЩЕСТВА ПРИ α = 100% РАВНА _____ МОЛЬ/ДМ3
1) 0,05
2) 0,1
3) 0,01
4) 0,001
06. рН РАСТВОРА ГИДРОКСИДА БАРИЯ РАВЕН 13, КОНЦЕНТРАЦИЯ ОСНОВАНИЯ В НЕМ ПРИ α =100% РАВНА ______ МОЛЬ/ ДМ3
1) 0,005
2) 0,1
3) 0,05
4) 0,001
07. РАСТВОР, В 500 МЛ КОТОРОГО РАСТВОРЕНО 1,825 г HCl, ИМЕЕТ рН, РАВНЫЙ
1) 2
2) 4
3) 5
4) 1
08. УКАЖИТЕ рН 0,003 МОЛЯРНОГО РАСТВОРА СОЛЯНОЙ КИСЛОТЫ
1) 11,5
2) 3
3) 7
4) 2,5
Контрольные задания
09. Рассчитать рН и рОН слюны, если концентрация ионов водорода в ней составляет
1,78·10–7 моль·дм-3.
10. Физиологическое значение рН крови 7,36. Определить концентрацию ионов [H+] и [OH-] в крови.
11. Рассчитать рН раствора соляной кислоты с концентрацией 0,03 моль/дм3 и водного раствора гидроксида калия с концентрацией 0,12 моль/дм3, считая, что указанные вещества диссоциируют полностью.
12. Определите рН кишечного сока, если концентрация гидроксид- анионов ОН- в составе кишечного сока составляет 2,3·10-6 моль·дм-3.
