
- •Государственное бюджетное образовательное учреждение
- •Предисловие
- •Тематические разделы дисциплины «Химия»
- •1. 1. Растворы. Способы выражения концентрации растворов
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.2. Введение в титриметрический анализ. Метод нейтрализации
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.3. Оксидиметрия. Перманганатометрия.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.4. Элементы химической термодинамики
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.5. Энергетика химических процессов
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.6. Коллигативные свойства растворов. Осмос.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.7. Водородный показатель среды растворов – pH.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.8. Буферные системы
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.9. Электрохимия. Потенциометрия.
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.10. Окислительно-восстановительные потенциалы и электроды
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература
- •1.11. Комплексные соединения
- •Контрольные вопрросы
- •Типовые задачи
- •Тестовые задания
- •Контрольные задания
- •Литература
- •1.12. Поверхностные явления. Способы получения и свойства коллоидных растворов.
- •Контрольные вопросы
- •Тестовые задания
- •Контрольные задания
- •Литература
- •1.13. Свойства растворов высокомолекулярных веществ (вмв)
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания
- •Контрольные задания
- •Литература
- •1.14. Биогенные элементы
- •Контрольные вопросы
- •Типовые задачи
- •Тестовые задания
- •Темы рефератов
- •Литература
- •2. Инструкция по охране труда и пожарной безопасности для студентов при работе в лабораториях кафедры химии
- •2.1. Общие требования безопасности
- •2.2. Требования безопасности перед началом работы
- •2.3. Требования безопасности во время работы
- •2.4. Требования безопасности в аварийных ситуациях
- •2.5. Требования безопасности по окончании работы
- •3. Кодификатор зачетной работы дисциплины «Химия» для студентов I курса специальностей
- •060101- Лечебное дело; 060103-педиатрия
- •Характеристика зачетной работы и инструкция по ее выполнению
- •Часть 2
- •Часть 3
- •Заключение
- •Глоссарий
- •Ответы на тестовые задания
- •Приложения
- •1. Основные физико-химические константы
- •2. Важнейшие единицы си и их соотношение с единицами других систем
- •3. Приставки для дольных и кратных единиц си
Тестовые задания для самоконтроля
Выберите правильный вариант ответа
01. УКАЖИТЕ СХЕМУ ХЛОРСЕРЕБРЯНОГО ЭЛЕКТРОДА
1) КСIнасыщ., АgОН |Аg
2) КBr, АgОН |Аg
3) Аg| АgCl, КСIнасыщ.
4) Аg| АgNO3, КNO3насыщ.
02. НА ГРАНИЦЕ РАЗДЕЛА МЕТАЛЛ – РАСТВОР СОЛИ МЕТАЛЛА ВОЗНИКАЕТ ___________ ПОТЕНЦИАЛ
1) контактный
2) диффузный
3) мембранный
4) электродный
03. УРАВНЕНИЕ НЕРНСТА ИМЕЕТ ВИД
1![]()
![]() )E
= E0
± ln
aкат.,
ан.
2) E
= E0
±
)E
= E0
± ln
aкат.,
ан.
2) E
= E0
±
![]() lg
aкат.,
ан.
3)
E
= E0
± lg
a(кат./ан.)
lg
aкат.,
ан.
3)
E
= E0
± lg
a(кат./ан.)
04. ДИФФЕРЕНЦИАЛЬНАЯ КРИВАЯ ПОТЕНЦИОМЕТРИЧЕСКОГО ТИТРОВАНИЯ ИМЕЕТ ВИД
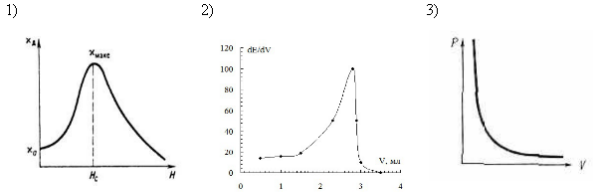
05. ВЕЛИЧИНА СТАНДАРТНОГО ЭЛЕКТРОДНОГО ПОТЕНЦИАЛА НЕ ЗАВИСИТ ОТ
1) концентрации вещества в растворе
2) природы электрода
3) величины ЭДС гальванического элемента
4) рН раствора
06. ПРИНЦИП ПОТЕНЦИОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ рН ЗАКЛЮЧАЕТСЯ В
1) измерении ЭДС цепи, состоящей из электродов определения и сравнения
2) измерении потенциала электрода сравнения
3) измерении электрической проводимости исследуемого раствора
4) измерении потенциала хлорсеребряного электрода
07. НАЙДИТЕ ЭДС ГАЛЬВАНИЧЕСКОГО ЭЛЕМЕНТА, СОСТАВЛЕННОГО ИЗ МАГНИЕВОГО И ЦИНКОВОГО ЭЛЕКТРОДОВ ПРИ 250C, ЕСЛИ КОНЦЕНТРАЦИИ ИОНОВ Mg2+ И Zn2+ В РАСТВОРЕ ОДИНАКОВЫ И РАВНЫ 0,1 МОЛЬ/Л.
Е0 (Мg2+/Mg) = – 2,37 B; Е0 (Zn2+/Zn) = – 0,74 B
1) -1,63B
2) +1,63B
3) –3,11B
4) + 3,11B
Дополните высказывание
08. МАКСИМАЛЬНАЯ РАЗНОСТЬ ПОТЕНЦИАЛОВ, ВОЗНИКАЮЩАЯ НА ГРАНИЦЕ ТВЕРДАЯ ФАЗА – РАСТВОР В МОМЕНТ УСТАНОВЛЕНИЯ ЭЛЕКТРОХИМИЧЕСКОГО РАВНОВЕСИЯ НАЗЫВАЕТСЯ _______.
09. ВЕЛИЧИНУ ЭЛЕКТРОДНОГО ПОТЕНЦИАЛА РАССЧИТЫВАЮТ ПО УРАВНЕНИЮ ___________ .
10. В ЭЛЕКТРОХИМИЧЕСКОМ РЯДУ НАПРЯЖЕНИЙ МЕТАЛЛЫ РАСПОЛОЖЕНЫ В ПОРЯДКЕ ________ ИХ АКТИВНОСТИ.
Контрольные задания
11. Рассчитать величину электродного потенциала цинкового электрода, если активная концентрация ионов цинка в жидкой фазе составляет 0,2 моль/дм3. Е0 (Zn2+/Zn) = – 0,76 В.
12. Вычислить активную концентрацию ионов меди Cu2+ в жидкой фазе медного электрода при Т = 298 К, если Е (Сu2+/Cu) = 0,8 В, Е0(Сu2+/Cu) = 0,35 В.
13. Как изменится потенциал хромового электрода, если активную концентрацию ионов Cr2+ в жидкой фазе электрода при 298 К понизить от 0,08 моль/дм3 до 0,05 моль/дм3?
Е0 (Cr2+/Cr) = – 0,913 В.
14. Для определения рН желчи была составлена водородно-хлорсеребряная цепь, ЭДС которой оказалась равной 0,577 В при 298 К. Определить потенциал водородного электрода и рассчитать рН исследуемой биологической жидкости.
(Ответ: рН = 12)
15. На миллиметровой бумаге построить калибровочный график зависимости ЭДС гальванической цепи от рН стандартных растворов по результатам потенциометрического анализа с использованием гальванической цепи включающей хлорсеребряный электрод сравнения и стеклянный электрод определения:
|
рН |
ЭДС, мВ |
|
1,0 |
40 |
|
2,0 |
85 |
|
3,0 |
120 |
|
4,0 |
165 |
|
5,0 |
205 |
По калибровочному графику определить рН исследуемого раствора, если ЭДС составила 150 мВ. Рассчитать концентрацию ионов Н+ в исследуемом растворе.
16. Провели потенциометрическое титрование 50 мл анализируемого раствора хлорида калия стандартным раствором нитрата серебра с молярной концентрацией С(AgNO3) = 0,10 моль/л. Получили следующие результаты: V(AgNO3) – объём прибавленного титранта, Е – ЭДС цепи соответственно:
|
V(AgNO3), мл |
23,50 |
24,00 |
24,20 |
24,30 |
24,40 |
24,50 |
25,00 |
25,50 |
|
Е, мВ |
146 |
165 |
194 |
233 |
316 |
340 |
373 |
385 |
Постройте кривые потенциометрического титрования и определите молярную концентрацию С(KCl) исследуемого раствора хлорида калия.
