
Гінекологічна патологія
.pdf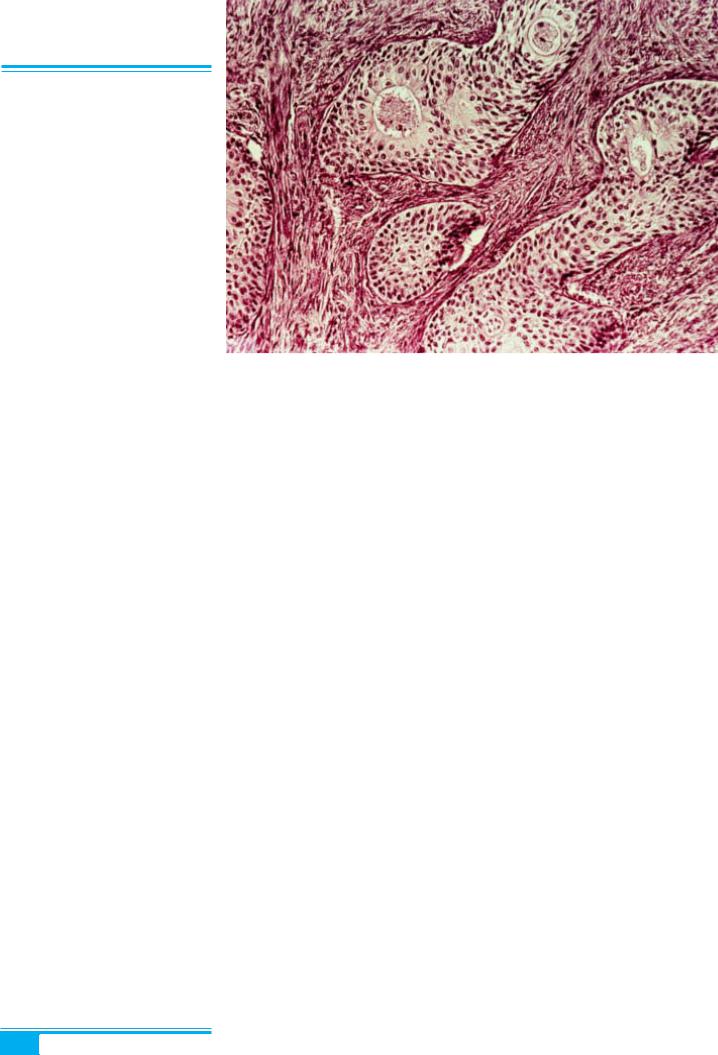
8. Яєчник
Рис. 8.60. Пухлина Бреннера. Ядра |
|
клітин з поздовжніми жолобками («ка- |
|
вове зернятко») |
|
стромальної інвазії. Інвазивна пухлина майже виключ- |
ною карциномою. Середній вік хворих становить 49– |
но представлена перехідно-клітинною або, рідше, |
56 років. Інколи відзначається асоціація з плоско- |
плоскоклітинною чи муцинозною карциномою. Інва- |
клітинним раком шийки матки. |
зивний компонент звичайно має помірний ступінь ди- |
Гістогенез. Епідермоїдні кісти виникають у моз- |
ференціації. |
ковій речовині яєчника. Вважають, що вони можуть |
Якщо доброякісні або пограничні елементи пухли- |
походити з епітеліальних інклюзійних залоз, Вальтар- |
ни Бреннера відсутні, карцинома класифікується як пе- |
дових залишків або rete ovarii. Виявлення хрящової |
рехідно-клітинна. Вона характеризується хвилястим |
тканини в деяких кістах наводить на думку щодо їх |
вистеленням кіст, внутрішньокістозною сосочковою |
можливоготератоматозного походження. |
структурою(папілярнийтип), наявністю«гнізд» атипо- |
Плоскоклітинна карцинома виникає переважно з |
вих епітеліальних клітин у фіброзній стромі. Пухлина |
епітелію, який вистилає дермоїдну кісту, менш часто |
звичайно належить до ІІ або ІІІ ступеня диференціації, |
— як компонент пухлини Бреннера або з ендометріоїд- |
але не має таких виразних ядерних рис, як серозні кар- |
ної кісти. Виділяють і так звані чисті форми плоско- |
циноми. У50 % пухлинвиявляєтьсямуцин, оточенийза- |
клітинного раку яєчників. До категорії поверхневих |
лозистим епітелієм. У більшості випадків пухлина є |
епітеліально-стромальних пухлин яєчників належать |
змішаною з іншими типами поверхневих епітеліальних |
лише чисті та ендометріоїдні оваріальні плоско- |
карцином(найчастішезсерозноюкарциномою). |
клітинні карциноми. |
Диференційний діагноз доброякісних пухлин Брен- |
Макроскопічне дослідження: епідермоїдні кісти |
нерапроводятьзендометріоїдною аденофібромою, що |
звичайно є однобічними, діаметром 0,2–4,6 см і містять |
має плоскоклітинну диференціацію (метаплазію); гра- |
жовто-білий, кремоподібний матеріал. Мікроскопічно |
нульозоклітинною та муцинозною пухлинами. Погра- |
стінка кісти вистелена зроговілим (кератинізованим) |
ничні та злоякісні пухлини Бреннера диференціюють з |
плоским епітелієм. У деяких випадках у стінці кісти |
метастатичною перехідно-клітинною карциномою се- |
трапляються Вальтардові клітинні «гнізда» або «гніз- |
чових шляхів (відсутність «гнізд» клітин, товстих со- |
да», які нагадують пухлину Бреннера. |
сочків і муцину); гранульозоклітинною пухлиною |
Плоскоклітинний рак яєчників є переважно со- |
(юний вік, часта ендокринна маніфестація, типова уль- |
лідним. Численні маленькі кісти виникають внаслідок |
траструктура). |
некрозів пухлинної тканини. Інколи спостерігаються |
Прогноз. Пограничні пухлини Бреннера звичайно |
кістозні пухлини. |
не розповсюджуються за межі яєчників; злоякісні ма- |
Мікроскопічне дослідження: картина плоско- |
ють екстраоваріальні прояви в 20 % випадків. Зло- |
клітинної карциноми варіює і характеризується як со- |
якісні перехідно-клітинні пухлини під час діагностики |
сочкова, поліпоїдна, кістозна, острівцева, дифузно |
в 70 % хворих мають розповсюдження в черевну по- |
інфільтративна, бородавчаста, саркоматоїдна. Пухли- |
рожнинуігіршийпрогноз, ніжзлоякісні пухлиниБрен- |
на майже завжди є низькодиференційованою. |
нера (середнє 5-річне виживання хворих не перевищує |
Диференційний діагноз проводять з ендометріоїд- |
35 %). П’ятирічне виживання хворих для ІА стадії зло- |
ною аденокарциномою з екстенсивною плоскоклітин- |
якісної перехідної карциноми дорівнює лише 43 % по- |
ною диференціацією (особливості структури залозис- |
рівняно з 88 % для злоякісної пухлини Бреннера. Але |
того компонента); вторинним плоскоклітинним раком |
вважають, що метастази перехідно-клітинної карцино- |
цервікального або іншого походження. Наявність доб- |
ми можуть бути більш чутливими до хіміотерапії. |
роякісного плоского епітелію, осередків ендометріозу |
|
і пухлини Бреннера свідчить на користь яєчникового |
Плоскоклітинні пухлини |
походженнякарциноми. |
Плоскоклітинні пухлини яєчників є рідкісними і |
Прогноз. Чистий та ендометріоїдний плоскоклітин- |
ний рак мають гірший прогноз, ніж у разі його розвит- |
|
представлені епідермоїдними кістами і плоскоклітин- |
ку з дермоїдної кісти. Важливе прогностичне значен- |
239

ня маютьстадія ігістопатологічний ступінь диференці- ації пухлини. Хворі з чистим плоскоклітинним раком яєчників не доживають і 1 року, з ендометріоїдним — однорічне виживання дорівнює 38 %.
Змішані епітеліальні пухлини яєчників
До змішаних епітеліальних пухлин яєчників нале- жать поверхневі епітеліально-стромальні пухлини, в яких макроскопічно виявляються різні пухлинні типи або при мікроскопічному дослідженні один або більше компонентів становлять щонайменше 10 % об’єму до- мінуючого компонента. Згідно з класифікацією ВООЗ, змішані епітеліальні пухлини яєчників поділяються на доброякісні, пограничні (з низьким малігнізуючим по- тенціалом) і злоякісні.
Найбільшчастимикомбінаціямипухлиннихтипівє:
— пухлина Бреннера з муцинозною кістозною пух- линою (змішана муцинозна — Бреннера пухлина);
Гінекологічна патологія
—ендоцервікальноподібна погранична муцинозна кістозна пухлина, змішана з серозною, ендометріоїд- ною або плоскоклітинною пухлиною;
—ендометріоїдна карцинома (аденокарцинома), змішана зі світлоклітинною карциномою (пухлини ма- ють схожий прогноз, тому він не погіршується у разі змішаної пухлини);
—перехідно-клітинний рак з іншою карциномою;
—ендометріоїдна карцинома (аденокарцинома) з серозним або недиференційованим компонентом. На- явність серозного абонедиференційованого компонен- та в III або IV стадії ендометріоїдної карциноми змен- шує 5-річне виживання хворих з 63 до 8 %, а 10-річне
—з 45 до 0 %.
Недиференційована карцинома
Недиференційована карцинома яєчників становить близько 5 % випадків епітеліального раку. На I стадії
Рис. 8.61. Недиференційований рак яєчників. Солідна пухлина
Рис. 8.62. Недиференційований рак яєчників. Маси злоякісних клітин, розділені фіброзною стромою
240

8. Яєчник
захворювання діагностується у 12 % пацієнток (у 20 % випадків спостерігаються білатеральні пухлини), на II
стадії — в 11 %, на III — у 51 % і на IV — у 26 %
випадків.
Макроскопічне дослідження: пухлина є переважно солідною, з зонами геморагій і некрозів і може нага- дувати низькодиференційовану серозну або ендомет- ріоїдну карциному (рис. 8.61).
Мікроскопічне дослідження: пухлина демонструє відсутність будь-якої диференціації або містить лише маленькі диференційовані зони (рис. 8.62). Виявляють- ся солідні маси, або нерівні «гнізда», або смуги уні- формних полігональних, або, рідше, веретеноподібних епітеліальнихклітинзвиразнимиядернимирисами, що може нагадувати картину саркоматоїдної карциноми. Інколи в залозах є маленькі фокуси диференціації, клітини з інтрацитоплазматичним муцином, псамомні тільця. Рідконедиференційована карциномаможебути представлена дрібноклітинним типом і демонструвати нейроендокринні риси (дрібноклітинна карцинома пульмонарного типу) чи гіперкальціємію (дрібноклі- тинна карцинома гіперкальціємічного типу).
Диференційний діагноз проводять з перехідно-
клітинноюкарциномою, низькодиференційованоюсар- комою, злоякісними мезодермальними змішанимипух- линами, лімфомами, дифузною гранульозоклітинною пухлиною. Накористьнедиференційованої карциноми свідчать розповсюджена стадія, ядерний плеоморфізм і гіперхроматизм, атипові мітотичні фігури, імунопо- зитивність до ЕМА й імунонегативність до інгібіну, відсутність ендокринної маніфестації. Диференційна діагностика метастатичної недиференційованої карци- номи базується на загальних критеріях щодо відокрем- лення первинних і метастатичних пухлин.
Ведення хворих з пухлинами яєчників
Більшість доброякісних епітеліальних пухлин (без- симптомні однобічні ураження) яєчників підлягають хірургічному лікуванню шляхом оофоректомії або, рідше, цистектомії. Біопсія протилежного яєчника у разі доброякісної пухлини не є необхідною. У жінок нерепродуктивного віку, особливо при наявності се- розної цистаденоми, яка має тенденцію до білатераль- ного ураження, рекомендується виконання гістерек- томії з двобічною аднексектомією.
При доброякісних і пограничних муцинозних пух- линах (є найбільшими з усіх епітеліальних пухлин) у молодих жінок виконують однобічну аднексектомію; у жінок старшого віку — гістеректомію з двобічною аднексектомією. Ускладненням може бути перфорація ірозривмуцинозноїкістиззатримкоюіподальшимро- стом муцинсекретуючого епітелію в черевній порож- нині (псевдоміксома очеревини). Захворювання часто рецидивує і потребує повторних лапаротомій для ліквідації обструкції кишок. З метою профілактики рецидивів призначають хіміотерапію (циклофосфамід, доксорубіцин, цисплатин) і муколітичні засоби.
Доброякісні аденофіброми, які складаються з епі- теліального (серозного, муцинозного, світлоклітинно- го, ендометріоїдного) і фіброзного компонентів, підля- гають хірургічному видаленню.
Пухлини Бреннера є переважно доброякісними і підлягають лікуванню шляхом простої оофоректомії.
При злоякісних пухлинах Бреннера (переважно дво- бічних) виконують гістеректомію з двобічною аднекс- ектомією і подальшою хіміотерапією.
У репродуктивному віці пухлини частіше є добро- якіснимиіпідлягаютьхірургічномувидаленнюшляхом лапароскопії або лапаротомії за Пфанненштилем. Солідні пухлини з сосочковими виростами мають більше шансів бути злоякісними. Можливість лапаро- скопічного лікування злоякісних пухлин яєчників дис- кутується (існує ризик раннього розповсюдження пух- лини). У жінок віком понад 40 років при підозрі на зло- якісну пухлину або при великих розмірах пухлини яєч- ників більшість фахівців рекомендують виконувати лапаротомію зпоздовжнім (вертикальним) розрізом та інтактним видаленням пухлини. В усіх випадках підоз- ри щодо злоякісності ураження яєчників можливо ви- користання інтраопераційної експрес-діагностики пух- лини.
При пограничних пухлинах яєчників у молодих жінок із нереалізованою репродуктивною функцією у стадії ІА (пухлина обмежена яєчником), відсутності ураження лімфатичних вузлів і негативних змивах з очеревини можливо проведення консервативних, в тому числі лапароскопічних операцій (однобічна ад- нексектомія). Якщо другий яєчник не має ознак ура- ження, його біопсія або резекція не є необхідною. У пацієнток старшого віку або з розповсюдженою ста- дією хвороби виконують радикальну гістеректомію з двобічною аднексектомією. При більш ніж I стадії по- граничної пухлини в комбінації з радикальним хірур- гічним лікуванням можна застосовувати хіміотерапію (6 курсів) і, можливо, променевутерапію, особливопри наявності інвазивних імплантів з виразною цитологіч- ною атипією. Вважають, що пацієнтки з доброякісни- ми (неінвазивними) імплантами звичайно не потребу- ють хіміо- або променевої терапії.
Як підготовка до оперативного лікування для оцін- ки стану печінки та регіонарних лімфатичних вузлів можебутивикористанакомп’ютернатомографія. Важ- ливими підготовчими заходами є профілактична анти- біотикотерапія, механічне очищення кишок і компре- сія нижніх кінцівок (з метою профілактики тромбоем- болічних ускладнень).
Рак яєчників інфільтрує перитонеальні поверхні (парієтальна очеревина, серозна оболонка кишок, піддіафрагмальна поверхня), особливо з правого боку (рис. 8.63). Це слід враховувати, тому що пухлина, особливо серозна, яка під час операції обмежена яєч- ником, може супроводжуватися маленькими зонами позаяєчникового розповсюдження. Важливу роль у розповсюдженні хвороби відіграє також лімфогенна дисемінація (затульні, загальні та зовнішні клубові, крижові, парааортальні й здухвинні лімфатичні вузли, (рис. 8.64). Серознакарциномамаєнайгіршийпрогноз; кращий прогноз у муцинозного, ендометріоїдного й світлоклітинного раку. Світлоклітинний рак може та- кож мати поганий прогноз. Перехідно-клітинний рак (варіант серозної папілярної карциноми) більш чутли- вий до хіміотерапії. Ендометріоїдний рак, асоційова- нийзендометріозомяєчників, маєкращийпрогноз, ніж типова ендометріоїдна карцинома.
Лікування раку яєчників комбіноване (хірургічне з подальшою хіміотерапією або променевою терапією). Первинним лікуванням інвазивного епітеліального
241

раку яєчників є максимальне видалення пухлинної маси. Підчасоперації (лапаротоміязповздовжнім роз- різом) виконується так зване хірургічне стадіювання, яке включає:
1)перитонеальні змиви (з дугласового простору, латеральних каналів, поверхні великого сальника, пе- чінки, нижньої поверхні діафрагми справа і зліва) та дослідження асцитичної рідини;
2)пальпаторний контроль усіх перитонеальних по- верхонь;
3)біопсію всіх підозрілих на метастази ділянок;
4)інфраколярну оментектомію.
Додатково, занеобхідності, виконуютьбіопсіюздух- винних і парааортальних лімфатичних вузлів, рандомі- зованібіопсіїзретровезикальноїочеревини, дугласово- гопростору, латеральнихканалівчеревноїпорожнини.
За наявності технічних можливостей виконується радикальна гістеректомія з двобічною сальпінгоофор- ектомією та інфраколярною оментектомією, а також видалення всіх уражених лімфовузлів. Рекомендують одночасне виконання апендектомії. У разі обструкції кишок виникає необхідність їх резекції. При розпов- сюджених стадіях (III–IV) раку яєчників виконується максимальна хірургічна резекція пухлини (циторедук- тивна операція).
Прогноз кращий у пацієнток віком до 50 років, якщо резидуальне ураження не перевищує 1,5 см. Не- сприятливими прогностичними ознаками є наявність
Гінекологічна патологія
великих метастазів до операції, асцит і перитонеаль- нийкарциноматоз. Розривкапсулипухлини(стадіяІС), особливо до моменту операції, є несприятливою озна- кою. При підвищенні рівня СА-125 понад 500 Од/мл оптимальне хірургічне втручання можливе лише в
20% випадків.
Уразі високодиференційованої епітеліальної кар- циноми, обмеженої одним яєчником (стадія ІА), у мо- лодих жінок з нереалізованою репродуктивною функ- цією можливе збереження матки і протилежного яєч- ника за таких умов:
1) пухлина обмежена одним яєчником;
2) пухлина є високодиференційованою (1-й ступінь) з відсутністю інвазії капсули, лімфатичних просторів або брижі яєчника;
3) наявність негативних змивів з очеревини;
4) біопсія сальника негативна;
5) молодий вік жінки і бажання зберегти репродук- тивну функцію.
Широка резекція другого візуально нормального яєчниканеєнеобхідною. Післяопераціїтакимпацієнт- кам показане динамічне ультрасонографічне спостере- ження, за необхідності — second-look лапароскопія.
Кахектичним хворим з раком яєчників III–IV стадії після екстенсивних операцій у післяопераційному пе- ріоді рекомендується тотальне парентеральне харчу- вання (гіпераліментація) в об’ємі 2000–3000 ккал на день (20 % декстроза, амінокислоти, ліпіди).
3
2
1
4
5
6
7
Рис. 8.63. Перитонеальне розпов- сюдження раку яєчників. Частина ве- ликого сальника, тонкої кишки і по-
8перечної кишки резекована:
1— матка; 2 — яєчник; 3 — вузли метастатичної хвороби; 4 — селезін- ка; 5 — ниркова артерія; 6 — вузли метастатичної хвороби; 7 — яєчнико- ва артерія; 8 — нижня мезентеріаль- на артерія
242

8. Яєчник
2
1
Рис. 8.64. Регіонарні лімфатичні вузли яєчника:
1 — загальні клубові; 2 — пара- аортальні; 3 — внутрішні клубові; 4 — здухвинні
Після оперативного видалення злоякісної пухлини пацієнткизвичайноотримуютькурсихіміотерапії(цис- платин, адріаміцин, циклофосфамід) або променевої терапії, особливо при значних розмірах резидуальної пухлини. Хіміотерапія призначається кожні 3 тижні. Можливо також використання інтраперитонеальної терапії цисплатином. Повторні(second-look) операції рекомендують після 6–12 курсів хіміотерапії (перева- га віддається лапароскопії). Хіміотерапія, особливо з використанням алкілуючих агентів (цисплатин ідоксо- рубіцин), можепідвищуватиризикподальшогорозвит- ку лейкемії (з 2 % через 4 роки до 10 % через 8 років після хіміотерапії). Післяопераційна променева тера- пія може застосовуватись у комбінації з хіміотерапією. Пацієнткам з рецидивним асцитом і (або) гідроторак- сом виконують парацентез або торакоцентез; у плев- ральну порожнину вводять склерозивні розчини для профілактики повторного накопичення рідини.
Імунотерапевтичні агенти, зокрема Corynebacterium parvum (C. parvum) і бацилиCalmette — Guerin (BCG),
призначаютьсязметоюдосягненняімунноївідповідіта розвитку пухлинної резистентності у хазяїна. Ці аген- ти можуть застосовуватися в комбінації з цитотоксич- ною хіміотерапією з метою покращання її результатів. Для інтраперитонеальної імунотерапії використову- ють такі препарати, як інтерферон, кілерні клітини, ак- тивованілімфокінами(LAK), інтерлейкін-2 (IL-2) іфак- тор некрозу пухлини (TNF).
Досліджуються можливості застосування монокло- нальних антитіл в якості місцевого лікування рецидив- ного раку яєчників (пухлино-асоційований антиген, зв’язаний з131I, автологічні Т-лімфоцити з біспецифіч- ними моноклональними антитілами). Повідомляють, що трансфекція р53 в оваріальну карциному in vitro інгібує клітинну проліферацію.
3
4
Зародковоклітинні (герміногенні) пухлини
Герміногенні пухлини виникають із зародкових клітин яєчника. Вони посідають друге за частотою місце серед усіх пухлин яєчника (20–30 %).
Доброякісні кістозні тератоми (дермоїдні кісти, дермоїди) є найбільш частими з-поміж герміногенних пухлин (95 %). Злоякісними є лише 1–3 % зародково- клітинних пухлин, серед них найчастішою є дисгермі- нома (45 % усіх злоякісних герміногенних пухлин). Другою за частотою є незріла тератома, третьою —
пухлина ендодермального синуса. У жінок віком до 30
років зародковоклітинні пухлини є найбільш частими (60 %) серед усіх пухлин яєчників у цій віковій кате- горії, причому понад 1/3 з них у пацієнток віком до 21 року є злоякісними. Близько 90 % цих пухлин є чисти- ми і 10 % — змішаними.
Понад 60–75 % герміногенних пухлин яєчників під час діагностики мають І стадію, сприятливий прогноз відзначається в 90 % випадків при комбінованому лікуванні (хірургічне + хіміотерапія).
Гістогенез. Герміногенні пухлини походять від пер- винноїзародковоїклітиниіпоступоводиференціюють- ся аналогічно розвитку тканин ембріонального похо- дження (ектодерма, мезодерма й ендодерма) та екстра- ембріональнихтканин(жовтковиймішокітрофобласт) (рис. 8.65). Зародковоклітинні пухлини, які виникають в яєчнику, мають гомологічні варіанти в яєчках (дис- гермінома і семінома). Герміногенні пухлини звичай- но є однобічними, за виключенням тератом і дисгермі- ном. Більшість злоякісних зародковоклітинних пухлин належать до так званого «примітивного типу». Рідко ці пухлини виникають із соматичних тканин тератоми (плоскоклітинний рак); у цьому разі вони належать до так званого дорослого типу.
243

Класифікація зародковоклітинних (герміногенних) пухлин яєчника
I.Дисгермінома (варіант — з клітинами синцитіо- трофобласта)
II.Пухлина жовткового мішка
1.Пухлина ендодермального синуса.
2.Полівезикулярнийвітеліновийваріантпухлини.
3.Гепатоїдний варіант.
4.Залозистий варіант.
5.Ендометріоїдний варіант.
III. Ембріональна карцинома
IV. Поліембріома
V. Хоріокарцинома
VI. Тератоми
1.Незрілі.
2.Зрілі:
а) солідні; б) кістозні (дермоїдні кісти);
в) звторинною пухлиною (специфічний тип); г) фетиформні (гомункулюс).
3. Монодермальні:
а) струма яєчника (варіант — з вторинною пух- линою, специфічний тип);
б) карциноїд (інсулярний, трабекулярний); в) струмальний карциноїд; г) муцинознийкарциноїд;
д) нейроектодермальні пухлини (специфічний тип);
е) сальна пухлина; ж) інші пухлини.
VII. Змішаніформи(специфічний тип)
Пухлини, які виникають з клітин, не здатних до ди- ференціації, класифікуються як дисгерміноми. Ембріо- нальнакарцинома, навпаки, розвиваєтьсязполіпотент- них клітин, що можуть піддаватися диференціації. Пухлини, які складаються з ембріональних елементів, дістали назву тератом. Новоутворення, що розвива- ються з екстраембріональних елементів, поділяють на 2 категорії: пухлини, яківиникаютьзпопередниківтро-
Гінекологічна патологія
Таблиця 8.10
Маркери зародковоклітинних пухлин
Пухлина |
Маркер |
|
|
Пухлина ендодермального синуса |
AФП |
Ембріональна карцинома |
AФП, ХГ |
Хоріокарцинома |
ХГ |
Дисгермінома |
ЛДГ |
Незріла тератома |
Відсутні |
|
|
фобласта — хоріокарциноми або з ендодерми — пух- лини жовткового мішка.
Кілька біологічних маркерів виявлено як у тканині герміногенних пухлин, так і в сироватці крові пацієн-
ток (табл. 8.10).
Ці маркери можуть допомагати під час діагности- ки та диференційної діагностики герміногенних пух- лин, а також здійснювати контроль за ефективністю лікування. Так, наприклад, пухлини жовткового мішка секретують АФП. Після видалення пухлини си- роватковий рівень AФП нормалізується через 4–6 тижнів. Хоріонічний гонадотропін (ХГ) продукується в нормі плацентарним синцитіотрофобластом і про- міжним трофобластом. Він також синтезується трофо- бластичнимипухлиннимиклітинами(хоріокарцинома). Менш специфічні маркери включають лужну фосфата- зу та ізофермент лактатдегідрогеназу (ЛДГ). Лужну фосфатазу ідентифікують у плазматичній мембрані за- родкових клітин, що допомагає під час диференційної діагностики дисгерміноми з іншими пухлинами (на- приклад, зізлоякісною лімфомою). Лактатдегідрогена- за, яка в нормі продукується печінкою і центральною нервовою системою, може бути виявлена в дисгермі- номах і пухлинах ендодермального синуса.
Дисгермінома— нетератоматозназародковоклітин- на пухлина — є найбільш частою (50 %) злоякісною зародковоклітинною пухлиною і становить 1 % раку яєчників, а у віковій категорії до 30 років — 5–10 % оваріальної карциноми. Близько 80 % пухлин діагнос-
|
|
Зародкова |
|
|
|
|
||
|
|
клітина |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
Семінома |
Дисгермінома |
|
|
Пухлини з поліпотентних |
||||
|
|
клітин |
||||||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ембріональна карцинома |
|||
|
|
|
|
|
|
|
|
|
Екстраембріональні |
Ембріональна ектодерма, |
|||||||
структури |
мезодерма, ендодерма |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пухлина жовт- |
|
Хоріокарцинома |
|
|
Тератома |
|
||
кового мішка |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 8.65. Гістогенез зародковоклі- тинних (герміногенних) пухлин яєч- ника
244

8. Яєчник
туються у віці 20–30 років (середній вік хворих — 20 років), причому у 2/3 жінок — у І стадії. Описані ви- падки розвитку дисгерміноми під час вагітності. Пух- лина рідко виникає до 5 і після 50 років.
Гістогенез. Можливо, деякі дисгерміноми виника- ють з дисгенетичної гонади (пухлина розвивається з гонадобластоми). Близько 5 % дисгерміном розвива- ються у дівчаток із хромосомними аномаліями (46, XY або 45, Х/46, ХYмозаїцизм).
Клініка і діагностика. Звичайно симптоми пухли- ни пов’язані зі збільшенням яєчників і живота. При швидкому рості пухлини можливо виникнення симп- томів її перекручування з розвитком гемоперитонеуму. Захворювання нерідко супроводжується естрогенною маніфестацією (передчасний ізосексуальний пубертат- ний розвиток, порушення ритму менструацій). Інколи відзначаютьсясимптомиандрогенізації. Майжезавжди спостерігається підвищення сироваткових рівнів ЛДГ. Сироватковий рівень ХГ підвищений у 3 % випадків. Позаяєчникове (перитонеальне й лімфогенне) розпов- сюдження — на очеревину, ретроперитонеальні лімфа- тичні вузли — спостерігається у 1/3 пацієнток.
Пацієнткамздисгерміномою впубертатномуперіо- ді рекомендується дослідження каріотипу. При дисге- незії гонад обидва яєчники підлягають видаленню.
Макроскопічне дослідження: пухлина є солідною,
згладкою, часточковоюсерозноюповерхнею, середній діаметр — 15 см. Дисгермінома є білатеральною в 10– 20 % випадків, причому в половині цих випадків ура- ження другого яєчника мікроскопічне. На розрізі пух- лина м’ясиста, часточкова, кремового, сірого, роже- вого або рудувато-коричнюватого забарвлення. Інко- ли виявляються некрози і крововиливи (рис. 8.66). Кальцифікація свідчить про гонадобластомне похо- дження пухлини.
Гістопатологічне дослідження: гістологічно дис-
гермінома є ідентичною семіномі яєчка у чоловіків. Вона складається з уніформних зародкових клітин і є найменш диференційованою серед усіх пухлин цієї гру- пи. Пухлина утворена трьома клітинними типами: «гніздами» або трабекулами зародкових клітин, про- міжною фіброзною стромою і лімфоцитарним інфільт- ратом (рис. 8.67). Трапляються зони казеозноподібних некрозів. Круглі пухлинні клітини мають чіткі мемб-
рани, світлу або еозинофільну цитоплазму, багату на глікоген. Ядра клітин великі, круглі або сплощені, центрально розміщені; вони містять великозернистий хроматин і виразні ядерця, численні мітотичні фігури
(рис. 8.68).
Строма утворює тонкі або широкі фіброзні пучки, які містять зрілі лімфоцити (переважно Т-лімфоцити й макрофаги) і, інколи, лімфоїдні фолікули. В 20 % ви- падків спостерігається гранулематозна стромальна ре- акція. У3 % пухлинвиявляютьсясинцитіотрофобластні велетенські клітини (імунореактивні до ХГ), що не по- гіршує прогнозу. Лютеїнізовані стероїдсекретуючі стромальні клітини можуть бути перемішані з неопла- стичними клітинами або локалізуватися на периферії пухлини.
Диференційний діагноз проводять з пухлиною жовт- кового мішка (гіалінові тільця, відсутність стромаль- них лімфоцитів, імунореактивність до AФП); ембріо- нальною карциномою (залозиста і сосочкова структу- ра, темна цитоплазма, гіперхроматичні великі ядра, відсутність лімфоцитарного або гранулематозного ін- фільтрату); солідною світлоклітинною карциномою (трубчасто-кістозна і сосочкова структура, муцин, стромальні плазмоцити); великоклітинною лімфомою (відсутність глікогену, різні імуногістохімічні реакції).
Імуногістохімічне дослідження: дисгермінома зви-
чайно є негативною до цитокератину, карціоембріо- нального антигену (СЕА), AФПіХГідемонструє мем- бранозв’язану позитивність до плацентарної лужної фосфатази (PLAP). Якщо рівень ХГ перевищує 100 мМО/мл, дисгермінома звичайно містить елемен- ти хоріокарциноми і вважається змішаною зародково- клітинною пухлиною.
Лікування. У молодих жінок бажано збереження репродуктивної функції. Якщо пухлина обмежена яєч- ником, виконують однобічну аднексектомію після ре- тельного обстеження черевної порожнини з метою ви- явлення інтраперитонеального і ретроперитонеально- го розповсюдження пухлини. Але якщо розміри пухли- ни перевищують 15 см, після такої операції рецидиви можливі в 20 % випадків. З метою профілактики реци- дивів застосовують післяопераційну хіміотерапію або променеву терапію (якщо розмір пухлини перевищує 10 см). Пухлина є дуже радіочутливою (ефективність
Рис. 8.66. Дисгермінома. Зони гемо- рагій і некрозів
245

при рецидивних пухлинах дорівнює 75 %). Пацієнткам після консервативного лікування виконують динаміч- не ультрасонографічне дослідження і комп’ютерну то- мографію, контролюютьрівеньЛДГусироватцікрові. З метою збереження (резервації) функції яєчників мо- лодим пацієнткам протягом курсу хіміотерапії реко- мендується призначення агоністів гонадотропін-рилі- зинг-гормонів(ГнРГ).
Прогноз. П’ятирічне виживання хворих становить понад 90 % при ІА стадії дисгерміноми, 60–90 % для інших стадій або рецидивної пухлини.
Пухлини жовткового мішка становлять 10–20 %
злоякісних зародковоклітинних пухлин. Вони виника- ють переважно у дітей та підлітків (середній вік — 19 років) і є рідкісними після 40 років.
Гістогенез. Пухлина жовткового мішка частково нагадує так званий ендодермальний синус (жовтковий мішок) родентної плаценти, тобтоповторює (резюмує) ембріональний розвитокекстраембріональної тканини
— жовткового мішка. Жовтковий мішок людини має прямий зв’язок з первинною кишкою, яка належить до так званого вторинного пухирця жовткового мішка. Диференціація жовткового мішка може відбуватися за
Гінекологічна патологія
Рис. 8.67. Дисгермінома. Уні- формні атипові зародкові клітини, проміжна фіброзна строма і лімфоци- тарний інфільтрат
парієтальним або вісцеральним типом; але більшість пухлин демонструють обидва типи диференціації. Па- рієтальна диференціація жовткового мішка характе- ризується накопиченням в екстрацелюлярному про- сторі матеріалу, подібного до базальної мембрани, що складається з ламініну і колагену (IV тип) і є негатив- ним до AФП (мембранаReichert, аналогічна базальній мембрані клітин парієтального жовткового мішка у щурів). Вісцеральна диференціація жовткового мішка асоційована з продукцією ним AФП і гіалінових кра- пель. Кишкова та гепатоїдна диференціація в деяких пухлинах жовткового мішка означає як ембріональну, так і екстраембріональну диференціацію. Ці дані уз- годжуються з розвитком гепатобіліарних зачатків з первинної кишки.
Деякі пухлини жовткового мішка виникають у па- цієнток з дисгенезією гонад. Рідко пухлини жовтково- го мішка розвиваються з поверхневих епітеліальних пухлин.
Клініка. Пацієнтки звичайно скаржаться на болі в животі. Втазовій абоабдомінальній ділянці виявляють об’ємні придаткові маси. В сироватці крові підви- щується рівень AФП. Позаяєчникове розповсюдження (очеревина, ретроперитонеальні лімфовузли) відзна-
Рис. 8.68. Дисгермінома. Ядерна атипія, численні мітози
246
8. Яєчник
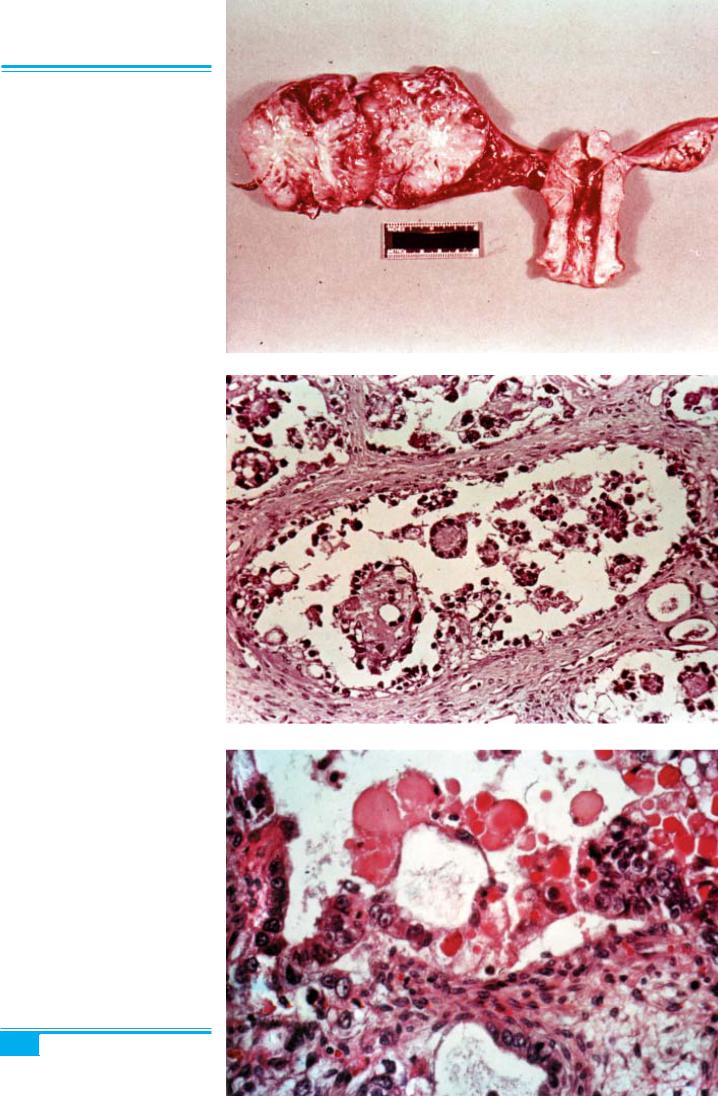
Рис. 8.69. Пухлина жовткового мішка (ендодермального синуса). Осе- редки некрозів і кістозної дегенерації
Рис. 8.70. Пухлина жовткового мішка. Примітивні мітотично активні ембріональні клітини утворюють сіт- ку кістозних просторів
Рис. 8.71. Пухлина жовткового мішка. Сосочкові виступи в кістозних просторах пухлини
247

чається в 30–70 % випадків під час визначення діаг- нозу.
Макроскопічне дослідження: пухлина є солідною або кістозною, крихкою, жовтого кольору; середній діаметр її дорівнює 15 см. На поверхні розрізу помітні зони геморагій, некрозів, кістозної дегенерації (рис. 8.69). Макроскопічна картина «медових стільників» (численні маленькі кісти) часто пов’язана з полівези- кулярним вітеліновим компонентом. У 15 % випадків виявляються інші елементи зародковоклітинних пух- лин (дермоїдні кісти). Пухлина майже завжди є одно- бічною.
Мікроскопічне дослідження: структура пухлини жовткового мішка може бути варіабельною (рис. 8.70– 8.72). Найчастіше це ретикулярна, або мікрокістозна структура, щохарактеризується ріденькоюсіткоюпро- сторів і каналів, вистелених примітивними мітотично активними клітинами зі світлою цитоплазмою і нерів- ними гіперхромними ядрами з виразними ядерцями. У 50 % випадків у ретикулярних зонах можна помітити так звані тільця Schiller — Duval. Вони складаються з округлих або витягнутих сосочків з фіброваскулярним ядромівистеленіпримітивнимициліндричними, кубої- дальнимисплощенимиабоцвяхоподібнимиклітинами. Ці клітини продукують гіалінові краплі, які містять α -фетопротеїн(AФП) та α 1-антитрипсинірозміщують- ся як у цитоплазмі клітин, так і екстрацелюлярно.
Стромальні зміни включають так звану парієталь- нуйвісцеральну диференціацію. Парієтальна диферен- ціація полягає у позаклітинному накопиченні речови- ни, подібної до матеріалу базальної мембрани, звичай- но в ретикулярних і солідних зонах. Інколи мезенхімо- подібний компонент бідної наколаген стромивключає зірчасті або веретеноподібні клітини, тонкостінні су- дини і, рідко, скелетні м’язи та хрящ.
Вісцеральна диференціація може бути представле-
на кількома варіантами. Полівезикулярна вітелінова структура характеризується щільною веретеноклітин- ною стромою, що містить кісти, які ексцентрично зву- жуються. Ці кісти мають гістологічну структуру нор- мального жовткового мішка людини і вистелені ци- ліндричним, кубоїдальним або сплощеним епітелієм. Фокуси кишкової (інтестинальної) диференціації на- явні в чітко окреслених залозах із великих «гнізд» при-
Гінекологічна патологія
мітивнихпсевдостратифікованих циліндричних клітин. Гепатоїдна структура пухлини жовткового мішка нагадує гепатоцелюлярну карциному: великі поліго- нальні клітини з рясною еозинофільною цитоплазмою, круглим центрально розміщеним ядром і одним вираз- ним ядерцем утворюють компактні маси, відокремлені фіброзними пучками. Виявляються численні гіалінові тільця. Як і гепатоцелюлярна карцинома, пухлина є
імунореактивною до СЕА.
Ендометріоїдний варіант нагадує високодиферен-
ційовану ендометріоїдну карциному ендометрія (аде- нокарциному): трубчасті залози, клітини з під’ядерни- ми і над’ядерними вакуолями.
Диференційний діагноз проводять з дисгерміномою, ембріональною карциномою, ендометріоїдною адено- карциномою, світлоклітинною карциномою, гепатоце- люлярною карциномою (табл. 8.11, 8.12).
Лікування. Хірургічне лікування пацієнток із ста- дією ІА може бути обмежене однобічною аднексекто- мією. До впровадження сучасної хіміотерапії пухли- на ендодермального синуса вважалась фатальною. Тому всім пацієнткам через 2 тижні після операції при- значають курси хіміотерапії: VAC-вінкристин, адріа- міцин D і циклофосфамід або більш токсичний VBP- вінбластин, блеоміцин, цисплатин, або Act-FU-Cy — актиноміцин D, 5-фторурацил і циклофосфамід (цито- ксан) та інші режими.
Прогноз. П’ятирічне виживання після комбіновано- го хірургічного лікування й хіміотерапії для хворих з І стадією дорівнює 70–90 %, з іншими стадіями — 30– 50 %. Сироватковий рівень AФП визначають для кон- тролю за ефективністю лікування й виявленням реци- дивної пухлини. Несприятливі прогностичні ознаки — це II і більша стадії, великий об’єм резидуальної пух- лини після циторедуктивної хірургії; ураження печін- ки.
Ембріональна карцинома — рідкісна герміногенна пухлина (3 %), яка складається з примітивних зарод- кових клітин. Виникає в юному віці (4–28 років). Вона може містити елементи трофобласта; у цьому разі спо- стерігається імунореактивність до ХГ і AФП.
Клініка. Відзначаються збільшення придатків мат- ки; ендокринна маніфестація — в 50 % випадків. Гор-
Рис. 8.72. Пухлина жовткового мішка. Центральний капіляр у сосоч- ковому виступі, вистеленому пухлин- ними клітинами
248
