
Гінекологічна патологія
.pdf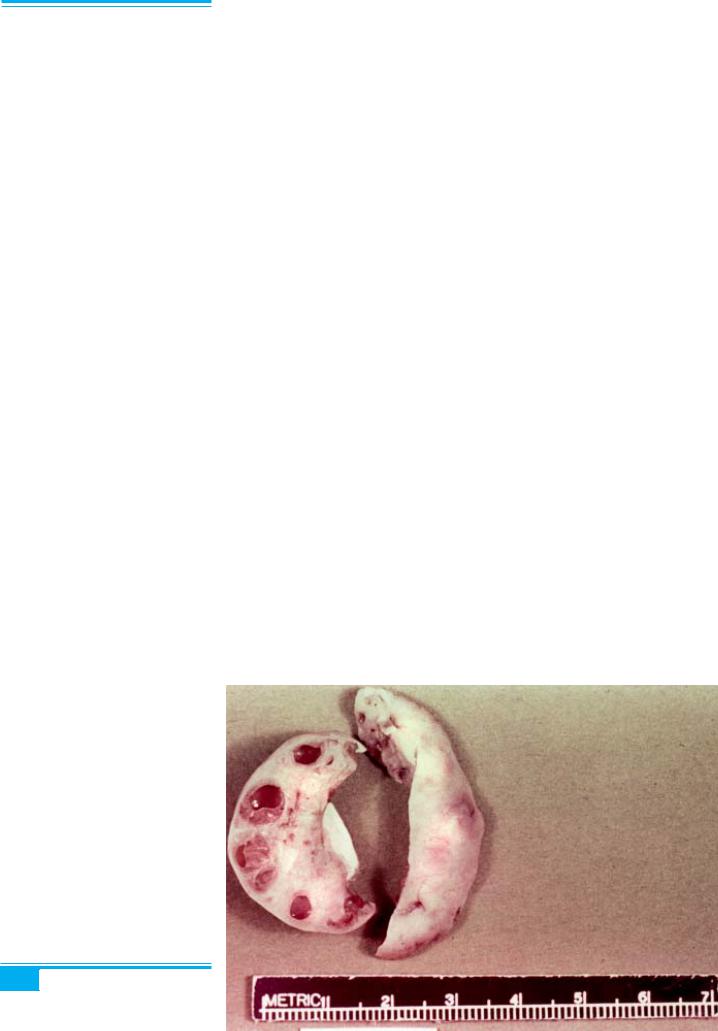
8. Яєчник
Макроскопічне дослідження: в яєчнику утворюють-
ся чітко окреслені м’ясисті вузли коричнюватого або червоно-коричнюватого кольору, які можуть бути со- ліднимиабо, рідше, кістозними(рис. 8.26). Інколитрап- ляються фолікули зі світлим або колоїдоподібним вмістом. Розмір лютеом варіює від мікроскопічного до більш ніж 20 см у діаметрі (середній розмір 6,6 см). Лютеома ніколи не виникає з жовтого тіла вагітності. Близько 50 % лютеом вагітності є численними і 30 %
— білатеральними.
Мікроскопічне дослідження: виявляються солідні масиуніформнихполігональнихлютеїнізованихклітин середніх розмірів, лютеїнізовані гранульозні клітини та лютеїнізовані тека-клітини сусідніх фолікулів (рис. 8.27). Клітини мають рясну еозинофільну цитоплазму з центральним поверхнево розміщеним, дещо плео- морфним і гіперхромним ядром і виразними ядерцями. Мітотичні фігури (до 7 в 10 полях зору) можуть бути аномальними. Інколивідзначаютьсябалоноподібнаде- генерація цитоплазми і внутрішньоклітинні колоїдні краплини. Пухка строма складається з ретикулінових волокон, які оточують групи клітин.
Лютеома вагітності спонтанно регресує після по- логів; розміри яєчників і сироватковий рівень андро- генів нормалізуються протягом кількох тижнів.
Гранульозоклітинна проліферація при вагітності
може бути випадковою знахідкою в яєчниках вагітних і, рідко, невагітних жінок і новонароджених. Проліфе- рація звичайно численна і спостерігається в атретич- них фолікулах, які оточені товстим шаром лютеїнізо- ваних тека-клітин. Гранульозні клітини можуть бути організовані в солідні, острівцеві, мікрофолікулярні або трабекулярні структури, містять невиразну цито- плазму і жолобкові ядра. Інколи проліферуючі кліти- ни можуть нагадувати маленькі Сертолі-клітинні пух- лини з солідною тубулярною структурою й помірною кількістю вакуолізованої цитоплазми, яка може місти- ти ліпіди.
Ектопічна децидуальна реакція в яєчниках може бути відповіддю на гормональний вплив вагітності (з 9-го тижня до закінчення вагітності). Інколи оваріаль- на ектопічна тканина асоційована з трофобластичною
хворобою, лікуванням прогестинами, гормонально ак- тивнимияєчниковимиінаднирковозалознимизахворю- ваннями. Вона може розвинутися після опромінення таза, інколи виявляється як ідіопатична знахідка в жінок у пре- і постменопаузі. Оваріальна децидуаль- на реакція звичайно є мікроскопічною і складається з рудувато-коричнюватих вузлів на поверхні яєчника і, рідко, з великих м’яких геморагічних мас. Децидуаль- на реакція також виникає в поверхневій кірковій стромі, у періоваріальних спайках і, інколи, в мозку яєчника.
Синдром полікістозних яєчників
Синдром полікістозних яєчників (СПКЯ) — захво- рювання центрально-гіпоталамічного генезу, яке ха- рактеризується тонічним підвищенням рівня лютропі- ну, або ЛГ. Типовими ознаками СПКЯ є овуляторна дисфункція (хронічна ановуляція), клінічні прояви гі- перандрогенії та (або) гіперандрогенемії при виклю- ченні супровідних розладів, наприклад, природжено- го дефіциту гідроксилази з пізнім початком. Диску- сійним залишається питання, чи є необхідною на- явність специфічних морфологічних змін у полікістоз- них яєчниках для визначення діагнозу СПКЯ.
Хворобу полікістозних яєчників вперше було опи- сано у 1935 роціStein і Leventhal (синдром Штейна — Левенталя) як тріаду класичних симптомів: аменорея, гірсутизм й ожиріння в асоціації зі збільшеними яєч- никами, які мають численні фолікулярні кісти в корі та стовщену капсулу (рис. 8.28).
Частота СПКЯ в популяції становить 3–5 %. Етіологія і патогенез. Етіологія ендокринних ано-
малій при СПКЯ остаточно не з’ясована. Вважають, що спадковість, центральні порушення продукції ка- техоламінів, психологічний стрес, резистентність до інсуліну можуть відігравати суттєву роль у патогенезі СПКЯ. Проте чітких доказів щодо первинної ролі будь-якого з цих порушень немає.
Синдром полікістозних яєчників вважають ендо- кринним захворюванням, що починається невдовзі після менархе і полягає в аномальній секреції гонадо- тропінів, спричиненій як підвищенням амплітуди пуль- сації гонадотропін-рилізинг-гормону (ГнРГ), так і зро-
Рис. 8.28. Полікістозні яєчники. Численні маленькі (близько 1 см) фолі- кулярні кісти в корі збільшеного яєч- ника, стовщення білкової оболонки
209

|
|
|
|
|
|
|
|
|
Гінекологічна патологія |
|
|
|
|
|
|
|
|
|
|
станням чутливості гіпофіза до дії ГнРГ. Така анома- |
щений рівень пролактину (20–30 нг/мл). Це, можливо, |
||||||||
лія призводить до підвищення рівня ЛГ у 2/3 пацієн- |
пов’язано зі збільшенням пульсації ГнРГ і (або) віднос- |
||||||||
ток з цим синдромом. Після болюсного викиду ГнРГ |
нимдефіцитомдопаміну. |
||||||||
спостерігається надмірна реакція ЛГ, на відміну від |
Чітко встановлено, що у більшості пацієнток із |
||||||||
ФСГ. Крім того, зростає рівень циркулюючих яєчни- |
СПКЯ відзначається певний ступінь інсулінової рези- |
||||||||
кових і наднирковозалозних андрогенів. Рівень тесто- |
стентності. Інсулін й інсуліноподібний фактор росту-1 |
||||||||
стерону в сироватці крові коливається від 0,7 до |
(ІФР-1) посилює продукцію андрогенів яєчниками |
||||||||
1,2 нг/мл, а рівень андростендіону — від 3 до 5 нг/мл. |
шляхом потенціювання стимулювальної дії ЛГ на яєч- |
||||||||
Отже, підвищеннярівняЛГйандростендіонупринизь- |
никову секрецію андростендіону і тестостерону. Висо- |
||||||||
ких значеннях ФСГ мають високу чутливість і спе- |
кий рівень зв’язування інсуліну рецепторами ІФР-1 є |
||||||||
цифічність щодо СПКЯ. Крім того, кожна друга паці- |
результатом гомологічності рецепторів ІФР-1 та інсу- |
||||||||
єнтка з цим синдромом має підвищений рівень дегід- |
лінових рецепторів. Гранульозні клітини також проду- |
||||||||
роепіандростерон сульфату (ДГЕАС > 4 мкг/мл). |
кують ІФР-1 і ІФР-зв’язуючі протеїни. Наслідком цієї |
||||||||
Хоча майже всі пацієнтки з СПКЯ мають підвище- |
локальної продукції ІФР-1 і ІФР-зв’язуючих протеїнів |
||||||||
ний рівень сироваткових андрогенів, вважають, що |
єпаракриннийконтрользазбільшеннямЛГ-стимуляції, |
||||||||
виразність гірсутизму залежить відступеня периферич- |
а також продукції андрогенів тека-клітинами у жінок |
||||||||
ної конверсії цих андрогенів за допомогою 5α -редук- |
із СПКЯ. У зв’язку з тим, що рівень ІФР-зв’язуючого |
||||||||
тази в більш сильний андроген дегідротестостерон |
протеїну у пацієнток із СПКЯ низький, рівень біодос- |
||||||||
(ДГТ). Індикаторомцьогопроцесуєпідвищенийрівень |
тупного ІФР-1 зростає, що в комбінації з ЛГ стимулює |
||||||||
циркулюючого 3α -діол-G. Пацієнтки з СПКЯ без |
вироблення тека-клітинами андрогенів. Резистентність |
||||||||
гірсутизму мають підвищений рівень циркулюючого |
до інсуліну і, як наслідок, гіперінсулінемія також сти- |
||||||||
тестостерону та (або) ДГЕАС, але нормальні значення |
мулюють продукцію андрогенів яєчниками. |
||||||||
3α -діол-G. Рівень ЛГ звичайно вище 15 мМО/мл; |
Експериментально було встановлено, що наванта- |
||||||||
співвідношення ФСГ/ЛГ > 3, в тому числі для імуно- |
женняандрогенами(андрогеннийексцес) непризводить |
||||||||
реактивних ЛГ і ФСГ. Рівень адренокортикотропного |
до аномальної секреції інсуліну. Незрозуміло, чому |
||||||||
гормону (АКТГ) у цих жінок є нормальним. Втім вияв- |
жінки зі СПКЯ мають резистентність до інсуліну, тим- |
||||||||
лено, що у деяких жінок інфузія АКТГ викликає над- |
часом як здорові жінки цього ж віку і маси тіла, але |
||||||||
мірну відповідь ДГЕАС, що свідчить про зростання |
без СПКЯ, не виявляють інсулінорезистентності. Гі- |
||||||||
чутливості до АКТГ ретикулярної зони надниркових |
перінсулінемія відзначається у пацієнток із СПКЯ з |
||||||||
залоз, тобто про участь надниркових залоз в патоге- |
ожирінням абобезнього, алелишепацієнтки зожирін- |
||||||||
нетичних механізмах СПКЯ. |
|
|
|
|
ням і СПКЯ здебільшого мають порушену толерант- |
||||
Додатково до зростання рівня циркулюючих анд- |
ність до глюкози. Негативний ефект ожиріння і СПКЯ |
||||||||
рогенів, у таких пацієнток виявлено збільшення кон- |
на інсулінорезистентність сумується. Існує думка, що |
||||||||
центрації біологічно активного естрадіолу, хоча за- |
первинногіперінсулінемія спричинюєгіперандрогенізм |
||||||||
гальний рівень циркулюючого естрадіолу може не під- |
у пацієнток із СПКЯ. Призначення антигіперглікеміч- |
||||||||
вищуватися. Зростання вмісту вільного естрадіолу |
них препаратів, наприклад метформіну, знижує рівні |
||||||||
спричинюється зменшенням концентрації стероїдзв’я- |
інсуліну й сироваткових андрогенів. |
||||||||
зуючого глобуліну, який продукується первинно при |
Отже, хоча яєчники при СПКЯ продукують над- |
||||||||
зростанні рівня андрогенів і вторинно — внаслідок |
мірну кількість андрогенів, особливо андростендіону, |
||||||||
ожиріння у цих пацієнток. Збільшення рівня біологіч- |
в них відсутні природні ендокринні аномалії. Зростан- |
||||||||
но активного естрадіолу може стимулювати зростан- |
няпульсаціїГнРГспричинюєтонічнепідвищеннярівня |
||||||||
ня пульсації ГнРГ і спричинювати підвищення рівня |
ЛГ, що, в свою чергу, стимулює стромальну тканину |
||||||||
ЛГ й ановуляцію. Крім того, знижений рівень стероїд- |
до продукції більшої кількості андростендіону та ін- |
||||||||
зв’язуючого глобуліну сприяє зростанню біологічно |
ших андрогенів, і, в свою чергу, призводить до перед- |
||||||||
активної фракції циркулюючих андрогенів (рис. 8.29). |
часної атрезії фолікулів. Крім цього, вяєчниках відзна- |
||||||||
Близько 20 % жінок із СПКЯ мають трохи підви- |
чається дефіцит ароматази, що зменшує оваріальну |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Незв’язаний |
|
|
Андрогенний |
|
|
|
|
|
|
Т+А2↑ |
|
|
ексцес |
|
|
|
|
|
|
|
|
|
|
|
|
Надниркові |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
залози |
|
|
|
|
|
|
|
|
|
|
|
Стероїдзв’язую- |
|
|
|
|
|||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
|
|
|
|
чий глобулін↓ |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Т+А2↑ |
|
|
|
|
|
|
|||
Незв’язаний Е2↑ |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
Рис. 8.29. Механізм можливої ролі |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
наднирковозалозних андрогенів у |
Яєчники |
|
|
ЛГ↑ |
|
|
Ановуляція |
розвитку андрогенного ексцесу й ан- |
||
|
|
|
|
овуляції: А2 — андростендіол; Т — те- |
|||||
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
стостерон |
|
|
|
|
|
|
|
|
|
|
210

8. Яєчник
конверсію андростендіону в естрон. Полікістозні яєч- ники не секретують збільшену кількість естрону або естрадіолу, але зростання рівня андростендіону з його подальшою периферичною конверсією в естрон разом зі зниженням рівня стероїдзв’язуючого глобуліну при- зводить до зростання рівня естрону в циркулюючій крові. Гіперестрогенія у відповідь посилює чутливість гіпофіза до ГнРГ і спричинює вивільнення ЛГ (рис. 8.30).
Клініка і діагностика. У жінок із СПКЯ можуть спостерігатися різні клінічні симптоми. Синдром полі- кістозних яєчників виявляють у молодих жінок із по- рушеннями менструального циклу, безплідністю, ожи- рінням і гірсутизмом. Близько 70 % хворих мають збільшені полікістозні яєчники, які виявляються при клінічному і ультрасонографічному обстеженні. При ультрасонографії типовими ознаками СПКЯ є збіль- шення яєчників з численними (понад 10) підкапсуляр- ними маленькими фолікулами (від 2 до 10 мм у діа- метрі) на периферії і підвищення ехогенності оваріаль- ної строми. Об’єм яєчників при СПКЯ перевищує 10 см3 (у нормі 4,7–5,2 см3). Але у багатьох жінок із клінічними й ендокринологічними проявами СПКЯ не виявляється типової ультрасонографічної картини полікістозних яєчників. Вважають, що в даному ви- падку наявна гіперандрогенна хронічна ановуляція, але не СПКЯ.
Ознаки гіперандрогенії варіюють від легких форм акне до тяжкого гірсутизму. Порушення менструаль- ного циклу можуть бути у вигляді олігоменореї, аме- нореї і менометрорагії. Ожиріння не є обов’язковим симптомом, але у пацієнток з СПКЯ воно корелює з високою частотою нерегулярних менструацій і гіпер- андрогенії, на відміну від жінок з нормальною ма- сою тіла. Клінічна картина СПКЯ може симулюва- ти розвиток андроген- або естрогенпродукуючої пухлини.
Акантоз (acanthosis nigrans) виявляється у 30 % па- цієнток з гіперандрогенією і у кожної другої пацієнт- ки зСПКЯупоєднанні зожирінням. Інколи виділяють окремий синдром: гіперандрогенія, інсулінова резис- тентність і acantosis nigrans (ГАІР-АН), який, скоріше,
єсубтипом СПКЯ.
Узв’язку з гіперандрогенією та ожирінням пацієнт- ки з СПКЯ мають аномальний ліпопротеїновий профіль. Зростання рівня тригліцеридів і зменшення холестеролу ліпопротеїнів низької щільності та ліпо- протеїнів високої щільності пов’язують зі збільшенням маси тіла і (або) гіперандрогенією. За відсутності ліку- вання СПКЯ ці аномалії персистують і можуть поси- люватись; вони тривають до припинення функції яєч- ників у постменопаузі. Доведено, що пацієнтки з СПКЯ мають більший ризик розвитку цукрового діа- бету, гіпертензії і, можливо, кардіоваскулярних роз- ладів.
Майже у 25 % здорових жінок з овуляторними цик- лами без гіперандрогенії або з її мінімальними проява- ми, але без порушення ритму менструацій, спостері- гається ультрасонографічна і макроскопічна картина, яка нагадує полікістозні яєчники. Це свідчить про відсутність чіткої межі між нормальними й полікістоз- нимияєчниками.
Зміни в ендометрії у пацієнток з СПКЯ варіюють від неактивних до гіперпластичних. У 5 % випадків виявляється аденокарцинома ендометрія (найчастіше
—ендометріоїдний ракнизькогоступенязлоякісності).
Макроскопічне дослідження: обидва яєчники
збільшені (понад 5 см у діаметрі), кулясті й містять чис- ленні маленькі фолікулярні кісти, щорозміщуються під гладкою, стовщеноюбілковоюоболонкою; інколияєч- никиможутьматинормальнірозміри. Нарозрізівкорі яєчника виявляються численні уніформні кісти діамет- ром до 1 см; мозкова речовина складається з гомоген- ної строми; жовті та білі тіла відсутні або розсіяні (див.
Рис. 8.30. Механізм підвищення співвідношення ЛГ/ФСГ, спричинено- го посиленням секреції ГнРГ внаслі- док зростання гіпоталамічної інгі- біції. Роль збільшення продукції яєч- никових андрогенів тека-клітинами й ациклічної продукції естрогенів за ме- ханізмом зворотного зв’язку і перси- стенції хронічної ановуляції при СПКЯ
|
|
|
|
|
|
|
Гіпоталамус |
|
|
||||||
|
|
|
|
|
|
|
|
Опіоїди |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
Дофамін |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||||||
|
↑ Збільшення |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
↑ Збільшення |
|||||
|
ациклічного |
|
|
|
|
|
|
|
|
|
|
||||
|
синтезу |
|
|
|
|
|
|
|
|
|
|
пульсуючого |
|||
|
естрогенів |
|
|
|
|
|
|
|
|
|
|
викиду ГнРГ |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Наднирковоза- |
|
|
|
|
↓ Зменшення |
|
|
↑ Збільшення |
|||||||
лозні андрогени |
|
|
|
|
|
|
ГнРГ-рецепторів |
||||||||
|
|
|
|
|
|
|
дозрівання |
|
|
|
|
||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
фолікулів |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Збільшення |
|
|
|
|
|
|
|
|
|
|
↑ Збільшення |
|||
|
|
|
|
|
|
Інгібін |
|
|
|
||||||
|
секреції яєчнико- |
|
|
|
|
|
|
|
|
чутливості |
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
вих андрогенів |
|
|
|
|
|
|
|
|
|
|
гіпофізарного ЛГ |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
до ГнРГ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
↓ Зменшення |
|
|
||||
|
↑ Збільшення |
|
|
|
|||||||||||
|
|
|
|
|
|
|
ФСГ |
|
|
||||||
|
стимуляції |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
тека-клітин |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
↓ Зменшення |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
ароматази |
|
|
|
|
|
↑ Збільшення |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
ЛГ-пульсації |
|
|
||||
211
|
|
Гінекологічна патологія |
|
|
|
рис. 8.28). Але ці морфологічні характеристики не є |
ним хворим із СПКЯ рекомендують оперативне (лапа- |
|
патогномонічними для СПКЯ. Вони також спостеріга- |
роскопічне) лікування (часткова оваріальна електро- |
|
ються у пацієнток із синдромом Кушинга (Іценко — |
каутеризація або лазерна деструкція), яке майже пов- |
|
Кушинга), природженою гіперплазією кори і деякими |
ністю витіснило традиційну клиноподібну резекцію |
|
пухлинами надниркових залоз. |
яєчників. Після часткової оваріальної деструкції |
|
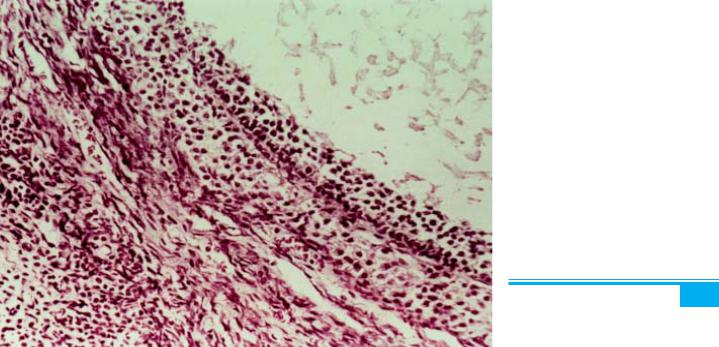
Гістопатологічне дослідження: фолікулярні кісти |
рівень андрогенів звичайно нормалізується. |
|
вистелені тонким шаром нелютеїнізованих гранульоз- |
Жінкам віком понад 35 років з надмірною яєчни- |
|
них клітин і звичайно товстим шаром лютеїнізованих |
ковою продукцією андрогенів внаслідок СПКЯ, не за- |
|
клітин внутрішньої теки, які можуть розміщуватися |
цікавленим у збереженні репродуктивної функції, які |
|
навколо атретичних фолікулів(фолікулярний гіперте- |
не бажають продовжити лікування, можливо виконан- |
|
коз) (рис. 8.31). Деякі лютеїнізовані стромальні кліти- |
ня радикальної гістеректомії з білатеральною сальпін- |
|
ни виявляються в більшості випадків, що нагадує кар- |
гоофоректомією з метою хірургічної профілактики |
|
тину стромального гіпертекозу. Зовнішня кора типо- |
раку ендометрія. |
|
во є гіпоцелюлярною, фібротизованою і містить чис- |
|
|
ленні, часто товстостінні кровоносні судини. Інколи |
|
|
виявляють супровідні пухлини яєчників різних типів. |
Стромальний гіпертекоз |
|
Диференційний діагноз. Інколи полікістозні яєчни- |
Стромальний гіпертекоз — доброякісне захворю- |
|
ки, які нагадують СПКЯ, виявляють у дівчаток у пре- |
||
пубертатному і пубертатному періодах, а також у |
вання яєчників, яке характеризується їх білатеральним |
|
дівчат після 20 років з первинним гіпотиреоїдизмом. |
збільшенням до 5–7 см у діаметрі. Захворювання час- |
|
Диференційну діагностику проводять зі стромальним |
тіше діагностують у жінок в пременопаузі, які нерідко |
|
гіпертекозом. |
мають супровідне ожиріння, гіпертензію і знижену то- |
|
Лікування СПКЯ залежить від клінічних проявів |
лерантність до глюкози. |
|
синдрому(гірсутизм, безплідність абоаменореячидис- |
Етіологія і патогенез. Захворювання може бути |
|
функціональні маткові кровотечі) і репродуктивних |
сімейним. У пацієнток нерідко діагностують синдром |
|
намірів. Якщо вагітність не є бажаною, методом ви- |
ГАІР-АН (гіперандрогенія, резистентність до інсуліну, |
|
боруєпризначеннякомбінованихоральнихконтрацеп- |
інколи асоційована з цукровим діабетом і acantosis |
|
тивів. Вживання оральних стероїдних контрацептивів |
nigrans). У лютеїнізованих стромальних клітинах і при- |
|
(з низькодозованим естрогенним компонентом і слаб- |
леглих веретеноподібних стромальних клітинах з до- |
|
ким антиандрогенним прогестиновим компонентом) |
помогою імуногістохімічних методів доведено на- |
|
сприяє зниженню рівня ЛГ і циркулюючого тестосте- |
явність ензимів, які конвертують холестерол у сте- |
|
рону і збільшує рівень стероїдзв’язуючого глобуліну. |
роїдні гормони, в тому числі в андрогени. |
|
Альтернативою може бутилікування аналогами ГнРГ, |
Клініка і діагностика. Захворювання нагадує |
|
але воно не перериває патофізіологічний ланцюг |
СПКЯ, але стромальний гіпертекоз частіше супрово- |
|
СПКЯ(після відміни препаратів рівень гонадотропінів |
джується поступовою або раптовою вірилізацією з |
|
йандрогенів повертається допочаткового). Уразіано- |
підвищенням рівня тестостерону, який продукується |
|
мальноїтолерантностідоглюкозипацієнткамрекомен- |
тека-клітинами. Початковими проявами можуть бути |
|
дують редукційну дієту і фізичні вправи для запобіган- |
ановуляція, аменорея або гірсутизм. Але, на відміну |
|
ня або відстрочення розвитку цукрового діабету. |
від СПКЯ, зі збільшенням віку пацієнтки яєчники про- |
|
Пацієнткам, які бажають вагітності, призначають |
дукуютьбільшукількістьтестостерону. Ознакамивіри- |
|
лікування, спрямоване на індукцію овуляції (кломіфен- |
лізації можуть бути скроневе облисіння, збільшення |
|
цитрат або гонадотропіни). При підвищеному рівні |
клітора, зміна тембру голосу, зменшення молочних за- |
|
ДГЕАС додатково призначають 0,5 мг дексаметазону |
лоз. У цей час рівень тестостерону звичайно більше |
|
нанічразомзкломіфен-цитратом. Кломіфенрезистент- |
2 нг/мл, якприяєчниковихчинаднирковозалозних тес- |
|
Рис. 8.31. Полікістозні яєчники. Лютеїнізація внутрішньої теки кісти (фолікулярний гіпертекоз), гіперпла- зія строми
212
8. Яєчник
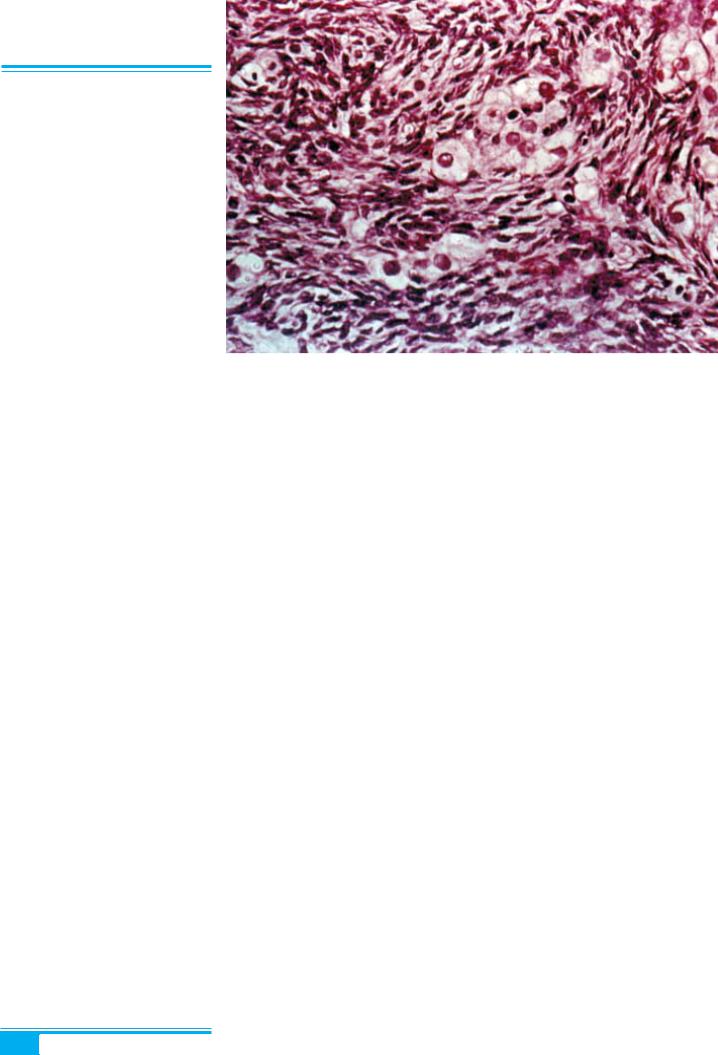
Рис. 8.32. Стромальний гіпертекоз. «Гнізда» та вузли тека-клітин, збага- чених ліпідами, серед гіперплазованої строми
тостеронпродукуючих пухлинах, хоча захворювання прогресує повільніше. Як і у пацієнток з СПКЯ, ви- являють підвищення рівня естрону, що може сприяти розвитку гіперплазії або раку ендометрія.
Макроскопічне дослідження: діаметр обох яєчників збільшений звичайно понад 8 см. Капсула яєчників товста, але, на відміну від СПКЯ, субкапсулярні кісти майже не трапляються. Строма варіабельна, білувато- го або жовтого кольору, що інколи симулює білате- ральні яєчникові пухлини. Рідко може бути однобічне ураження. Інколи виявляються супровідні яєчникові пухлини, які можуть бути гормоносекретуючими.
Мікроскопічне дослідження: на фоні гіперплазова-
ної строми спостерігаються «гнізда» або вузли тека- клітин з різним вмістом ліпідів уцитоплазмі (рис. 8.32). У жінок в пременопаузі також можуть виявлятися фо- лікулярний гіпертекоз і склероз кори яєчника, набряк і фіброз строми. В одному або обох яєчниках інколи виявляють гіперплазію гілюсних клітин або гілюсно- клітинні пухлини.
Лікування аналогічно такому при СПКЯ.
Стромальна гіперплазія
Мікроскопічний процес, якийспостерігається вяєч- никах жінок у пре- і постменопаузі (стромальна гіпер- плазія), інколи може мати андрогенну або естрогенну маніфестацію, а також супроводжуватись ожирінням, гіпертензією, порушенням метаболізму глюкози, хоча ці порушення є менш частими і менш виразними, ніж при стромальному гіпертекозі.
Макроскопічне дослідження: яєчники можуть мати нормальні розміри або бути трохи збільшеними з не- чітко окресленими білими або блідо-жовтими, інколи злитимивузликамивстромімозковоїречовинита(або) кори.
При мікроскопічному дослідженні виявляється за-
міщення мозкової речовини і, меншою мірою, кори проліферуючимималенькимистромальнимиклітинами
зневиразною, нелютеїнізованою цитоплазмою. Деякі
згіперпластичних клітин містять окислювальні ензи- ми, що важливо для продукції стероїдних гормонів. У деяких випадках гормони продукуються рідкісними лютеїновими або веретеноподібними клітинами пере-
хідного морфологічного типу (між стромальними ілю- теїновими клітинами).
Диференційний діагноз інколи проводять з фібро- моюяєчника ісаркомоюендометріальної строминизь- кого ступеня злоякісності.
Набряк яєчника
Описаний у пацієнток віком від 6 до 33 років. У 75 % випадків захворювання проявляється абдоміналь- ним болем, у тому числі гострим, та збільшенням жи- вота. Іншими проявами можуть бути порушення мен- струального циклу та (або) андрогенізація. Під час ла- паротомії виявляють збільшення яєчників (у 10 % ви- падків — білатеральне). Часткове або повне перекру- чування оваріальної ніжки наявне в кожному другому випадку, що свідчить про важливу роль цього проце- су в патогенезі набряку яєчника.
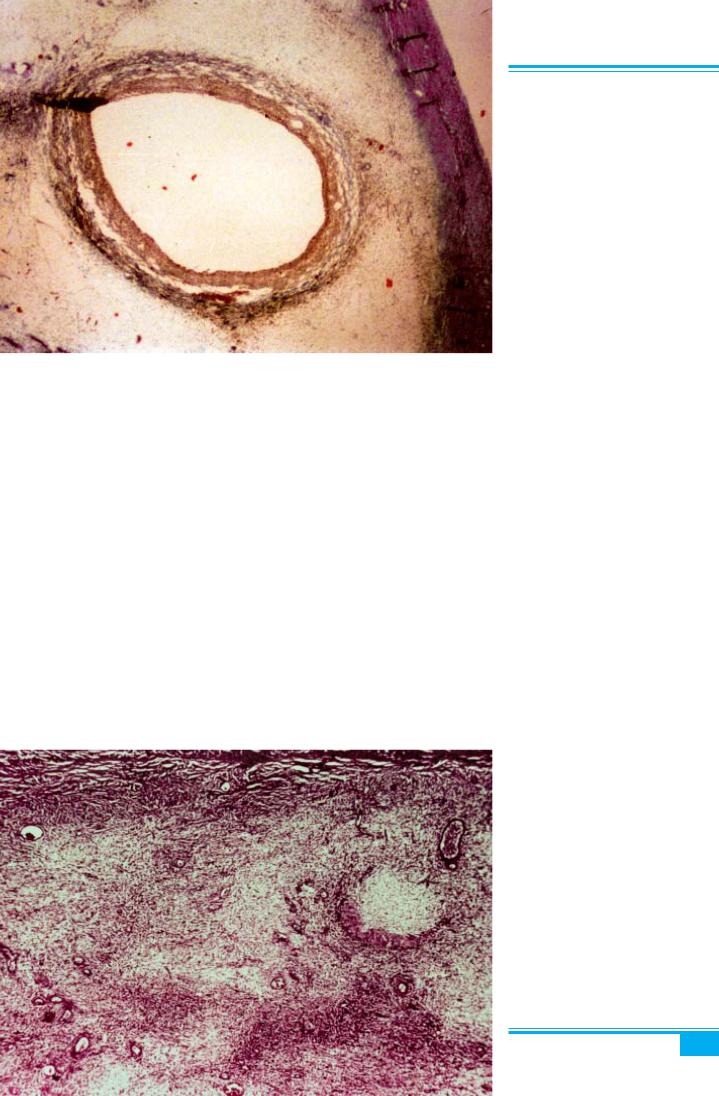
Макроскопічне дослідження: яєчники збільшені до 5,5–35 см у діаметрі (у середньому 11,5 см), ма- ють непрозору білу зовнішню поверхню. Інколи в корі спостерігаються маленькі фолікулярні кісти. З поверхні розрізу яєчника, яка має едематозний або желатиновий вигляд, виділяється значна кількість водявої рідини.
Мікроскопічне дослідження: набрякла, гіпоцелю-
лярна строма оточує поодинокі фолікули. Периферич- на кора типово складається зі щільної, неедематозної, колагенізованої тканини. У деяких випадках трапля- ютьсямаленькіфокусифіброматозноїстромальноїпро- ліферації й лютеїнізованих стромальних клітин (рис. 8.33, 8.34).
Диференційний діагноз проводять з едематозною фібромою, лютеїнізованою текомою, пухлиною Кру- кенберга (відсутність перснеподібних клітин й едема- тозноїтканини).
Фіброматоз яєчника
Виявляють у пацієнток віком 13–39 років (середній вік 25 років) зі скаргами на нерегулярні менструації або аменорею і, рідко, вірилізацію. Під час операції виявляють збільшення яєчників (у 20 % випадків —
213
двобічне ураження); в деяких випадках — перекручу- вання ніжки яєчника.
Макроскопічне дослідження: яєчники збільшені до
8–14 см у найбільшому вимірі і мають гладку або час- точковузовнішнюповерхню. Поверхнярозрізузвичай- но тверда, біло-сірого кольору, з кількома маленькими кістами. Спостерігається проліферація веретеноподіб- них клітин з виразним колагеновим оточенням дегене- руючих фолікулів (дериватів фолікулів). Фіброматозна проліфераціязвичайноєдифузною, алеінколипереваж- но уражає кору (кірковий фіброматоз). Типовими зна- хідками є лютеїнізовані стромальні клітини, фокуси стромального набряку, і, в деяких випадках, локальні «гнізда» клітин типу строми статевого тяжа.
Диференційний діагноз проводять з фібромою яєч- ника, гранульозоклітинноюпухлиноюзфіброматозним компонентом, пухлиноюБренера. Виявленнядериватів фолікулів свідчить на користь фіброматозу.
Гінекологічна патологія
Рис. 8.33. Масивний набряк яєчни- ка. Виразний набряк строми навколо фолікулярної кісти
збільшені у розмірах, інколи багатоядерні, з ознаками ядерногоплеоморфізму, гіперхромазії. Фізіологічнапро- ліферація гілюсних клітин може відбуватися під час ва- гітності і після менопаузи й клінічно проявлятися лег- ким ступенем гірсутизму. Андрогенна або естрогенна маніфестація цього стану може супроводжуватися підвищеннямсироватковогорівнятестостерону.
Гілюсноклітинна гіперплазія часто асоційована зі стромальною гіперплазією, стромальним гіпертекозом чи гілюсноклітинними пухлинами або з іншими пух- линами і кістами яєчника, які виникають поблизу його воріт. Рідко вона асоційована з синдромом ре- зистентних яєчників або дисгенезією гонад, а також із захворюваннями, які супроводжуються підвищен- ням рівня ЛГ.
Мікроскопічно досить складно відрізнити гілюс- ноклітинний вузол (проліферацію) від гілюсноклітин- ної пухлини (діаметр пухлини звичайно більше 1 см).
Гілюсноклітинна гіперплазія |
Змішані захворювання |
Характеризується наявністю в яєчнику вузлуватих |
Яєчникова вагітність становить близько 1 % усіх |
структур, утворених гіперплазованими гілюсними |
випадків ектопічної вагітності; частота її зростає у |
клітинами (гілюсними клітинами Лейдига). Ці клітини |
жінок, які користуються ВМС. |
Рис. 8.34. Масивний набряк яєчни- ка. Набряк строми в центральній час- тині кори яєчника
214

8. Яєчник
Клінічна симптоматика нагадує таку при трубній |
ням оваріальних судин, — можуть призводити до ат- |
вагітності (гострий біль у животі, гемоперитонеум). |
рофії яєчників. |
Макроскопічне дослідження: виявляють збільшений |
|
яєчник з осередками геморагій, що може нагадувати |
Автоімунний оофорит. У літературі описано 25 |
неопластичний процес. Ідентифікація ембріона полег- |
гістологічно підтверджених випадків автоімунного |
шує діагноз, який підтверджується даними гістологіч- |
оофориту, субтипу первинного ураження яєчників. Вік |
ного дослідження. Імплантація плідного яйця звичай- |
пацієнток коливається між 17 і 48 роками (середній вік |
но відбувається в corpus luteum. |
— 31 рік). Типовими симптомами є олігоменорея або |
Диференційний діагноз проводять з яєчниковою ге- |
аменорея, тазовий біль (може виникати внаслідок ут- |
стаційною трофобластичною хворобою. |
ворення численних фолікулярних кіст або перекручу- |
|
вання придатків матки). |
Синдром залишків яєчника може розвинутися у |
При імунологічному дослідженні виявляють сиро- |
жінок з наявністю в анамнезі технічно складної біла- |
ваткові антитіла проти стероїдних клітин різних типів, |
теральної оофоректомії (численні фіброзні адгезії вна- |
у деяких випадках — супровідні автоімунні захворю- |
слідок запальних захворювань органів таза або ендо- |
вання(хворобаАдісона, автоімунний тиреоїдит Хаши- |
метріозу тощо). Клінічні симптоми можуть розвинути- |
мототощо). |
ся через місяці й роки після оофоректомії і включати |
Макроскопічне дослідження: яєчники можуть бути |
тазовий біль, зокрема циклічний, та, в 50 % випадків, |
зменшеними або мати нормальні розміри. В 1/3 ви- |
наявність мас, що пальпуються, в проекції придатків |
падків один або обидва яєчники збільшені внаслідок |
матки. Інколи маніфестацією захворювання є симпто- |
утворення численних фолікулярних кіст. Кісти більш |
ми обструкції сечоводу або тонкої кишки. Під час ре- |
характерні дляранніх стадій хворобиі, можливо, спри- |
лапаротомії нерідко виявляються кісти жовтого тіла. |
чиняються підвищеним рівнем гонадотропінів. |
Мікроскопічне дослідження підтверджує наявність |
Мікроскопічне дослідження: виявляють лімфоцити, |
яєчникової тканини, яка може містити кістозні фоліку- |
плазматичніклітини, еозинофілиі, рідко, саркоїдоподібні |
ли або жовті тіла, оточені фіброзною тканиною, або |
гранульоми. Кількістьзапальнихклітинзбільшуєтьсяод- |
осередки ендометріозу. |
ночасно зі зростанням ступеня зрілості фолікула. |
|
Інфільтраціявнутрішньоїтекичастоєбільшінтенсивною, |
Мезотеліальнапроліферація— проліфераціямезоте- |
ніжгранульозногошару. Інколиспостерігаєтьсячастко- |
ліальнихклітинповерхніяєчника, втомучисліперіова- |
вадеструкціятека- і, вдеякихвипадках, гілюснихклітин. |
ріальніфіброзніадгезії, стінкиендометріоїднихтаінших |
|
кіст; потребуєдиференціаціїзнеопластичнимпроцесом. |
Перекручування та інфаркт яєчника частіше є ус- |
|
кладненнямоваріальнихіпараоваріальнихзахворювань |
Поверхнева стромальна проліферація — поліпоїд- |
(кіст, доброякіснихпухлині, інколи, злоякіснихпухлин). |
на стромальна проліферація клітин поверхні яєчника |
Перекручуваннянормальногояєчникаєрідкісним, час- |
в жінок у пізньому репродуктивному і постменопау- |
тіше спостерігається у новонароджених і дітей і може |
зальному періоді. |
бутибілатеральним. Потенційнурольуперекручуванні |
При макроскопічному дослідженні може мати ви- |
яєчникаможевідіграватийогомасивнийнабряк. |
гляд бородавчастих розростань. Частіше спостеріга- |
Клінічна картина симулює напад гострого апенди- |
ються лише мікроскопічні зміни. Виступи (сосочки) |
циту; біль у животі може стихати і поновлюватись. |
складаються з оваріальної строми з різним ступенем |
Інколи пальпуються збільшені придатки матки. Інтра- |
гіалінізації; вони вистелені одним шаром поверхнево- |
операційно виявляють перекручені збільшені тубоова- |
гоепітелію. Розмірутвореньдо1 смсвідчитьнакористь |
ріальні утворення з осередками геморагій таінфарктів. |
поверхневоїстромальноїпроліферації, понад1 см— се- |
У поодиноких випадках безсимптомного перекручу- |
розної поверхневої папіломи. Осередки поверхневої |
ванняабоінфарктівможевиникнутиавтоампутаціяту- |
стромальної проліферації часто є численними. |
бооваріальних мас, яківільно розміщуються учеревній |
|
порожнині або приєднуються до прилеглих структур. |
Передчасне виснаження яєчників характеризуєть- |
Будь-які геморагічні маси з осередками інфарктів |
ся припиненням менструацій у віці до 40 років. У яєч- |
підлягають гістологічному дослідженню з метою ви- |
никах виявляють примордіальні або незрілі фолікули, |
ключення неопластичного процесу. |
що нагадує картину постменопаузального яєчника. |
|
Синдром розвивається внаслідок виснаження фолі- |
Прості кісти мають нез’ясоване походження, тому |
кулів або втрати здатності примордіальних фолікулів |
що їх вистілка атрофується або руйнується під час або |
реагувати на дію гонадотропінів. Цей стан також |
після оперативного видалення кісти. Деякі прості кісти |
дістав назву гіпергонадотропного гіпогонадизму. |
вистелені тонким шаром індиферентних клітин, які на- |
Гіпогонадотропне ураження яєчників (гіпогона- |
гадують епітеліальні або мезотеліальні клітини. Стінка |
дотропний гіпогонадизм) є наслідком патології гіпо- |
кісти утворена фіброзною тканиною. Ідентифікація в |
фіза або гіпоталамуса, що призводить до порушення |
стінці кісти тека-клітин або серозного, ендометроїдно- |
секреції гонадотропінів. У цих випадках яєчник |
го чи іншого типу епітелію (трапляються навіть |
містить численні примордіальні фолікули, але розвит- |
кістозні елементи струми яєчника) допомагає визначи- |
ку їх не відбувається. Близько 30–40 % пацієнток з пер- |
ти більш специфічний діагноз. |
винним недорозвиненням яєчників мають аномальні |
|
статеві хромосоми чи дисгенезію гонад. Інколи ятро- |
Ідіопатична кальцифікація може призводити до ут- |
генні фактори: радіаційна терапія, хіміотерапія, |
ворення кам’янисто-твердого яєчника, який має нор- |
хірургічні втручання, що ускладнюються ушкоджен- |
мальні розміри. |
215

Гінекологічна патологія
При мікроскопічному дослідженні виявляють чис- |
|
|
Таблиця 8.1 |
ленні пластинчасті кальцифіковані фокуси без оточу- |
|
Фактори ризику розвитку раку яєчників |
|
ючих епітеліальних клітин. |
|
|
|
Диференційний діагноз проводять з серозними пух- |
|
Збільшення ризику |
Зменшення ризику |
линами, що містять псамомні тільця (неопластичні |
|
|
|
|
|
|
|
клітини), кальцифікованою гонадобластомою (виявля- |
|
Вік |
Грудне годування |
ютьY-хромосоми). |
|
Дієта |
Оральні контрацеп- |
|
|
||
Маткоподібні придаткові маси — рідкісне захво- |
|
Сімейнийанамнез |
тиви |
|
Індустріалізована країна |
Вагітність |
|
рювання, яке характеризується наявністю в яєчнику |
|
||
або в місці його локалізації центральної порожнини, |
|
проживання |
Перев’язка маткових |
вистеленої ендометрієм, оточеним товстою гладком’я- |
|
Безплідність |
труб і гістеректомія |
зовою стінкою. Вказівки на супровідні аномалії |
|
Відсутність пологів в анам- |
зізбереженням |
верхніх сечових шляхів у деяких випадках дозволяють |
|
яєчників |
|
припустити можливість мюллерового походження цієї |
|
незі |
|
|
Овуляція |
|
|
аномалії. Патогенетичний механізм у більшості ви- |
|
|
|
|
Медикаментозна стимуляція |
|
|
падків пов’язують з виразною гладком’язовою мета- |
|
|
|
плазією в осередках ендометріозу яєчників (так званий |
|
овуляції |
|
ендоміометріоз). У деяких пацієнток захворювання |
|
Тальк |
|
супроводжується підвищенням сироваткового рівня |
|
|
|
|
|
|
|
СА-125. В анамнезі деяких пацієнток є вказівки на пе- |
протягом щонайменше 5 років знижує ризик раку яєч- |
||
ренесений рак молочної залози. |
ників на 50 % (на 10–12 % щорік). Протекція зростає |
||
|
|||
|
при використанні оральних контрацептивів протягом |
||
Пухлини яєчників |
10 років. |
|
|
|
Існує точка зору, що експозиція тальку в ділянці |
||
Доброякісні пухлини яєчників є найбільш частими |
промежини збільшує ризик оваріальної карциноми, |
||
хоча цей зв’язок є слабким. Висловлюється думка, що |
|||
у віці 20–29 років. Ризик малігнізації пухлин яєчників |
трубна стерилізація і, в меншому ступені, гістеректо- |
||
зростає після 40–45 років і у жінок віком понад 45 |
мія зі збереженням яєчників можуть зменшувати ри- |
||
років дорівнює 33 %, тимчасом у віці 20–45 років — |
зик оваріальної карциноми. Наводяться дані, що за- |
||
менше ніж 1:15. Причини розвитку оваріальних пух- |
стосування медикаментозних препаратів, які стиму- |
||
лин не є визначеними і найбільш досліджені для раку |
люють овуляцію (кломіфен) більше 1 року, підвищує |
||
яєчників. |
ризик раку яєчників. Інші дослідники доводять, що |
||
|
застосування гонадотропінів у циклі фертилізації in |
||
Рак яєчників |
vitro не призводить до зростання частоти раку яєч- |
||
ників. |
|
||
|
|
||
Посідає друге за частотою місце серед усіх злоякіс- |
|
Вважають, що збільшення частки насичених тва- |
|
них новоутворень жіночої статевої системи після раку |
ринних жирів у харчовому раціоні збільшує ризик роз- |
||
ендометрія. Смертність від раку яєчника є найвищою |
витку раку яєчників, а рослинні харчові волокна змен- |
||
серед усіх гінекологічних малігнізацій. У США в 2000 |
шують його. Рак яєчників частіше виявляється у жінок |
||
році було зареєстровано близько 23 100 нових ви- |
білої раси в багатих індустріально розвинених країнах |
||
падків раку яєчників і близько 14 000 жінок померли. |
(США, Західна Європа), ніж в азіатських й африкансь- |
||
Важливим фактором, що пояснює високу смертність, |
ких жінок. |
|
|
є відсутність ранніх діагностичних критеріїв хвороби. |
|
Пацієнтки з раком яєчників становлять групу ри- |
|
В більшості випадків захворювання діагностується |
зику розвитку раку ендометрія та молочної залози. |
||
після розповсюдження пухлини за межі яєчників та |
Наводятьсядані, щопрофілактична оофоректомія зни- |
||
(або) таза. Частота раку яєчників зростає після 50 |
жує ризик розвитку раку молочної залози. |
||
років. |
|
Спадковий рак яєчників є рідкісним, але звичайно |
|
Незважаючи на численні епідеміологічні дослі- |
летальним захворюванням. Термін «сімейний рак яєч- |
||
дження, етіологія раку яєчників залишається невідо- |
ників» використовується при наявності генетичних пе- |
||
мою. Запропоновані численні теорії патогенезу раку |
редумов до його розвитку. Родичами першого ступе- |
||
яєчників (табл. 8.1). |
ня спорідненості вважають матерів, сестер або дочок |
||
Вважають, що захворювання може бути пов’язано |
хворої; другого ступеня — материнських або батьків- |
||
з частою овуляцією (щомісячна травма яєчника), |
ських тіток і бабусь. У разі сімейного раку яєчників |
||
відсутністю пологів в анамнезі або з пологами в більш |
захворювання має тенденцію розвиватися в більш ран- |
||
старшому віці. Висловлюється думка, що на розвиток |
ньому віці, ніж у загальній популяції. Вважають, що |
||
хвороби впливає «овуляторний вік» — кількість років, |
гермінативна мутація гена-супресора пухлини BRCA |
||
протягом яких відбувалась овуляція. Це число може |
на хромосомі 17q є відповідальною за значну частину |
||
бути зменшено шляхом вагітностей, грудного годуван- |
випадків спадкового раку яєчників. Проте спадковий |
||
ня, застосування оральних контрацептивів (індукція |
рак становить лише невелику частку всіх випадків |
||
ановуляції). Доведено, що надмірна експресія мутант- |
оваріальної карциноми. Є повідомлення, що застосу- |
||
ного білка р53 при раку яєчників має зв’язок з частою |
ванняоральнихконтрацептивів упацієнток змутацією |
||
овуляцією. Застосування оральних контрацептивів |
BRCA може знижувати ризик раку яєчників. |
||
216

8. Яєчник
|
|
|
|
Таблиця 8.2 |
|
Очікуваний ризик розвитку раку при мутаціях BRCA1 і BRCA2 |
|||
|
|
|
|
|
Генетичні мутації |
|
Ризик раку |
Ризик раку |
Ризик раку |
|
яєчників, % |
товстої кишки, % |
молочної залози, % |
|
|
|
|||
|
|
|
|
|
BRCA1 |
|
40–60 |
8 |
80–90 |
BRCA2 |
|
20 |
Зростає |
80–90 |
Відсутні |
|
1–2 |
2 |
10–12 |
|
|
|
|
|
Клонування гена BRCA1, який локалізується на 17q21 хромосомі, розширило уявлення про молекуляр- ну генетику раку яєчників, хоча його роль не зовсім зрозуміла. BRCA1 вважають геном-супресором, який виявляє надмірну експресію при пограничних карци- номах яєчника. Мутації генів BRCA1 і BRCA2 мають сильнийзв’язокзізростаннямризикуракумолочноїза- лози та яєчників (табл. 8.2).
Цікавим є той факт, що мікроскопічні ракові пух- лини, виявлені у пацієнток з мутаціями BRCA і візу- ально нормальними яєчниками, при дослідженні вияв- ляютьсярозвинутимиde novo серознимиабонедиферен- ційованимикарциномами.
За даними сучасних досліджень, більш ніж у 90 % випадків рак яєчників розвивається спорадично. Жінкам із сімейним раком яєчників (не домінантного генетичного типу), рекомендують трансвагінальне уль- тразвукове дослідження кожні 6 місяців після 35-річно- го віку. Альтернативним варіантом є використання профілактичноїгістеректоміїзбілатеральноюоофорек- томією у пацієнток, матері яких хворіли на рак яєч- ників. Деякі дослідники вважають, що спадковий рак яєчниківможематикращийпрогноз, ніжспонтанніра- кові пухлини.
Останніми дослідженнями встановлено, що біль- шість випадків раку яєчників (переважно, серозного) розвивається з мікроскопічного, «мініатюрного» раку (рання карцинома яєчника de novo), який розповсю- джується за межі яєчників до початку їх помітного збільшення. Деякі пухлини яєчників можуть розвива- тись зендометріозу (ендометріоїдний рак) абокіст (му- цинозна карцинома). Для цих варіантів раку яєчників, можливо, більш ймовірним є кістозне походження, ніж розвиток ракуde novo (тому ендометріоми і муцинозні кісти слід піддавати особливо ретельному гістологіч- ному дослідженню).
Дослідженнямизадопомогоюпроточноїцитометрії встановлено, що анеуплоїдія пухлини є несприятливим прогностичним фактором. Іншими незалежними про- гностичними чинниками є ДНК-індекс і фракція S- фази. Кращий прогноз спостерігається, якщо клітини S-фази становлять менш ніж 11 % або ДНК-індекс (відносний вміст ДНК в анеуплоїдних клітинах по- рівняно з диплоїдними) менше 1,3. Генетичний аналіз показав, що при раку яєчників (30 % випадків епітелі- ального раку), а також раку молочної залози спосте- рігається надмірна експресія онкогена HER-2/neu, що пов’язано з гіршим прогнозом. Мутація гена-супресо- ра пухлини р53 відбувається в 50 % випадків епіте- ліального раку яєчників. Надмірна експресія С-myc онкогена є більш характерною для серозної карцино- ми, K-ras онкогена — при пограничному раку яєч- ників.
Частота пухлин яєчників |
Таблиця 8.3 |
|
|
||
згідно з класифікацією ВООЗ |
||
|
|
|
Клас пухлини |
|
Частота, % |
|
|
|
Епітеліально-стромальні (звичайно |
|
65 |
епітеліальні) пухлини |
|
|
Зародковоклітинні (герміногенні) |
|
20–25 |
пухлини |
|
|
Пухлини строми статевого тяжа |
|
6 |
Ліпідноклітинні пухлини |
|
< 0,1 |
Гонадобластома |
|
< 0,1 |
Пухлини м’яких тканин (неспеци- |
|
|
фічні для яєчника) |
|
|
Пухлини, що не класифікуються |
|
|
Вторинні (метастатичні) пухлини |
|
|
Пухлиноподібні стани (несправжні |
|
|
пухлини) |
|
|
|
|
|
Отже, молекулярно-генетичні події навколо раку яєчників інтенсивно вивчаються, але сьогодні розви- ток і біологічна поведінка пухлини не є остаточно зро- зумілими.
Гістогенез. У жодному іншому органі тіла людини неутворюєтьсястільки різноманітних пухлин, яквяєч- никах. Це пов’язано зі складністю ембріо- та гістоге- незу яєчника та його гормональною активністю. Більшість пухлин яєчника мають гістологічну струк- туру, подібну до інших похідних мюллерового трак- ту: серозні пухлини нагадують слизову оболонку мат- кових труб, ендометріоїдні пухлини подібні до ендо- метрію, муцинозні демонструють риси ендоцервікаль- них пухлин. Початок розвитку більшості пухлин яєч- ника дають три основні клітинні типи:
1)поверхневий епітелій;
2)зародкові клітини;
3)строма статевого тяжа.
Найбільш розповсюдженою є гістологічна класи- фікація пухлин яєчників, запропонована ВООЗ. Най- частішими є епітеліально-стромальні пухлини яєч- ників (табл. 8.3).
Клініка і діагностика. Пухлини яєчника можуть бути безсимптомними або спричинювати абдоміналь- ний чи тазовий біль, збільшення живота. Звичайно клінічні прояви захворювання невиразні. Деякі пухли- ни, в тому числі рак яєчників, характеризуються дея- кими абдомінальними симптомами, нездужанням, гас- троінтестинальними розладами, аномальними матко- вими кровотечами, дизуричними розладами, втратою маси тіла. Гормонопродукуючі пухлини викликають
217

Гінекологічна патологія
КЛАСИФІКАЦІЯ РАКІВ ЯЄЧНИКІВ ЗА СИСТЕМОЮ TNM І FIGO
TNMFIGO-
категорії стадії
ТПервинна пухлина
Тx |
|
Не досить даних для оцінки первинної пухлини |
Т0 |
|
Первинна пухлина не визначається |
Т1 |
I |
Ріст обмежений яєчниками (одним або двома) |
Т1a |
ІA |
Пухлина обмежена одним яєчником, капсула інтактна, немає ознак пухлини на зовніш- |
|
|
ній поверхні яєчника, відсутні злоякісні клітини в асцитичній рідині або змивах |
|
|
з очеревини |
Т1b |
ІB |
Пухлина обмежена двома яєчниками, капсула інтактна, відсутні ознаки пухлини |
|
|
на зовнішній поверхні яєчника, відсутні злоякісні клітини в асцитичній рідині |
|
|
або змивах з очеревини |
Т1c |
IC |
Пухлина обмежена одним або двома яєчниками з будь-якою з таких ознак: розрив |
|
|
капсули, ознаки пухлини на поверхні яєчника, наявність злоякісних клітин в асцитичній |
|
|
рідині або змивах з очеревини |
Т2 |
ІI |
Пухлина уражає один або два яєчники з розповсюдженням у таз |
Т2а |
IIA |
Розповсюдження і (або) імплантація пухлини на матку і (або) маткову трубу (труби); |
|
|
відсутність злоякісних клітин в асцитичній рідині або змивах з очеревини |
T2b |
IIB |
Розповсюдження на інші тканини таза; відсутність злоякісних клітин в асцитичній |
|
|
рідині або змивах з очеревини |
Т2c |
IIC |
Розповсюдження в таз (ІІА або ІІВ) з наявністю злоякісних клітин в асцитичній рідині |
|
|
або змивах з очеревини |
Т3 i (або) |
III |
Пухлина охоплює один або обидва яєчники з мікроскопічно підтвердженими |
N1 |
|
перитонеальними метастазами за межами таза і (або) метастази в регіонарні |
|
|
лімфатичні вузли |
Т3a |
ІІIA |
Мікроскопічні перитонеальні метастази поза межами таза |
Т3b |
IIIB |
Макроскопічні перитонеальні метастази поза межами таза, жоден з них не перевищує |
|
|
2 см у найбільшому вимірі |
Т3c i (або) |
IIIC |
Перитонеальні метастази поза межами таза розмірами понад 2 см у найбільшому вимірі |
N1 |
|
і (або) метастази в регіонарні лімфатичні вузли |
M1 |
IV |
Віддалені метастази (за виключенням перитонеальних метастазів)* |
*Метастази в капсулу печінки належать до Т3/стадії III, в паренхіму печінки — до М1/стадії IV. У разі плевраль- ного випоту необхідне цитологічне підтвердження для зарахування до М1/стадії IV.
N — Регіонарні лімфатичні вузли
Nx Не досить даних для оцінки стану регіонарних лімфатичних вузлів N0 Немає ознак ураження регіонарних
лімфатичних вузлів
N1 Наявні метастази в регіонарних лімфатичних вузлах
М — Віддалені метастази
Mx Не досить даних для визначення віддалених метастазів
М0 Віддалені метастази не визначаються М1 Наявні віддалені метастази
pTNM Патоморфологічна класифікація
Категорії рТ, pN і рМ відповідають категоріям Т, N і М.
pN0 матеріал для гістологічного дослідження після тазової лімфаденектомії повинен включати не менше 10 лімфатичних вузлів
G Гістопатологічна градація
G Гістопатологічна градація
Gx Ступінь диференціації не може бути визначений
GB Погранична злоякісність
G1 Високий ступінь диференціації
G2 Середній ступінь диференціації G3–4 Низький ступінь диференціації або недиференційована пухлина
|
Групування за стадіями |
|
|
Стадія 0 |
Тis |
N0 |
M0 |
Стадія ІА |
Т1а |
N0 |
M0 |
Стадія IВ |
T1b |
N0 |
M0 |
Стадія IC |
T1c |
N0 |
M0 |
Стадія IIA |
Т2а |
N0 |
M0 |
Стадія IIB |
T2b |
N0 |
M0 |
Стадія ІІС |
Т2с |
N0 |
M0 |
Стадія ІІІА |
Т3а |
N0 |
M0 |
Стадія IIIВ |
Т3b |
N0 |
M0 |
Стадія IIIС |
Т3c |
N0 |
M0 |
|
Будь-яке Т |
N1 |
M0 |
Стадія IV |
Будь-яке Т |
Будь-яке N |
M1 |
218
