- •1 Основні поняття та цілі теорії металургійних процесів
- •2 Теоретичні основи утворення і дисоціації складних хімічних сполук
- •2.1 Термодинаміка утворення і дисоціації карбонатів
- •2.2 Термодинаміка реакцій утворення і дисоціації оксидів металів
- •2.3 Термодинаміка реакцій утворення і дисоціації оксидів заліза
- •2.4 Механізм процесів дисоціації і утворення складних хімічних з’єднань
- •2.5 Процеси окислення твердих металів
- •2.6 Будова структури окалини
- •3 Основи теорії горіння
- •3.1 Термодинаміка гомогенного горіння
- •3.2 Механізми горіння гомогенних реакцій
- •3.3 Термодинаміка реакцій горіння твердого вуглецю
- •3.4 Механізми горіння гетерогенних реакцій
- •3.5 Кінетичні закономірності горіння твердого вуглецю
- •4.1 Відновлення оксидів газами
- •4.2 Термодинаміка відновлення оксидів твердим вуглецем
- •4.3 Відновлення з участю розчинів
- •4.4 Відновлення оксидів заліза
- •4.5 Механізм відновлення оксидів металів газами
- •4.6 Механізм відновлення оксидів твердим вуглецем
- •5.Основыокислительных процессов
- •5.1. Состав, свойства и роль шлака в процессе производства стали
- •5.2.Металлический расплав
- •5.3. Важнейшие реакции сталеплавильных процессов
- •5.3.1 Окисление углерода
- •5.3.2 Окисление кремния
- •5.3.3 Поведение марганца
- •5.3.4 Поведение фосфора
- •5.3.5 Поведение серы
- •5.3.6 Газы в стали
- •5.4 Раскисление стали
- •5.4.1 Способы раскисления
- •5.4.2 Продукты раскисления и их удаление
4.5 Механізм відновлення оксидів металів газами
Реакція відновлення оксидів починається на окремих активних центрах на поверхні оксидів. На цих центрах відбувається адсорбція молекул відновника. Виникнення тривимірних зародків нової фази – металу або нижчого оксиду протікає важко, поволі – це так званий інкубаційний період.
У міру зростання поверхні розділу між старою і новими фазами процес швидшає – йде в автокаталітичному режимі. Каталізатором в цьому випадку виступає продукт відновлення, що утворюється. Але при зростанні поверхні розділу окремі ділянки нової фази, що утворилася, зливаються і швидкість росту поверхні сповільнюється. Відповідно, сповільнюється і хід процесу відновлення.
Першою стадією процесу відновлення є хімічна адсорбція молекул відновника – газу на активних центрах поверхні оксиду. При цьому відбувається деформація молекул газу-відновника аж до розриву цих молекул на окремі атоми. Деформовані молекули або атоми володіють підвищеною хімічною активністю. Цю стадію можна записати рівнянням МеОт + Вг = МеОтВадс.
Друга стадія процесу – кристалохімічне перетворення полягаючи в тому, що атом кисню відривається з молекули оксиду і з'єднується з атомом відновника з одночасною перебудовою решітки оксиду металу в решітку металу або нижчого оксиду МеОтВадс = МетВОадс.
Третя стадія полягає в десорбції молекули оксиду відновника в газову фазу
МетВОадс = Мет +ВОг.
Розрізняють два типи взаємодії, які відрізняються один від одного по співвідношенню швидкостей дифузії металу і кисню до поверхні оксиду і швидкості взаємодії відновника з оксидом.
Перший тип взаємодії – східчастий. Цей тип взаємодії характерний для вищих оксидів, відновлюваних до нижчих. Швидкість дифузії перевищує швидкість відновлення. На реакційній поверхні оксиду йде повільна взаємодія з відновником. Катіони металу з великою швидкістю, що утворюються при цьому, відводяться в глиб кристалів оксиду і не нагромаджуються на поверхні. Тому на поверхні оксиду не відбувається утворення решітки нового нижчого оксиду. Ця нова фаза, тобто "наступний" по ступеню зменшення окисленності оксид, виникає лише після того, як у всьому об'ємі відновлюваного зерна оксиду нагромадиться така кількість катіонів металу, яка приведе до утворення пересиченого металом розчину оксиду, і лише після цього у всьому об'ємі відбувається перетворення в нижчий оксид. На закінчення, до завершення одного ступеня відновлення у всьому об'ємі зерна оксиду, інші процеси розвитку не одержують. Таким чином, якщо узяти оксиди заліза, із зерна гематиту спочатку утворюється магнетит, потім вюстит і тільки потім вже залізо.
Другий тип відновлення – зональний. Швидкість відновлення перевищує швидкість дифузії. В цьому випадку на поверхні взаємодії оксиду з відновником швидкість відновлення настільки велика, що шляхом дифузії не встигає відводитися в глиб старої фази метал, що утворюється, і на поверхні відбувається накопичення металу. Утворюється пересичений розчин, виникає нова фаза – нижчий оксид. З'являється і межа розділу між старою і новою фазою. Потім аналогічна дія відбувається і на поверхні нової фази – утворюється наступний нижчий оксид даного металу. І на закінчення процесу на поверхні з'являється шар відновленого металу. Відбувається просторове розділення ступенів відновлення. Шматок гематиту, відновлений частково, складатиметься з чотирьох зон. Проте в ядрі шматка збережеться чистий гематит, а на поверхні буде шар заліза, між ними розташовуватиметься шар магнетиту, прилеглого до гематиту, і шар вюститу, прилеглий до заліза. Це спостерігається при t > 570С. Три межі розділу в процесі відновлення переміщатимуться до центрі шматка до тих пір, поки він весь не перетвориться на шматок заліза. Цей тип процесу є переважаючим при відновленні кускових матеріалів.
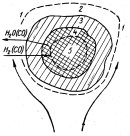
На рис. 4.9 показана схема зональної моделі відновлення шматка оксиду.
|
|
Рис. 4.9 - Схема відновлення шматка рудного матеріалу в струмі газу: 1 – газовий потік; 2 – ламінарна плівка; 3 – шар продукту відновлення; 4 – реакційна зона; 5 – початковий оксид
|
Відновний процес складається з ряду послідовних і паралельних стадій:
Підведення відновника з газового потоку через газовий дифузійний шар до зовнішньої поверхні оксиду.
Дифузія газу-відновника через пори і тріщини шару твердих продуктів реакції – металу або нижчого оксиду до межі розділу твердого продукту відновлення з початковим оксидом.
Хімічна взаємодія відновника з оксидом, включаючи адсорбцію молекул відновника, обмін електронами, зародження і зростання нової кристалічної фази, утворення оксидів відновника, десорбцію молекул оксиду відновника.
Дифузія іонів металу і кисню і перенесення електронів через кристалічні решітки продуктів відновлення і первинного оксиду.
Дифузія газоподібних продуктів відновлення через відновлений шар до зовнішньої поверхні по порах покривного шару і через тонкий газовий шар в ядро газового потоку.