
- •Основные законы химии
- •Моль. Молярная масса
- •Относительная атомная и молекулярная массы
- •Газовые законы
- •1. Закон о суммарном давлении смеси газов: давление смеси химически не взаимодействующих идеальных газов равно сумме парциальных давлений газов, составляющих смесь
- •Закон эквивалентов
- •Периодический закон и периодическая система химических элементов д. И. Менделеева
- •Строение атома
- •Модели Томсона и Резерфорда
- •Закон Мозли
- •Электронная оболочка атомов по Бору
- •Представления квантовой механики
- •Современная модель состояния электрона в атоме
- •Строение электронных оболочек атомов
- •Способы записи электронных конфигураций атомов и ионов
- •Периодический закон и периодическая система элементов д.И. Менделеева в свете учения о строении атомов
- •Свойства атомов. Их периодичность
- •Химическая связь и строение молекул
- •Ковалентная связь
- •Метод валентных связей
- •Сигма () и пи ()-связи
- •Донорно-акцепторная связь
- •Свойства ковалентной связи
- •Полярные и неполярные молекулы
- •Относительная электроотрицательность атомов
- •Ионная связь
- •Гибридизация атомных орбиталей
- •Гибридизация орбиталей и пространственная конфигурация молекул
- •Металлическая связь
- •Водородная связь
- •Типы кристаллических решеток
- •Валентность
- •Степень окисления
- •Комплексные соединения (комплементарность) Структура комплексных соединений
- •Хелаты и внутрикомплексные соединения
- •Реакции образования комплексных соединений
- •Номенклатура комплексных соединений
- •Пространственное строение и изомерия комплексных соединений
- •Диссоциация комплексных соединений в растворах. Константа нестойкости. Константа устойчивости
- •Связь в комплексных ионах
- •Реакции с участием комплексных соединений
- •1) Реакции обмена
- •2) Окислительно-восстановительные реакции
- •Элементы химической термодинамики Основные понятия
- •Внутренняя энергия. Первый закон термодинамики. Энтальпия
- •Закон Гесса. Следствия из него
- •Второй закон термодинамики. Энтропия
- •Термодинамические потенциалы
- •14 Типы реакций, различающиеся возможностьюи условиями протекания в зависимости от характера изменения ∆н и ∆s
- •Химическая кинетика Основные понятия
- •Скорость химической реакции
- •Зависимость скорости реакции от концентрации реагентов
- •Влияние температуры на скорость реакции
- •Дисперсные системы
- •Классификация дисперсных систем
- •Классификация дисперсных систем
- •Классификация дисперсных систем по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •Количественные характеристики дисперсных систем
- •Устойчивость дисперсных систем
- •Применение
- •Растворы Растворы в природе. Теории растворов
- •Механизм процесса растворения
- •Тепловые эффекты при растворении
- •Ненасыщенные, насыщенные и пересыщенные растворы
- •Растворимость различных веществ в воде
- •Выражение количественного состава растворов
- •Разбавленные растворы неэлектролитов и их свойства
- •Эбуллиоскопическая и криоскопическая константы
- •Растворы электролитов и их свойства
- •Диссоциация воды. Водородный показатель
- •Гидролиз солей
- •Буферные растворы
- •Водородный показатель (рН) растворов
- •Свойства кислотно-основных индикаторов
- •Применение
- •Окислительно-восстановительные реакции
- •Распространенные окислители и их продукты
- •Важнейшие восстановители и окислители
- •Методы составления уравнений окислительно-восстановительных реакций
- •Влияние среды на протекание окислительно-восстановительных реакций
- •Эквивалентные массы окислителя и восстановителя
- •Классификация окислительно-восстановительных реакций
- •4) Особые случаи овр:
- •Электрохимические системы Общая характеристика
- •Электродный потенциал. Измерение электродных потенциалов
- •Ряд стандартных электродных потенциалов (напряжений). Уравнение Нернста
- •Ряд напряжений металлов
- •Гальванические элементы, их электродвижущая сила
- •Аккумуляторы
- •Характеристики аккумулятора Эдисона и свинцового аккумулятора
- •Топливные элементы
- •Электролиз
- •Законы электролиза
- •Применение электролиза
- •Высокомолекулярные соединения (вмс) или полимеры
- •Физические свойства
- •Классификация
- •Полимеризационные полимеры
- •Поликонденсационные полимеры
- •Применение
- •Олигомеры
Аккумуляторы
Аккумуляторами называются гальванические элементы многоразового и обратимого действия. Они способны превращать накопленную химическую энергию в электрическую при разрядке, а электрическую в химическую, создавая запас ее в процессе зарядки. Так как э.д.с. аккумуляторов невелика, при эксплуатации их обычно соединяют в батареи.
Свинцовый аккумулятор. Свинцовый аккумулятор состоит из двух перфорированных свинцовых пластин, одна из которых (отрицательная) после зарядки содержит наполнитель - губчатый активный свинец, а другая ( положительная) - диоксид свинца. Обе пластины погружены в 25 - 30 % раствор серной кислоты (рис. 35). Схема аккумулятора
(-) Pb/ p -p H2SO4/ PbO2/Pb(+).
Перед зарядкой в поры свинцовых электродов вмазывается паста, содержащая помимо органического связующего оксид свинца PbO. В результате взаимодействия оксида свинца с серной кислотой в порах электродных пластин образуется сульфат свинца
PbО + H2SO4 = PbSO4+ H2O.
Аккумуляторы заряжают, пропуская электрический ток
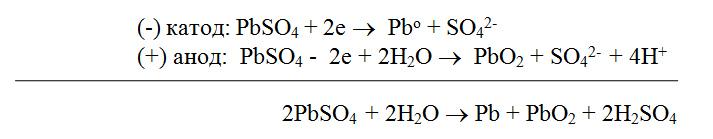
Процесс разрядки

Суммарно процессы, происходящие при зарядке и разрядке аккумулятора, можно представить следующим образом
![]()
При зарядке аккумулятора плотность электролита (серной кислоты) увеличивается, а при разрядке уменьшается. По плотности электролита судят о степени разряженности аккумулятора. Э.д.с. свинцового аккумулятора 2,1 В.
Преимущества свинцового аккумулятора - большая электрическая емкость, устойчивость в работе, большое количество циклов (разрядка- зарядка). Недостатки - большая масса и, следовательно, малая удельная ёмкость, выделение водорода при зарядке, не герметичность при наличии концентрированного раствора серной кислоты. В этом отношении лучше щелочные аккумуляторы.
Щелочные аккумуляторы. К ним относятся кадмиево-никеливые и железо-никелиевые аккумуляторы Т. Эдисона.
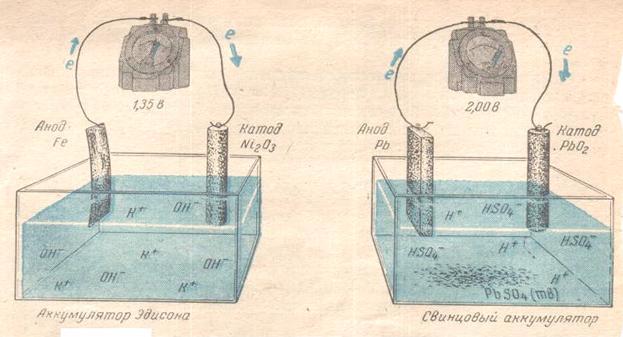
Схемы аккумулятора Эдисона и свинцового аккумулятора
|
Томас Эдисон(1847-1931) |
Они сходны между собой. Различие состоит в материале пластин отрицательного электрода. В первом случае они кадмиевые, во втором железные. Электролитом служит раствор КОН ω = 20 %. Наибольшее практическое значение имеют кадмиево-никелевые аккумуляторы. Схема кадмиево-никелевого аккумулятора
(-) Cd / раствор KOH /Ni2O3/Ni (+).
Работа кадмиевого-никелевого аккумулятора основана на окислительно-восстановительной реакции с участием Ni3+
![]()
Э.д.с. заряженного кадмиево-никелевого аккумулятора составляет 1.4 В.
В таблице представлены характеристики аккумулятора Эдисона и свинцового аккумулятора.
Характеристики аккумулятора Эдисона и свинцового аккумулятора
|
|
Аккумулятор Эдисона |
Свинцовый аккумулятор |
|
Окислитель |
Ni2O3 |
PbO2 |
|
Восстановитель |
Fe |
Pb |
|
Электролит |
КОН |
H2SO4 |
|
Напряжение (одного элемента) |
1,35 В |
2,0 В |
|
Особенности |
Легкий Постоянное напряжение
Дорогой
Необходимость перезарядки установить трудно (концентрация электролита постоянна) |
Тяжелый Переменное напряжение при разрядке
Недорогой
Необходимость перезарядки легко установить по напряжению и плотности H2SO4 |
Гальванические источники тока одноразового действия представляют собой унифицированный контейнер, в котором находятся электролит, абсорбируемый активным материалом сепаратора, и электроды (анод и катод), поэтому они называются сухими элементами. Этот термин используется применительно ко всем элементам, не содержащим жидкого электролита. К обычным сухими элементам относятся углеродно-цинковые элементы или элементы Лекланше, напряжение которых составляет 1,5 В.
Сухие элементы применяются при малых токах и прерывистых режимах работы. Поэтому такие элементы широко используются в телефонных аппаратах, игрушках, системах сигнализации и др.
