
- •Основные законы химии
- •Моль. Молярная масса
- •Относительная атомная и молекулярная массы
- •Газовые законы
- •1. Закон о суммарном давлении смеси газов: давление смеси химически не взаимодействующих идеальных газов равно сумме парциальных давлений газов, составляющих смесь
- •Закон эквивалентов
- •Периодический закон и периодическая система химических элементов д. И. Менделеева
- •Строение атома
- •Модели Томсона и Резерфорда
- •Закон Мозли
- •Электронная оболочка атомов по Бору
- •Представления квантовой механики
- •Современная модель состояния электрона в атоме
- •Строение электронных оболочек атомов
- •Способы записи электронных конфигураций атомов и ионов
- •Периодический закон и периодическая система элементов д.И. Менделеева в свете учения о строении атомов
- •Свойства атомов. Их периодичность
- •Химическая связь и строение молекул
- •Ковалентная связь
- •Метод валентных связей
- •Сигма () и пи ()-связи
- •Донорно-акцепторная связь
- •Свойства ковалентной связи
- •Полярные и неполярные молекулы
- •Относительная электроотрицательность атомов
- •Ионная связь
- •Гибридизация атомных орбиталей
- •Гибридизация орбиталей и пространственная конфигурация молекул
- •Металлическая связь
- •Водородная связь
- •Типы кристаллических решеток
- •Валентность
- •Степень окисления
- •Комплексные соединения (комплементарность) Структура комплексных соединений
- •Хелаты и внутрикомплексные соединения
- •Реакции образования комплексных соединений
- •Номенклатура комплексных соединений
- •Пространственное строение и изомерия комплексных соединений
- •Диссоциация комплексных соединений в растворах. Константа нестойкости. Константа устойчивости
- •Связь в комплексных ионах
- •Реакции с участием комплексных соединений
- •1) Реакции обмена
- •2) Окислительно-восстановительные реакции
- •Элементы химической термодинамики Основные понятия
- •Внутренняя энергия. Первый закон термодинамики. Энтальпия
- •Закон Гесса. Следствия из него
- •Второй закон термодинамики. Энтропия
- •Термодинамические потенциалы
- •14 Типы реакций, различающиеся возможностьюи условиями протекания в зависимости от характера изменения ∆н и ∆s
- •Химическая кинетика Основные понятия
- •Скорость химической реакции
- •Зависимость скорости реакции от концентрации реагентов
- •Влияние температуры на скорость реакции
- •Дисперсные системы
- •Классификация дисперсных систем
- •Классификация дисперсных систем
- •Классификация дисперсных систем по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •Количественные характеристики дисперсных систем
- •Устойчивость дисперсных систем
- •Применение
- •Растворы Растворы в природе. Теории растворов
- •Механизм процесса растворения
- •Тепловые эффекты при растворении
- •Ненасыщенные, насыщенные и пересыщенные растворы
- •Растворимость различных веществ в воде
- •Выражение количественного состава растворов
- •Разбавленные растворы неэлектролитов и их свойства
- •Эбуллиоскопическая и криоскопическая константы
- •Растворы электролитов и их свойства
- •Диссоциация воды. Водородный показатель
- •Гидролиз солей
- •Буферные растворы
- •Водородный показатель (рН) растворов
- •Свойства кислотно-основных индикаторов
- •Применение
- •Окислительно-восстановительные реакции
- •Распространенные окислители и их продукты
- •Важнейшие восстановители и окислители
- •Методы составления уравнений окислительно-восстановительных реакций
- •Влияние среды на протекание окислительно-восстановительных реакций
- •Эквивалентные массы окислителя и восстановителя
- •Классификация окислительно-восстановительных реакций
- •4) Особые случаи овр:
- •Электрохимические системы Общая характеристика
- •Электродный потенциал. Измерение электродных потенциалов
- •Ряд стандартных электродных потенциалов (напряжений). Уравнение Нернста
- •Ряд напряжений металлов
- •Гальванические элементы, их электродвижущая сила
- •Аккумуляторы
- •Характеристики аккумулятора Эдисона и свинцового аккумулятора
- •Топливные элементы
- •Электролиз
- •Законы электролиза
- •Применение электролиза
- •Высокомолекулярные соединения (вмс) или полимеры
- •Физические свойства
- •Классификация
- •Полимеризационные полимеры
- •Поликонденсационные полимеры
- •Применение
- •Олигомеры
Растворимость различных веществ в воде
Способность данного вещества растворяться в данном растворителе называется растворимостью.
С количественной стороны растворимость твердого вещества характеризует коэффициент растворимости или просто растворимость - это максимальное количество вещества, которое способно раствориться в 100 г или 1000 г воды при данных условиях с образованием насыщенного раствора.
Так как большинство твердых веществ при растворении в воде поглощают энергию, то в соответствии с принципом Ле-Шателье, растворимость многих твердых веществ увеличивается с повышением температуры.
Растворимость газов в жидкости характеризует коэффициент абсорбции - максимальный объем газа, который может раствориться при н.у. в одном объеме растворителя. При растворении газов выделяется тепло, поэтому с повышением температуры растворимость их понижается (например, растворимость NH3 при 0°С равна 1100 дм3/1 дм3 воды, а при 25°С - 700 дм3/1 дм3 воды). Зависимость растворимости газов от давления подчиняется закону Генри: масса растворенного газа при неизменной температуре прямо пропорциональна давлению.
Выражение количественного состава растворов
Наряду с температурой и давлением основным параметром состояния раствора является концентрация в нем растворенного вещества.
Концентрацией раствора называется содержание растворенного вещества в определенной массе или в определенном объеме раствора или растворителя. Концентрацию раствора можно выражать по-разному. В химической практике наиболее употребительны следующие способы выражения концентраций:
а) массовая доля растворенного вещества показывает число граммов (единиц массы) растворенного вещества, содержащееся в 100 г (единиц массы) раствора (ω, %)
ω
(%) =
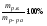
б) мольно-объемная концентрация, или молярность, показывает число молей (количество) растворенного вещества, содержащихся в 1 дм3 раствора (с или М, моль/дм3)

в) эквивалентная концентрация, или нормальность, показывает число эквивалентов растворенного вещества, содержащихся в 1 дм3 раствора (сэ или н, моль/дм3)

г) мольно-массовая концентрация, или моляльность, показывает число молей растворенного вещества, содержащихся в 1000 г растворителя (сm, моль / 1000 г)
 ;
;
д) титром раствора называется число граммов растворенного вещества в 1 см3 раствора (Т, г/см3)
T = mр.в./V.
Кроме того состав раствора выражается через безразмерные относительные величины -доли. Объемная доля - отношение объема растворенного вещества к объему раствора; массовая доля - отношение массы растворенного вещества к объему раствора; мольная доля отношение количества растворенного вещества (число молей) к суммарному количеству всех компонентов раствора. Наиболее употребительной величиной является мольная доля (N) – отношение количества растворенного вещества (ν1) к суммарному количеству всех компонентов раствора, то есть ν1 + ν2 (где ν2 –количество растворителя)
Nр.в. = ν1/( ν1 + ν2) = mр.в./Мр.в./( mр.в./Мр.в + mр-ля./Мр-ля).
Разбавленные растворы неэлектролитов и их свойства
При образовании растворов характер взаимодействия компонентов определяется их химической природой, что затрудняет выявление общих закономерностей. Поэтому удобно прибегнуть к некоторой идеализированной модели раствора, так называемому идеальному раствору. Раствор, образование которого не связано с изменением объема и тепловым эффектом, называют идеальным раствором. Однако, большинство растворов не обладает в полной мере свойствами идеальности и общие закономерности могут быть описаны на примерах так называемых разбавленных растворов, то есть растворов, в которых содержание растворенного вещества очень мало по сравнению с содержанием растворителя и взаимодействием молекул растворенного вещества с растворителем можно пренебречь. Растворы обладают коллигативными свойствами — это свойства растворов, зависящие от числа частиц растворенного вещества. К коллигативным свойствам растворов относят:
осмотическое давление;
давление насыщенного пара. Закон Рауля;
повышение температуры кипения;
понижение температуры замерзания.
Осмос. Осмотическое давление.
Пусть имеется сосуд, разделенный полупроницаемой перегородкой (пунктир на рисунке) на две части, заполненные до одинакового уровня О-О. В левой части помещается растворитель, в правой - раствор
0
I
IIII
0I

растворитель раствор
К понятию явления осмоса
Вследствие различия концентраций растворителя по обе стороны перегородки растворитель самопроизвольно (в соответствии с принципом Ле-Шателье) проникает через полупроницаемую перегородку в раствор, разбавляя его. Движущей силой преимущественной диффузии растворителя в раствор является разность свободных энергий чистого растворителя и растворителя в растворе. При разбавлении раствора за счет самопроизвольной диффузии растворителя объем раствора увеличивается и уровень перемещается из положения О в положение II. Односторонняя диффузия определенного сорта частиц в растворе через полупроницаемую перегородку называется осмосом.
Количественно охарактеризовать осмотические свойства раствора (по отношению к чистому растворителю) можно, введя понятие об осмотическом давлении. Последнее представляет собой меру стремления растворителя к переходу сквозь полупроницаемую перегородку в данный раствор. Оно равно тому дополнительному давлению, которое необходимо приложить к раствору, чтобы осмос прекратился (действие давления сводится к увеличению выхода молекул растворителя из раствора).
Растворы, характеризующиеся одинаковым осмотическим давлением, называются изотоническими. В биологии растворы с осмотическим давлением, большим, чем у внутриклеточного содержимого, называются гипертоническими, с меньшим – гипотоническими. Один и тот же раствор для одного типа клеток гипертонический, для другого – изотонический, для третьего – гипотонический.
Свойствами полупроницаемости обладает большинство тканей организмов. Поэтому осмотические явления имеют громадное значение для жизнедеятельности животных и растительных организмов. Процессы усвоения пищи, обмена веществ и т.д. тесно связаны с различной проницаемостью тканей для воды и тех или иных растворенных веществ. Явления осмоса объясняют некоторые вопросы, связанные с отношением организма к среде. Например, ими обусловлено то, что пресноводные рыбы не могут жить в морской воде, а морские в речной.
Вант-Гофф показал, что осмотическое давление в растворе неэлектролита пропорционально молярной концентрации растворенного вещества
Росм= сRТ,
где Росм - осмотическое давление, кПа; с - молярная концентрация, моль/дм3; R - газовая постоянная, равная 8,314 Дж/моль∙К; Т - температура, К.
Это выражение по форме аналогично уравнению Менделеева-Клапейрона для идеальных газов, однако эти уравнения описывают разные процессы. Осмотическое давление возникает в растворе при проникновении в него дополнительного количества растворителя через полупроницаемую перегородку. Это давление - сила, препятствующая дальнейшему выравниванию концентраций.
Вант-Гофф сформулировал закон осмотического давления: осмотическое давление равно тому давлению, которое производило бы растворенное вещество, если бы оно в виде идеального газа занимало тот же объем, который занимает раствор, при той же температуре.
Давление насыщенного пара. Закон Рауля.
Рассмотрим разбавленный раствор нелетучего (твердого) вещества А в летучем жидком растворителе В. При этом общее давление насыщенного пара над раствором определяется парциальным давлением пара растворителя, поскольку давлением пара растворенного вещества можно пренебречь.
Рауль показал, что давление насыщенного пара растворителя над раствором Р меньше, чем над чистым растворителем Р°. Разность Р° - Р = Р называется абсолютным понижением давления пара над раствором. Эта величина, отнесенная к давлению пара чистого растворителя, то есть (Р°-Р)/Р° =Р/Р°, называется относительным понижением давления пара.
Согласно закону Рауля, относительное понижение давления насыщенного пара растворителя над раствором равно молярной доле растворенного нелетучего вещества
(Р°-Р)/Р° = N = ν1/( ν1 + ν2) = mр.в./Мр.в./( mр.в./Мр.в + mр-ля./Мр-ля) = XA
где XA - мольная доля растворенного вещества. А так как ν1= mр.в./Мр.в, то используя этот закон можно определить мольную массу растворенного вещества.
Следствие закона Рауля. Понижение давления пара над раствором нелетучего вещества, например в воде, можно пояснить с привлечением принципа смещения равновесия Ле-Шателье. Действительно, при увеличении концентрации нелетучего компонента в растворе равновесие в системе вода - насыщенный пар сдвигается в сторону конденсации части пара (реакция системы на уменьшение концентрации воды при растворении вещества), что и вызывает уменьшение давления пара.
Понижение давления пара над раствором по сравнению с чистым растворителем вызывает повышение температуры кипения и понижение температуры замерзания растворов по сравнению с чистым растворителем (t). Эти величины пропорциональны моляльной концентрации растворенного вещества - неэлектролита, то есть:
t = К∙ст = К∙т∙1000/М∙а,
где сm- моляльная концентрация раствора; а - масса растворителя. Коэффициент пропорциональности К, в случае повышения температуры кипения, называется эбуллиоскопической константой для данного растворителя (Е), а для понижения температуры замерзания - криоскопической константой (К). Эти константы, численно различные для одного и того же растворителя, характеризуют повышение температуры кипения и понижение температуры замерзания одномоляльного раствора, т.е. при растворении 1 моль нелетучего неэлектролита в 1000 г растворителя. Поэтому их часто называют моляльным повышением температуры кипения и моляльным понижением температуры замерзания раствора.
Крископическая и эбуллиоскопическая постоянные не зависят от концентрации и природы растворенного вещества, а зависят лишь от природы растворителя и характеризуются размерностью кг∙град/моль.
