
- •Основные законы химии
- •Моль. Молярная масса
- •Относительная атомная и молекулярная массы
- •Газовые законы
- •1. Закон о суммарном давлении смеси газов: давление смеси химически не взаимодействующих идеальных газов равно сумме парциальных давлений газов, составляющих смесь
- •Закон эквивалентов
- •Периодический закон и периодическая система химических элементов д. И. Менделеева
- •Строение атома
- •Модели Томсона и Резерфорда
- •Закон Мозли
- •Электронная оболочка атомов по Бору
- •Представления квантовой механики
- •Современная модель состояния электрона в атоме
- •Строение электронных оболочек атомов
- •Способы записи электронных конфигураций атомов и ионов
- •Периодический закон и периодическая система элементов д.И. Менделеева в свете учения о строении атомов
- •Свойства атомов. Их периодичность
- •Химическая связь и строение молекул
- •Ковалентная связь
- •Метод валентных связей
- •Сигма () и пи ()-связи
- •Донорно-акцепторная связь
- •Свойства ковалентной связи
- •Полярные и неполярные молекулы
- •Относительная электроотрицательность атомов
- •Ионная связь
- •Гибридизация атомных орбиталей
- •Гибридизация орбиталей и пространственная конфигурация молекул
- •Металлическая связь
- •Водородная связь
- •Типы кристаллических решеток
- •Валентность
- •Степень окисления
- •Комплексные соединения (комплементарность) Структура комплексных соединений
- •Хелаты и внутрикомплексные соединения
- •Реакции образования комплексных соединений
- •Номенклатура комплексных соединений
- •Пространственное строение и изомерия комплексных соединений
- •Диссоциация комплексных соединений в растворах. Константа нестойкости. Константа устойчивости
- •Связь в комплексных ионах
- •Реакции с участием комплексных соединений
- •1) Реакции обмена
- •2) Окислительно-восстановительные реакции
- •Элементы химической термодинамики Основные понятия
- •Внутренняя энергия. Первый закон термодинамики. Энтальпия
- •Закон Гесса. Следствия из него
- •Второй закон термодинамики. Энтропия
- •Термодинамические потенциалы
- •14 Типы реакций, различающиеся возможностьюи условиями протекания в зависимости от характера изменения ∆н и ∆s
- •Химическая кинетика Основные понятия
- •Скорость химической реакции
- •Зависимость скорости реакции от концентрации реагентов
- •Влияние температуры на скорость реакции
- •Дисперсные системы
- •Классификация дисперсных систем
- •Классификация дисперсных систем
- •Классификация дисперсных систем по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •Количественные характеристики дисперсных систем
- •Устойчивость дисперсных систем
- •Применение
- •Растворы Растворы в природе. Теории растворов
- •Механизм процесса растворения
- •Тепловые эффекты при растворении
- •Ненасыщенные, насыщенные и пересыщенные растворы
- •Растворимость различных веществ в воде
- •Выражение количественного состава растворов
- •Разбавленные растворы неэлектролитов и их свойства
- •Эбуллиоскопическая и криоскопическая константы
- •Растворы электролитов и их свойства
- •Диссоциация воды. Водородный показатель
- •Гидролиз солей
- •Буферные растворы
- •Водородный показатель (рН) растворов
- •Свойства кислотно-основных индикаторов
- •Применение
- •Окислительно-восстановительные реакции
- •Распространенные окислители и их продукты
- •Важнейшие восстановители и окислители
- •Методы составления уравнений окислительно-восстановительных реакций
- •Влияние среды на протекание окислительно-восстановительных реакций
- •Эквивалентные массы окислителя и восстановителя
- •Классификация окислительно-восстановительных реакций
- •4) Особые случаи овр:
- •Электрохимические системы Общая характеристика
- •Электродный потенциал. Измерение электродных потенциалов
- •Ряд стандартных электродных потенциалов (напряжений). Уравнение Нернста
- •Ряд напряжений металлов
- •Гальванические элементы, их электродвижущая сила
- •Аккумуляторы
- •Характеристики аккумулятора Эдисона и свинцового аккумулятора
- •Топливные элементы
- •Электролиз
- •Законы электролиза
- •Применение электролиза
- •Высокомолекулярные соединения (вмс) или полимеры
- •Физические свойства
- •Классификация
- •Полимеризационные полимеры
- •Поликонденсационные полимеры
- •Применение
- •Олигомеры
Хелаты и внутрикомплексные соединения
Лиганды, занимающие в координационной сфере одно место, называются монодентатными. Лиганды, занимающие в координационной сфере два или несколько мест, называются би- и полидентатными. Примерами монодентатных лиганд является NH3, полидентатные комплексные соединения образуют органические реагенты с металлами. К полидентатным соединениям относятся так называемые хелаты циклические или клешнеобразные соединения, в которых центральный атом и полидентатный лиганд образуют цикл. Комплексообразователь при этом оказывается как бы втянутым внутрь лиганда, охвачен связями наподобие клешней рака. Отсюда и происходит название хелат («клешни рака»). Как правило, хелаты лучше растворимы в органических растворителях, чем в воде и более устойчивы по сравнению с комплексами тех же металлов с монодентатными лигандами. Различают обыкновенные хелаты, в которых связи или только парноэлектронные, или только донорно-акцепторного типа. Например, комплексы Fe3+ со щавелевой кислотой; Сu2+ c этилендиамином


натрия триоксалатоферрат(III) этилендиаминмедь(II) хлорид
Наличие в хелатах циклических группировок сильно увеличивает их устойчивость по сравнению с соединениями подобного состава, но не имеющими циклов. Такое повышение устойчивости называется хелатным эффектом. Известны хелаты, которые не разлагаются даже при 500 оС. Разновидность хелатов – внутрикомплексные соединения – это такие хелаты, в которых один и тот же лиганд связан с комплексообразователем как обычной, так и координативной связью. К внутрикомплексным соединениям относятся, например, гликолят меди. В реакции гидроксида меди с аминоуксусной кислотой (глицин) образуется нейтральный комплекс
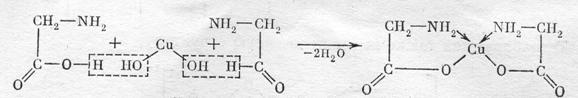
Каждая молекула глицина использует обе функциональные группы. В одном случае она связывается с центральным атомом через азот аминогруппы по донорно-акцепторному механизму, а во втором – через кислород карбоксильной группы обычной ковалентной связью.
Первым внутрикомплексным соединением, нашедшим применение в химии, был диметилглиоксимат никеля, открытый Л.А. Чугаевым в 1905 г. Это соединение не растворимо в воде и обладает ярко-красным цветом. Реакция с диметилглиоксиматом очень чувствительна и с успехом применяется для количественного определения никеля

В диметилглиоксимате имеется четыре цикла: два пятичленных и два шестичленных. Образование последних обусловлено водородной связью.
В последние годы широкое применение нашли внутрикомплексные соединения на основе этилендиаминтетрауксусной кислоты (ЭДТА) и других аминополикарбоновых кислот и их натриевые соли, называемые комплексонами. Они образуют весьма прочные комплексные соединения с большинством катионов (Ca2+, Mg2+, Pb2+, Zn2+, Cd2+ и т.д.). С ионами тяжелых металлов комплексоны образуют устойчивые комплексные соединения, которые не обладают вредным действием, присущим ионам металлов, что позволяет использовать трилон Б как антидот в химической промышленности при отравлениях тяжелыми металлами.
Метод анализа с использованием комплексонов (ЭДТА и трилона Б) – комплексонометрия используется в аналитической химии для определения жесткости воды, содержания металлов в различных материалах.
