
- •Глава 3 местные и общие реакции организма на повреждение
- •Часть I, общая нозология
- •Глава 3 / местные и общие реакции организма на повреждение67
- •Часть I. Общая нозология
- •Глава 3 / местные и общие реакции организма на повреждение
- •Часть I. Общая нозология
- •Глава 3 / местные и общие реакции организма на повреждение71
- •Часть I. Общая нозология
- •Глава 3 / местные и общие реакции организма на повреждение
- •Часть I. Общая нозология
- •Глава 3 / местные и общие реакции организма на повреждение
- •Часть I. Общая нозология
- •Глава 3 / местные и общие реакции организма на повреждение
- •Часть I. Общая нозология
- •Глава 3 / местные и общие реакции организма на повреждение
- •Часть I. Общая нозология
- •Глава 3 / местные и общие реакции организма на повреждение 6 Змсп № 532 пероксид ('00 ) и монооксид азота (n0) также выполняют полезные для организма функции.
- •Часть I. Общая нозология
- •Часть I. Общая нозология
- •Глава 3 / местные и общие реакции организма на повреждение
- •Часть I. Общая нозология
- •Глава 3 / местные и общие реакции организма на повреждение
- •Часть I. Общая нозология
- •Глава 3 / местные и общие реакции организма на повреждение
- •3.2. Общие реакции организма на повреждение
- •3.2.1. Общий адаптационный синдром (стресс)
Часть I. Общая нозология
убихинона (QH
, гидрохинон-форма):
О = N - О - ОН -> О = N - О + ОН (радикал гидроксила)
Образование пероксинитрита и радикала гидроксила приводит к повреждению клеток. По-видимому, одна из функций супероксиддисму-тазы состоит в предотвращении образования пероксинитрита за счет удаления супероксида из зоны образования окиси азота.
Радикал коэнзима Q. Биологическое окисление субстратов клеточного дыхания, таких как глюкоза, пировиноградная и янтарная кислоты и другие, осуществляется, как известно, в два этапа. На первом этапе в цикле трикарбоновых кислот происходит последовательный отрыв атомов водорода от субстрата и образование восстановленных форм пиридиннуклеотидов НАДН и НАДФН. На втором этапе электроны от НАДН и НАДФН переносятся по так называемой дыхательной цепи на кислород. В состав дыхательной цепи входят флавопротеиды, комплексы негемового железа, убихинон и гемопротеиды (цитохромы a, b и с и цитохромоксидаза). Схема дыхательной цепи дана на рис. 11.
сн,
В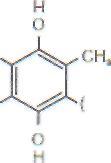 ажным
звеном цепи переноса электронов служит
убихинон (коэнзимQ)
:
ажным
звеном цепи переноса электронов служит
убихинон (коэнзимQ)
:
н,С-0
СН,-СН=С=СН,)„Н
Н,С-0
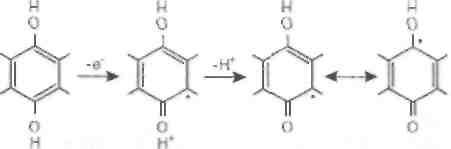
радикал которого (семихинон, QH на рис. 11) образуется либо при одноэлектронном окислении
гидрохинон катион-радикал нейтральный
гидрохинона радикал (семихинон)
либо при одноэлектронном восстановлении убихинона (Q на рис. 11):

|
о |
О |
О О |
|
хинон |
анион-радикал |
нейтральный |
|
|
хинона |
радикал (семихинон) |
В норме этот радикал является рядовым участником процесса переноса электронов, но при нарушении работы дыхательной цепи он может стать источником других, менее безобидных радикалов, в первую очередь радикалов кислорода.
Основные стадии цепного окисления. Реакция цепного окисления липидов играет исключительную роль в клеточной патологии. Она протекает в несколько стадий, которые получили название инициирование, продолжение, разветвление и обрыв цепи (см. схему 3).
Инициирование цепной реакции начинается с того, что в липидный слой мембран или ли-попротеинов внедряется свободный радикал.
митохондрий Глава 3 / МЕСТНЫЕ И ОБЩИЕ РЕАКЦИИ ОРГАНИЗМА НА ПОВРЕЖДЕНИЕ 83
Чаще всего это радикал гидроксила. Будучи небольшой по размеру незаряженной частицей, он способен проникать в толщу гидрофобного липидного слоя и вступать в химическое взаимодействие с полиненасыщенными жирными кислотами (которые принято обозначать как LH), входящими в состав биологических мембран и липопротеинов плазмы крови. При этом образуются липидные радикалы:
НО + LH -> Н20 + L Липидный радикал (L) вступает в реакцию с растворенным в среде молекулярным кислородом, при этом образуется новый свободный радикал - радикал липоперекиси (LOO ):
L + 02 -> LOO
Этот радикал атакует одну из соседних молекул фосфолипида с образованием гидроперекиси липида LOOH и нового радикала L':
LOO-+ LH -> LOOH + L-
Чередование двух последних реакций как раз и представляет собой цепную реакцию перекис-ного окисления липидов (см. схему 3).
Существенное ускорение пероксидации липидов наблюдается в присутствии небольших количеств ионов двухвалентного железа. В этом случае происходит разветвление цепей в результате взаимодействия Fe2i с гидроперекисями липидов:
Fe2+ + LOOH -> Fe3+ + НО + LO Образующиеся радикалы LO' инициируют новые цепи окисления липидов (см. схему 3): LO + LH -> LOH + L ;L + 02-> LOO -> и т.д.
В биологических мембранах цепи могут состоять из десятка и более звеньев. Но в конце концов цепь обрывается в результате взаимодействия свободных радикалов с антиоксидантами (InH), ионами металлов переменной валентности (например, теми же Fe2T) или друг с другом:
LOO + Fe2+ + Н+ -> LOOH + Fe3+
LOO + InH -> In ■+ LOOH
LOO' + LOO' -> молекулярные продукты
Последняя реакция особенно интересна, поскольку она сопровождается свечением (хеми-люминесценцией). Интенсивность этой хемилю-минесценции очень мала, поэтому ее иногда называют «сверхслабым свечением». Интенсивность свечения пропорциональна квадрату концентрации свободных радикалов в мембранах, а
Схема 3 Цепная реакция перекисного окисления липидов
скорость перекисного окисления прямо пропорциональна концентрации тех же радикалов. Поэтому интенсивность «сверхслабого» свечения однозначно отражает скорость липидной пероксидации в изучаемом биологическом материале и измерение хемилюминесценции довольно часто используется при изучении перекисного окисления липидов в различных объектах.
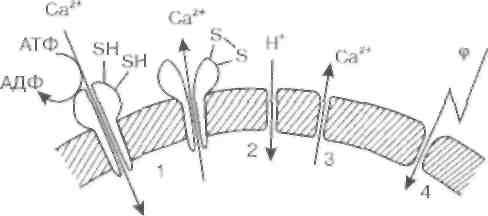
Рис. 12. Повреждающее действие перекисного окисления липидов на биологические мембраны
Повреждающее действие пероксидации липидов. На рис.12 показаны основные мишени перекисного окисления липидов в мембранных структурах клеток. Повреждаются либо белковые структуры, либо липидный бислой в целом. В последнее время ученые уделяют все большее внимание взаимодействию мембран с нуклеиновыми кислотами в ядре и митохондриях. По-видимому, одним из результатов пероксидации
84
