
- •Федеральное агентство по образованию рф
- •Введение
- •Литературный обзор
- •2.1 Исторический обзор
- •Пиразин. Общая характеристика
- •Нахождение в природе
- •2.4 Получение пиразинов
- •Строение пиразина и его производных
- •Химические свойства пиразина.
- •Электрофильное Замещение
- •Нуклеофильное замещение
- •Реакция с радикалами.
- •Металлирование галогендиазинов
- •Реакционноспособность заместителей боковой цепи
- •Окисление
- •Восстановление.
- •Производные пиразина
- •Аминопиразины.
- •Гидрированные пиразины.
- •Метилпиразины.
- •3. Обсуждение результатов
- •3.1 Синтез 1-[3-замещенных пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •3.1.1. Хлорирование 2-хлорпиразина сульфурилхлоридом
- •3.1.2. Синтез 2-хлор-3-(замещенных)пиразинов
- •3.1.3. Использование каталитической системы kf/Al2o3 для активации атома хлора в реакциях нуклеофильного замещения
- •Ямр 1н спектр 1-[3-(м-толилтио)пиразин-2-ил]-пиперидин-3-карбоновой кислоты
- •3.2. Амиды 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •3.2.1. Синтез карбамидных производных
- •3.2.2. Анализ спектров ямр 1н высокого разрешения амидов 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •3.2.3. Анализ спектров ямр 1н высокого разрешения амидов 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •Ямр1н спектр 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида
- •Ямр1н спектр 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида (ароматическая зона)
- •4. Экспериментальная часть
- •4.1.5. Методика получения 2-хлор-3-(замещенного)пиразина
- •4.1.6. Методика получения 1-[3-(замещенных)пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •4.2. Общая методика получения амидов 1-[3-(замещенных)пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •4.3. Физико-химические методы исследований
- •6. Список литературы
- •Приложение
- •Данные спектров 1н ямр производных 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоновой кислоты в дмсо-d6, δ (м. Д.), j (Гц)
- •В дмсо-d6, δ (м. Д.), j (Гц)
- •Физико-химические свойства исследуемых веществ
- •Физико-химические свойства исследуемых веществ
Восстановление.
Пиридазины и пиразины восстанавливаются только до гексагидропроизводных. При восстановлении натрием в кипящем этаноле пиридазины частично восстанавливаются дальше до диаминобутанов с разрывом связи N—N. Тетраметилпиразин в форме основания в отличие от хлоргидрата не восстанавливается действием Н2/Рt.
Схема 37
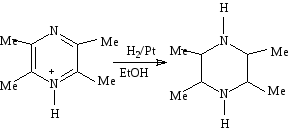
Пиразины легко восстанавливаются до насыщенных пиперазинов натрием в спирте, амальгамой алюминия, амальгамой натрия или оловом в соляной кислоте. С успехом применялись также методы каталитического гидрирования. При восстановлении 2,5-ди-фенилпиразина или его окси- или цианпроизводных йодистоводородной кислотой и красным фосфором получается 2,5-дифенил-3,6-дигидропиразин[22].
Схема 38
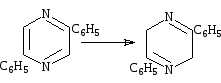
Производные пиразина
Аминопиразины.
Аминопиразины являются очень сильными основаниями. Аминопиразины можно диазотировать. Наилучшие результаты получаются, когда диазотирование проводится в водном растворе сильной кислоты или нитрозилсерной кислотой в концентрированной серной кислоте. Из диазониевых солей были получены только продукты гидролиза—оксипиразины. Известен один пример прямого гидролиза аминопиразина в оксипиразин, а именно превращение З-аминопиразиновой-2 кислоты в З-оксипиразиновую-2 кислоту при действии сильной щелочи при 170° . Возможно, что эта реакция включает в себя расщепление иминоструктуры.[30,49]
Аминопиразины и 2 – аминохиноксалины реагируют с азотистой кислотой в водной среде и дают 2- (1/f)pyrazinonesи 2 (1/f) –quinoxalinones. 2- аминохиноксалины гидролизуются лучше, чем типичные гетероциклические амины и 2- амино – 3 – метилхиноксалин. Например, подвергаются гидролизу при нагревании до 100°С с разбавленным гидроксидом натрия. Аминогруппа активизирует пиразин, хиноксалин, феназин к атаке электрофилов, обычно в орто- или пара – положение относительно аминогруппы. Таким образом бромирование 2 – аминопиразина в уксусной кислоте приводит к 2 – амино – 3,5 – дибромпиразину[23,50].
Схема 39
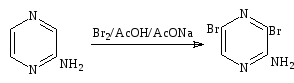
Гидрированные пиразины.
Некоторые дигидриды очень легко изомеризуются, так что убедительно доказать положение двойных связей часто невозможно. Дигидропиразины с двумя заместителями у одного и того же атома углерода вполне устойчивы к окислению, тогда как такие, в которых этот тип замещения отсутствует, легко превращаются в соответствующие пиразины. Это осуществляется нагреванием или воздействием воздуха при комнатной температуре. При кислом гидролизе дигидропиразины расщепляются по связям С = N. Однако на промежуточной стадии может происходить изомеризация, так что продукты гидролиза не обязательно будут те, которые можно предсказать на основании первоначальной структуры дигидропиразина[24].
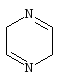
2,5-дигидропиразины.
38
2,5-Дигидропиразины являются, очевидно, первичными продуктами автоконденсации а-аминокетонов. Впервые они были исследованы Габриэлем, который получил в отсутствие килорода воздуха 3,6-дифенил-, 3,6-дифенил-2,5-диметил-, 3,6-диметил-2,5-дифенил- и 2,2,3,5,5,6-гексаметил-2,5-дигидропиразины.
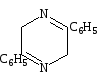
39
Обработка а,а-дихлорзамещенных третичных спиртов аммиаком приводит к образованию устойчивых дигидропиразинов.
Схема 40

Механизм, предложенный для этой реакции, включает самоконденсацию промежуточно образующего иминоспирта[25].
2,3-дигидропиразины.
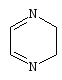
2,3-Дигидропиразины получаются конденсацией а,β-дикарбонильных соединений с а,β-диаминами. Если нагревать бензил с этилендиамином в спиртовом растворе, то с хорошим выходом получается 5,6-дифенил-2,3-дигидропиразин. Подобным же образом из бензила и замещенных этилендиаминов могут быть получены тризамещенные 2,3-дигидропиразины[50].
1,4-дигидрогшразины и 1,2-дигидропиразины.
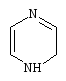
1,4 алкил – 1,4 дигидропиразины подвергаются изомеризации к 1,2 – дигидропиразинам[26].
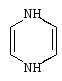
1,2 – дигидропиразины относительно устойчивы, хотя легко окисляются. Обычно образуются при взаимодействии металлоорганических реактивов с кольцом.
Галогенпиразины.
Бром- и хлорпиразины по своей реакционноспособности сравнимы с соответствующими а-галогенпиридинами. Например, бромпиразин дает положительную пробу на галоген со спиртовым раствором нитрата серебра, а хлорпиразин при действии концентрированного водного аммиака при 200° превращается в аминопиразин, а при действии сильной щелочи — в оксипиразин. Гомологи галогенпиразинов, по-видимому, несколько менее реакционноспособны, чем исходное соединение.
N-окиси пиразинов, подобно N-окиси пиридина, можно превратить в галогенированные основания. При действии хлорокиси фосфора моно-N-окиси и ди-N-окиси пиразина образуют соответственно монохлор- и дихлорпиразины. Непосредственное превращение 2-оксипиразинов в 2-хлорпиразины осуществляется при действии хлорокиси фосфора или ее смеси с пятихлористым фосфором[27].
