
- •Федеральное агентство по образованию рф
- •Введение
- •Литературный обзор
- •2.1 Исторический обзор
- •Пиразин. Общая характеристика
- •Нахождение в природе
- •2.4 Получение пиразинов
- •Строение пиразина и его производных
- •Химические свойства пиразина.
- •Электрофильное Замещение
- •Нуклеофильное замещение
- •Реакция с радикалами.
- •Металлирование галогендиазинов
- •Реакционноспособность заместителей боковой цепи
- •Окисление
- •Восстановление.
- •Производные пиразина
- •Аминопиразины.
- •Гидрированные пиразины.
- •Метилпиразины.
- •3. Обсуждение результатов
- •3.1 Синтез 1-[3-замещенных пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •3.1.1. Хлорирование 2-хлорпиразина сульфурилхлоридом
- •3.1.2. Синтез 2-хлор-3-(замещенных)пиразинов
- •3.1.3. Использование каталитической системы kf/Al2o3 для активации атома хлора в реакциях нуклеофильного замещения
- •Ямр 1н спектр 1-[3-(м-толилтио)пиразин-2-ил]-пиперидин-3-карбоновой кислоты
- •3.2. Амиды 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •3.2.1. Синтез карбамидных производных
- •3.2.2. Анализ спектров ямр 1н высокого разрешения амидов 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •3.2.3. Анализ спектров ямр 1н высокого разрешения амидов 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •Ямр1н спектр 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида
- •Ямр1н спектр 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида (ароматическая зона)
- •4. Экспериментальная часть
- •4.1.5. Методика получения 2-хлор-3-(замещенного)пиразина
- •4.1.6. Методика получения 1-[3-(замещенных)пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •4.2. Общая методика получения амидов 1-[3-(замещенных)пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •4.3. Физико-химические методы исследований
- •6. Список литературы
- •Приложение
- •Данные спектров 1н ямр производных 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоновой кислоты в дмсо-d6, δ (м. Д.), j (Гц)
- •В дмсо-d6, δ (м. Д.), j (Гц)
- •Физико-химические свойства исследуемых веществ
- •Физико-химические свойства исследуемых веществ
Введение
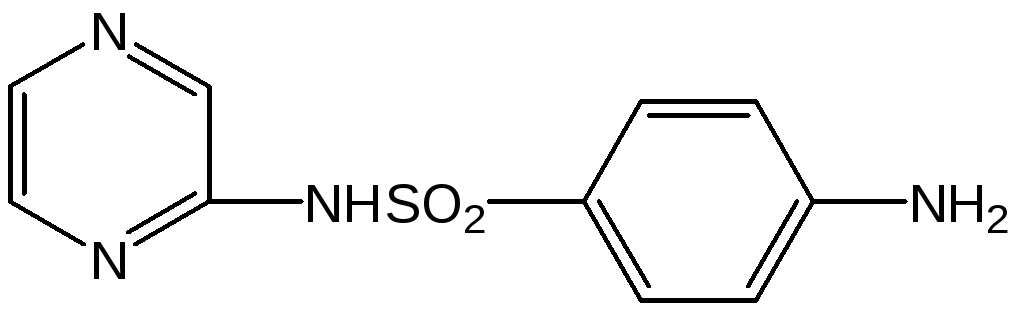
Одной из насущных задач органического синтеза является расширение арсенала доступных гетероциклических соединений, используемых в качестве субстратов для создания новых, более эффективных лекарственных препаратов. К числу таких производных относится пиразиновая структура, которая входит в состав ряда важных природных веществ, например рибофлавина, фолиевой кислоты и др. Производные пиразина и пиперазина нашли применение в качестве синтетических лекарственных средств, среди них бактериостатические препараты сульфапиразин[1] и сульфометопиразин[2], антигельминтное лекарство – дитразин, антигистаминный препарат – хлорциклизин[1], диуретик – амилорид[3], противотуберкулезный препарат – пиразинамид[4] и др. Еще более широкое применение в медицинской практике нашли производные пиперидина, которые давно используются в качестве препаратов нейротропного действия, средств, влияющих на сердечно-сосудистую систему, спазмолитиков, бронхолитиков, противоязвенных средств[5] и др.
Цель работы:синтез соединений, одновременно содержащих в своей структуре пиразиновый и пиперидиновый фрагменты
Задачи:
Разработка схемы синтеза амидных производных 1-[3-(замещенных)пиразин-2-ил]-пиперидин-3-карбоновых кислот;
Установление структуры синтезированных соединений методом ЯМР 1Н – спектроскопии;
Определение физико-химических свойств полученных веществ (Тпл., Rf, η).
Литературный обзор
2.1 Исторический обзор
Получение «амарона» Лаурентом [6] в 1844г. является первым зарегистрированным синтезом пиразина. Метод Л ау рента, однако, остался неясным, и лишь спустя более пятидесяти лет «амарон» был идентифицирован как тетрафенил-пиразин [7]. Тем временем этот ряд соединений систематически начали изучать Гуткнехт [8] и Трэдвелл [9] — ученики В. Мейера, которые нашли, что при восстановлении нитрозированных кетонов вместо ожидаемых α-аминокетонов образуются не содержащие кислорода основания. Теперь известно, что это превращение можно представить следующим образом:
Схема 1
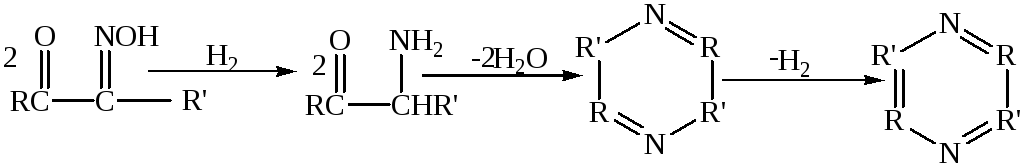
Правильная структура циклической системы продуктов реакции впервые была предложена Влюгелем [10]; синтез производных пиразина, проведенный другим методом [6], по-видимому, подтвердил эту структуру и позволил установить истинное положение заместителей. Наконец, осуществленное Вольфом [11] в 1893г. превращение тетраметилпиразина в пиперазин рядом реакций дало однозначное доказательство структуры пиразинов. Образование пиразина из α-аминокетона должно сопровождаться отщеплением водорода и воды. Габриэль и Пинкус [12] установили, что выходы получаются значительно более высокими, если окислитель добавляется к реакционной смеси после того, как закончилась конденсация. Габриэль доказал промежуточное образование дигидропиразинов выделением этих соединений в условиях отсутствия воздуха и последующим окислением их до соответствующих пиразинов.
Схема 2
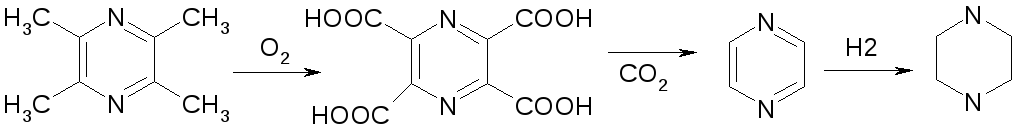
На основании молекулярных рефракций различных производных Брюль [13] установил, что структура пиразинового кольца скорее относится к типу структур Кекуле, чем к типу структур Дьюара.
Вследствие недостатка в природных источниках пиразина и его производных эти соединения прежде были сравнительно дорогостоящими. До последнего времени они не находили никакого важного применения, и после опубликования первых работ по химии пиразина этим соединениям уделялось мало внимания. Когда успехи химиотерапии открыли новые возможности применения этих малодоступных веществ, то снова возник интерес к пиразинам. Гидразиды пиразинмонокарбоновой кислоты были запатентованы в качестве укрепляющих средств [14], а то, что пиразинкарбоновые кислоты оказались эффективными при лечении пеллагры [15], показывает, что физиологическое действие некоторых пиразинов подобно действию соответствующих пиридинов. После открытия превосходных бактериостатических свойств сульфапиразина и некоторых его производных [16] началось широкое использование сульфамидных препаратов, которое привело также к общему оживлению в исследовании пиразинов.
1
