
- •Федеральное агентство по образованию рф
- •Введение
- •Литературный обзор
- •2.1 Исторический обзор
- •Пиразин. Общая характеристика
- •Нахождение в природе
- •2.4 Получение пиразинов
- •Строение пиразина и его производных
- •Химические свойства пиразина.
- •Электрофильное Замещение
- •Нуклеофильное замещение
- •Реакция с радикалами.
- •Металлирование галогендиазинов
- •Реакционноспособность заместителей боковой цепи
- •Окисление
- •Восстановление.
- •Производные пиразина
- •Аминопиразины.
- •Гидрированные пиразины.
- •Метилпиразины.
- •3. Обсуждение результатов
- •3.1 Синтез 1-[3-замещенных пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •3.1.1. Хлорирование 2-хлорпиразина сульфурилхлоридом
- •3.1.2. Синтез 2-хлор-3-(замещенных)пиразинов
- •3.1.3. Использование каталитической системы kf/Al2o3 для активации атома хлора в реакциях нуклеофильного замещения
- •Ямр 1н спектр 1-[3-(м-толилтио)пиразин-2-ил]-пиперидин-3-карбоновой кислоты
- •3.2. Амиды 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •3.2.1. Синтез карбамидных производных
- •3.2.2. Анализ спектров ямр 1н высокого разрешения амидов 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •3.2.3. Анализ спектров ямр 1н высокого разрешения амидов 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •Ямр1н спектр 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида
- •Ямр1н спектр 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида (ароматическая зона)
- •4. Экспериментальная часть
- •4.1.5. Методика получения 2-хлор-3-(замещенного)пиразина
- •4.1.6. Методика получения 1-[3-(замещенных)пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •4.2. Общая методика получения амидов 1-[3-(замещенных)пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •4.3. Физико-химические методы исследований
- •6. Список литературы
- •Приложение
- •Данные спектров 1н ямр производных 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоновой кислоты в дмсо-d6, δ (м. Д.), j (Гц)
- •В дмсо-d6, δ (м. Д.), j (Гц)
- •Физико-химические свойства исследуемых веществ
- •Физико-химические свойства исследуемых веществ
3.2.2. Анализ спектров ямр 1н высокого разрешения амидов 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот

Все полученные в работе карбоксамидные производные 5были выделены в индивидуальном виде и проанализированы с помощью ЯМР1Н спектроскопии. В качестве примера на рисунке 4 представлен спектр ЯМР1Н 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида.
В наиболее слабом поле при δ 8.41 м.д. проявляется триплетный сигнал амидной группы (3J = 5.6). При δ 7.97 и 7.86 м.д. наблюдаются два узких дублетных сигнала (3J= 2.7 Гц) незамещенных протонов пиразинового цикла. Пятиспиновая система протонов тиофенольной группы проявляется в виде мультиплета при δ = 7.46 и триплета (3J = 3.2) при δ = 7.43 м.д. 4 протона хлорбензильной группы не перекрываются протонами тиофенольной группы. Они дают триплетный сигнал при δ = 7.31 (1Н, Н5* ,3J=7,8), синглет при δ = 7.26 (1Н, Н2*), дуплетные сигналы при δ = 7,24 (1Н, Н4*,3J = 7,6), при δ = 7.20 (1Н, Н6*, 3J=7.6). Метиленовый фрагмент радикала проявляет дуплетный сигнал при при δ = 4.27 (3J=5.5).
Аксиальные и экваториальные протоны метиленовых групп пиперидинового цикла, преимущественно находящегося в конформации кресло, образуют группу хорошо разрешенных отдельных сигналов при δ = 3.73 м (He2”,6”), 2.94 т (Ha2”,3J= 11.7), 2.78 т (Ha6”, 3J= 11.6), 1,97 д (He4”,3J= 12.2) 1.71 м (Ha4”), 1.85 д (He5”,3J = 12.0), 1.65 м (Ha5”), метиновый протон при атоме С3 наблюдается в виде мультиплетного сигнала при δ 2.62 м.д..
Аналогичным образом были сделаны отнесения в спектрах ЯМР 1Н других соединений. Результаты приведены в таблице 1 (Приложение 1).
3.2.3. Анализ спектров ямр 1н высокого разрешения амидов 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот
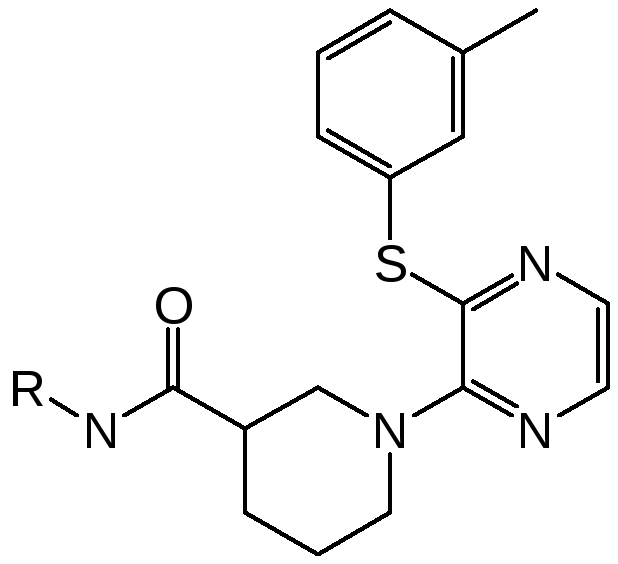
В качестве примера на рисунке 3 представлен спектр ЯМР 1Н 1-[3-(м-толлилтио)пиразин-2-ил]-пиперидин-3-карбоксо-N- 3 –хлор-бензиламида. В наиболее слабом поле при δ = 8,41 проявляется триплетный сигнал амидной группы (3J = 5.65). При δ 7.96 и 7.86 м.д. наблюдаются два узких дублетных сигнала (3J= 2.6 Гц) незамещенных протонов пиразинового цикла. Четырехспиновая система протонов тиофенольной группы проявляется в виде триплета при δ = 7,32 (3 J = 7,5), синглета при δ = 7.28, и двух дуплетов при δ = 7.26 ( 3J =9.0) и δ = 7.21 (3J =8.2) м.д.. 4 протона хлорбензильной группы перекрываются протонами тиофенольной группы. Они дают следующие мультиплетные сигналы при δ =7.32 (2Н, Н4*5*); 7,30 (1Н, Н2*), 7.20 (1Н, Н6*). Метиленовый фрагмент радикала проявляет дуплетный сигнал при δ =4.28 д (3J=5.7). Аксиальные и экваториальные протоны метиленовых групп пиперидинового цикла, преимущественно находящегося в конформациикресло, образуют группу хорошо разрешенных отдельных сигналов при δ = 3.76 т (He2”,6”, 3J = 10,05); 2.94 т (2Н,Ha2”,3J = 11.7), 2.78 т (1Н,Ha6”, 3J= 11.15), 2.00 д (1H,He4”,3J= 11.1), 1.71 м (1Н,Ha4”), 1.84 д (1H,He5”,3J= 12.4), 1.68 м (1Н,Ha5”), метиновый протон при атоме С3 наблюдается в виде мультиплетного сигнала при δ 2.62 м.д.. Протоны метильной группы дают синглет приδ2,35 м.д.
Аналогичным образом были сделаны отнесения в спектрах ЯМР 1Н других соединений. Результаты приведены в таблице 2 (Приложение 2).
