
- •Федеральное агентство по образованию рф
- •Введение
- •Литературный обзор
- •2.1 Исторический обзор
- •Пиразин. Общая характеристика
- •Нахождение в природе
- •2.4 Получение пиразинов
- •Строение пиразина и его производных
- •Химические свойства пиразина.
- •Электрофильное Замещение
- •Нуклеофильное замещение
- •Реакция с радикалами.
- •Металлирование галогендиазинов
- •Реакционноспособность заместителей боковой цепи
- •Окисление
- •Восстановление.
- •Производные пиразина
- •Аминопиразины.
- •Гидрированные пиразины.
- •Метилпиразины.
- •3. Обсуждение результатов
- •3.1 Синтез 1-[3-замещенных пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •3.1.1. Хлорирование 2-хлорпиразина сульфурилхлоридом
- •3.1.2. Синтез 2-хлор-3-(замещенных)пиразинов
- •3.1.3. Использование каталитической системы kf/Al2o3 для активации атома хлора в реакциях нуклеофильного замещения
- •Ямр 1н спектр 1-[3-(м-толилтио)пиразин-2-ил]-пиперидин-3-карбоновой кислоты
- •3.2. Амиды 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •3.2.1. Синтез карбамидных производных
- •3.2.2. Анализ спектров ямр 1н высокого разрешения амидов 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •3.2.3. Анализ спектров ямр 1н высокого разрешения амидов 1-[3-(замещенных) пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •Ямр1н спектр 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида
- •Ямр1н спектр 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида (ароматическая зона)
- •4. Экспериментальная часть
- •4.1.5. Методика получения 2-хлор-3-(замещенного)пиразина
- •4.1.6. Методика получения 1-[3-(замещенных)пиразин-2-ил]-пиперидин-3-карбоновых кислот
- •4.2. Общая методика получения амидов 1-[3-(замещенных)пиразин-2-ил]-пиперидин-3-карбоновых кислот.
- •4.3. Физико-химические методы исследований
- •6. Список литературы
- •Приложение
- •Данные спектров 1н ямр производных 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоновой кислоты в дмсо-d6, δ (м. Д.), j (Гц)
- •В дмсо-d6, δ (м. Д.), j (Гц)
- •Физико-химические свойства исследуемых веществ
- •Физико-химические свойства исследуемых веществ
Ямр1н спектр 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида
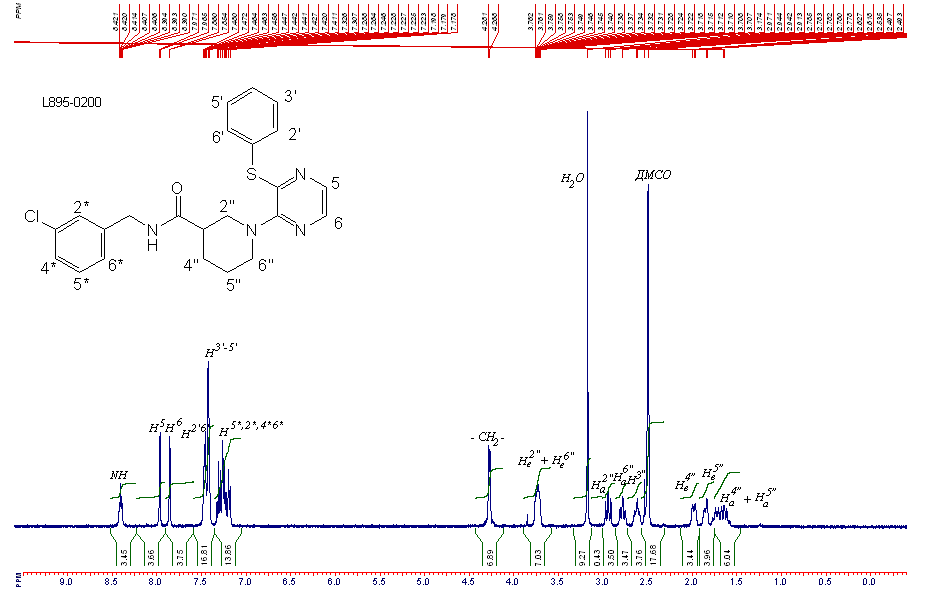
Ямр1н спектр 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида (ароматическая зона)
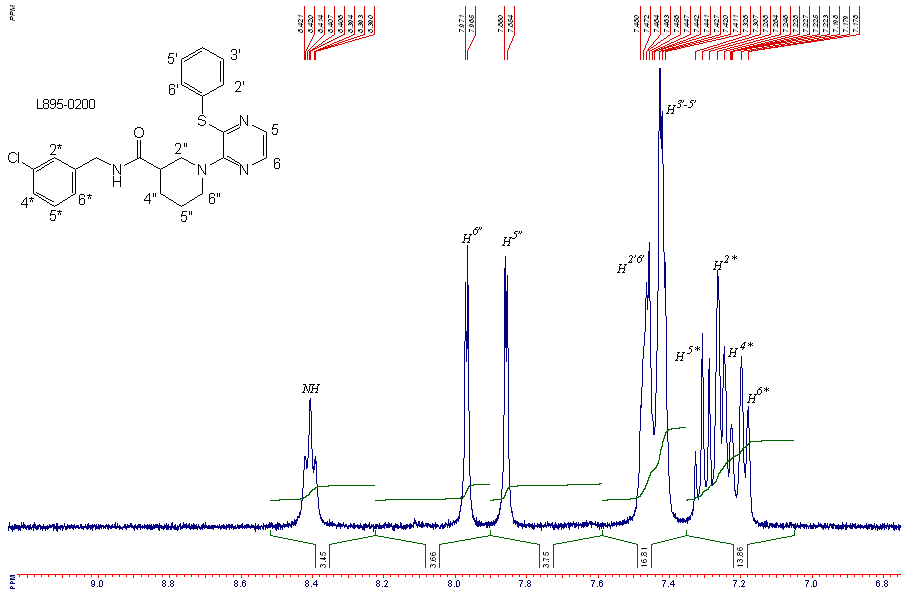
ЯМР1Н спектр 1-[3-(фенилтио)пиразин-2-ил]-пиперидин-3-карбоксо-3-хлор-бензиламида(алифатическая зона)

Рис. 3 ЯМР1Н спектр 1Н 1-[3-(м-толлилтио)пиразин-2-ил]-пиперидин-3-карбоксо- N - 3 –хлор-бензиламида.

Р ис.4
ЯМР1Н
спектр 1Н
1-[3-(м-толлилтио)пиразин-2-ил]-пиперидин-3-карбоксо-
N - 3 –хлор-бензиламида
(ароматическая зона).
ис.4
ЯМР1Н
спектр 1Н
1-[3-(м-толлилтио)пиразин-2-ил]-пиперидин-3-карбоксо-
N - 3 –хлор-бензиламида
(ароматическая зона).
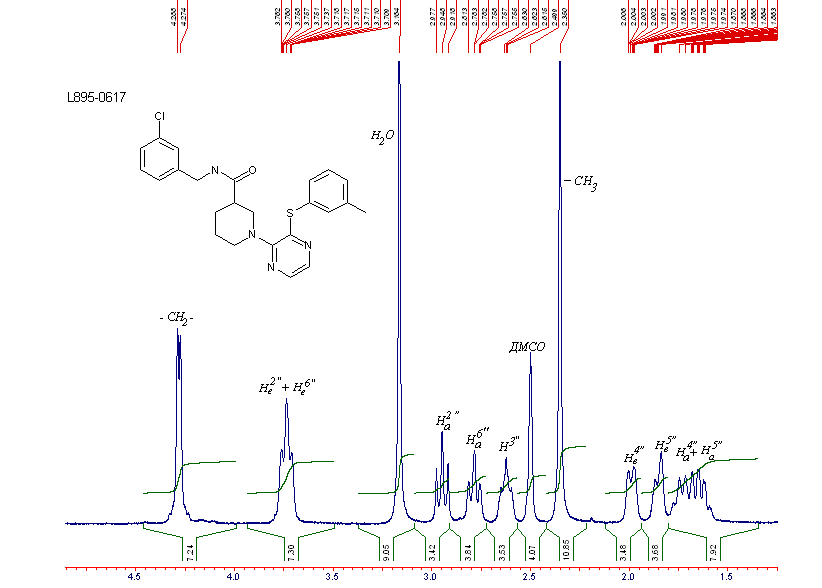
Рис. 5 ЯМР1Н спектр 1Н 1-[3-(м-толлилтио)пиразин-2-ил]-пиперидин-3-карбоксо- N - 3 –хлор-бензиламида (алифатическая зона).
4. Экспериментальная часть
4.1. Синтез исходных соединений и подготовка растворителей
4.1.1. Синтез и очистка исходных хлорпиразинов
В качестве субстрата для синтеза амидов1-[3-(замещенной)пиразин-2-ил]-пиперидин-3-карбоновой кислоты использовался товарный хлорпиразин Т.кип. 153-1540С.
4.1.2. Подготовка реагентов и растворителей
Амины использовались в виде готовых реагентов - солей (гидрохлоридов, гидробромидов) или свободных оснований.
Растворители очищали и абсолютировали по известным методикам [38]. Их чистоту контролировали по температуре кипения и показателю преломления на рефрактометре ИРФ-22.
4.1.3. Синтез катализатора KF/Al2O3
Для приготовления катализатора брали по массе 37 % сухой фторид калия и 63 % оксида алюминия. Тщательно перемешивали, добавляли воду, образуя суспензию. После чего воду выпаривали при нагревании до получения сухого KF/Al2O3.
4.1.4. Синтез 2,3-дихлорпиразина
К перемешиваемому раствору 2-хлорпиразина (29.7 г, 0.25 моль) в 30 мл ДМФА прибавляли по каплям при 70С сульфурилхлорид (73.0 г, 0.54 моль), избегая разогрева выше 75С. После прибавления всего SO2Cl2 смесь перемешивали 2 часа, охлаждали до комнатной температуры, осторожно прибавляли 100 мл воды (разогрев, бурное выделение газа). Затем рН раствора доводили до 7 сначала 50 %-ным раствором NaOH, потом 10%-ным NaHCO3. Целевой продукт извлекали из реакционной смеси перегонкой с водяным паром. После охлаждения отгона до 5 С, выпавший осадок отфильтровывали. Выход продукта 83%. Т.пл. 23-24°С. Спектр ЯМР 1Н, , м.д.: 8.56 с (2Н, Н5,6).
4.1.5. Методика получения 2-хлор-3-(замещенного)пиразина
К 0.1 моль 2,3-дихлорпиразина 2, 0.11 мольKOH, 0.01 моль тетрабутиламмоний бромида в 100 мл воды и 100 мл бензола добавляли 0.1 моль м-толилтиофенола (тиофенола). Полученную смесь перемешивали в течении 4 час при температуре 60-70 °С. Органический слой отделяли, сушили над безводнымNa2SO4, растворитель отгоняли в вакууме. Остаток промывали пропанолом-2 и высушивали. Выход 82%. Т. пл. 116-118С.Rf0.93 (CCl4-EtOH3:1). Спектр ЯМР1Н,, м.д. (J, Гц): 8.27 д (1Н, Н5,3J= 2.6), 8.15 д (1Н, Н6,3J= 2.6), 7.29 д (2Н, Н5,6,3J= 3,55), 7.26 с (1Н, Н2), 7.23 м (1Н, Н4’), 2.35 с (3H,CH3).
