
• Болезнь Педжета. Склонная к увеличению экзематозная поверхность, покрытая чешуйками и корочками. При гистологическом исследовании в эпителии выявляют клетки Педжета.
При поражении кожи полового члена возможно излечение.
При инфильтрации пещеристого тела или наличии остаточной опухоли прибегают в дальнейшем к контактному аппликационному облучению. Суммарная доза - 30 Гр.
В случае инфильтрации пещеристых тел при проведении сочетанной лучевой терапии суммарную дозу наружного облучения снижают до 50 Гр и затем контактно подводят не менее 30 Гр.
Если после проведения наружного облучения сохраняются небольшие остаточные опухоли кожи полового члена, лечение рекомендуют завершить фотодинамическим воздействием.
У больных с обширными поражениями и глубокой инфильтрацией пещеристых тел прибегают к предоперационному дистанционному облучению в дозе 40-50 Гр только в случае сомнений в радикальности оперативного лечения.
При проведении самостоятельного лучевого лечения и отсутствии клинических признаков опухолевого поражения паховых лимфатических узлов их подвергают облучению из отдельных полей с помощью электронных пучков или включают в единое поле с первичным очагом при дистанционной гамма-терапии. Доза облучения должна составлять не менее 60 Гр. Такая тактика оправданна, если пациент может находиться под строгим динамическим наблюдением, так как развитие микрометастазов возможно и после подведения указанной дозы. В противном случае выполняют превентивную пахово-бедренную лимфаденэктомию.
При наличии регионарных метастазов более эффективно применение комбинированного лечения - предоперационного облучения с последующей лимфаденэктомией. В этих случаях необходимо подведение СОД 40 Гр.
Медикаментозное лечение
Химиотерапия рака полового члена показана при наличии метастазов. Решение о проведении этого метода лечения принимают с учетом возраста, физического состояния, наличия обусловленной заболеванием симптоматики и предпочтений больного. Схемы полихимиотерапии • 1-я линия химиотерапии. Цисплатин 100 мг/м2 в 1-й день с гипергидратацией, фто-рурацил 1000 мг/м2 (внутривенно в виде непрерывной 96-часовой инфузии); интервал межу курсами 3 нед.
Цисплатин 75 мг/м2 в 1-й день с гипергидратацией, метотрексат 25 мг/м2 в 1-й и 8-й дни, блеомицин 15 мг внутримышечно № 5-7; интервал между введением цисплатина 3 нед.
Данная книга в списке рекомендаций к покупке и прочтению форума сайта https://meduniver.com/
Метотрексат 30 мг/м2 в 1-й и 8-й дни, доксорубицин 50 мг/м2 во 2-й и 9-й дни, блеомицин 15 мг внутримышечно № 5-7 через день.
• 2-я линия химиотерапии: можно использовать комбинацию GC.
Цисплатин 70-100 мг/м2 в 1-й день с гипергидратацией, гемцитабин 1250 мг/м2в 1-й и 8-й дни.
Оксалиплатин 130 мг/м2 в 1-й день, гемцитабин 1250 мг/м2 в 1-й и 8-й дни.
Интервал между курсами 3 нед. При проведении 2-й линии терапии или невозможности проведения гипергидратации циспла-тин можно заменить на карбоплатин или оксалиплатин.
Хирургическое лечение
Хирургическое лечение больных раком полового члена включает удаление первичного опухолевого очага и регионарных лимфатических узлов.
Виды хирургического вмешательства
•Иссечение крайней плоти полового члена (цирку-мизация). Выполняют только при начальном раке соответствующей локализации. В отдельных случаях операция необходима на диагностическом этапе, особенно при сопутствующем фимозе или парафимозе.
•Ампутация полового члена. При раке Tis, Ta, T1-2N0-3M0-1 c локализацией опухоли на головке и в дистальных отделах тела органа.
•Скальпирование полового члена. Показано при раке Tis-1N0M0 и интактной головке.
•Эмаскуляция. Выполняется при раке Т2-4N0-3М0-1 с локализацией опухоли в проксимальных отделах тела полового члена.
•Ампутация полового члена на уровне лонного сочленения с промежностной уретропластикой. Необходима при местнораспространенном раке (T2-3N0-3M0) с преимущественной локализацией в проксимальных отделах.
•Подвздошная, пахово-бедренная лимфаденэктомия. Показана при раке полового члена T1-4N1-3M0. В ходе данной операции удаляют единым блоком: поверхностные паховые лимфатические узлы и окружающую клетчатку с участком прилежащей поверхностной фасции бедра и резекцией участка большой подкожной вены бедра, глубокие паховые лимфатические узлы с окружающей клетчаткой по ходу бедренной артерии и вены, лимфатические узлы, расположенные по ходу наружной подвздошной артерии и вены до уровня развилки общей подвздошной артерии, лимфатические узлы, расположенные по ходу внутренней подвздошной артерии и вены, а также обтураторные лимфатические узлы.
• Пахово-бедренная и модифицированная паховая лим-фаденэктомия, ограниченная поверхностными и глубокими паховыми лимфатическими узлами с сохранением большой подкожной вены бедра. Показана при отсутствии метастазов в паховых лимфатических узлах, но при высоком риске их развития (умеренная или низкая степень дифференцировки опухоли, сосудистая или лимфатическая инвазия в новообразование или инфильтративный рост рака).
Оценка эффективности лечения
Проводится с учетом данных:
•визуального осмотра;
•биопсии зоны рубца;
•УЗИ культи полового члена, паховых зон, малого таза и брюшной полости;
•исследования опухолевого маркёра SCC;
•КТ или МРТ малого таза, паховых зон и зон отдаленного метастазирования;
•сканирования костей;
•рентгенографии органов грудной клетки.
Сроки наблюдения: 1-й год - 1 раз в 3 мес, 2-3-й годы - 1 раз в 6 мес.
Примерные сроки нетрудоспособности
•После ампутации полового члена - 7-12 дней.
•После эмаскуляции и скальпирования полового члена, а также после ампутации полового члена с промежностной уретропластикой - 15-20 дней.
•После подвздошной или пахово-бедренной лимфаденэкто-мии - 20-25 дней.
•После химиоили лучевой терапии - 7-10 дней.
Прогноз
Прогноз при раке полового члена относительно неблагоприятный: пятилетняя выживаемость при любых стадиях составляет около 52%. При отсутствии метастазов она достигает 90%. При появлении отдаленных метастазов пятилетняя выживаемость отсутствует.
Краткие рекомендации пациентам
Мужчина должен соблюдать правила личной гигиены и не заниматься самолечением воспалительных заболеваний полового члена. При длительном хроническом воспалении в области головки необходима консультация уролога для своевременного проведения хирургического вмешательства.

Данная книга в списке рекомендаций к покупке и прочтению форума сайта https://meduniver.com/
Глава 18. Опухоли женских половых органов
18.1. РАК ЯИЧНИКОВ И НЕЭПИТЕЛИАЛЬНЫЕ ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ ЯИЧНИКОВ
Код по МКБ-10
С56. Злокачественное новообразование яичника.
Эпидемиология
Злокачественные опухоли яичников в онкологической заболеваемости женского населения Российской Федерации занимают стабильно 7-е место (4,7%). Среди новообразований органов репродуктивной системы на долю злокачественных опухолей яичников приходится около 13,8%. Заболеваемость в России составляет 17,17 на 100 000, смертность - 10,25 на 100 000 женщин в год. Злокачественные опухоли яичников встречаются у женщин всех возрастных групп, с младенчества. Пик заболеваемости раком яичников приходится на 7-ю декаду жизни, для женщин в возрасте 60-64 лет заболеваемость составляет 41,15 на 100 000 человек в год. В то же время пик заболеваемости неэпителиальными опухолями яичников приходится на 3-4-ю декаду жизни. Стандартизованный показатель колеблется от 6,0 до 10,5 на 100 000 женского населения (в зависимости от региона).
В структуре умерших от злокачественных новообразований рак яичников стоит на 6-м месте (5,8%). У женщин в возрасте 40-49 лет опухоли этой локализации занимают 3-е место (9,2%) в структуре основных причин смерти после рака молочной железы и шейки матки.
Классификация
Стадирование злокачественных новообразований яичников проводят с использованием классификации опухолей, предложенной Международной федерацией акушеров и гинекологов (FIGO, 1985), и по системе TNM (6-е издание) (табл. 18-1, 18-2). • N - регионарные лимфатические узлы. Nx - нет достоверных данных о состоянии регионарных лимфатических узлов.
N0 - нет метастатического поражения регионарных лимфатических узлов.
N1 - метастазы в регионарных лимфатических узлах. • М - отдаленные метастазы.
Мх - нет достоверных данных об отдаленных метастазах.
М0 - нет отдаленных метастазов.
M1 - есть отдаленные метастазы (исключая метастатическое поражение брюшины, метастатическое поражение капсулы печени).
Таблица 18-1. Сравнение классификаций TNM и FIGO злокачественных новообразований яичников
TNM FIGOПризнак
T1 |
I |
Опухоль в пределах яичников (одного или обоих) |
T1a |
IA |
Опухоль ограничена одним яичником, капсула не поражена, нет опухолевого разрастания |
|
|
на поверхности яичника, нет опухолевых клеток в асците и смыве из брюшной полости |
T1b |
IB |
Опухоль ограничена двумя яичниками, капсула не поражена, нет опухолевого |
|
|
разрастания на поверхности яичника, нет опухолевых клеток в асците или смыве из |
|
|
брюшной полости |
T1c |
IC |
Опухоль ограничена одним или двумя яичниками, сопровождается разрывом капсулы, |
|
|
наличием опухолевого разрастания на поверхности яичника, наличием злокачественных |
|
|
клеток в асцитической жидкости или смыве из брюшной полости |
T2 |
II |
Опухоль поражает один или два яичника с распространением на таз |
T2a |
IIA |
Распространение и/или метастазирование в матку и/или одну или обе трубы |
T2b |
IIB |
Распространение на другие ткани таза, нет опухолевых клеток в асците или в смыве из |
|
|
брюшной полости |
Т2С |
IIC |
Распространение в область таза (2а или 2b) с наличием опухолевых клеток в асцитической |
|
|
жидкости или смыве из брюшной полости |
Т3 |
III |
Опухоль поражает один или оба яичника с микроскопически подтвержденными |
и/или |
|
внутрибрюшинными метастазами за пределами таза и/или метастазами в регионарных |
|
лимфатических узлах |
|
N1 |
|
|
|
|
|
Т3а |
IIIA |
Микроскопически подтвержденные внутрибрюшинные метастазы за пределами таза |
Т3b |
IIIB |
Макроскопические внутрибрюшинные метастазы за пределами таза до 2 см в наибольшем |
|
|
измерении |
Т3с |
IIIC |
Внутрибрюшинные метастазы за пределами таза более 2 см в наибольшем измерении |
и/или |
|
и/или метастазы в регионарных лимфатических узлах |
N1 |
|
|
М1 |
IV |
Отдаленные метастазы (исключая внутрибрюшинные метастазы) |
Тx |
|
Недостаточно данных для оценки первичной опухоли Первичная опухоль не определяется |
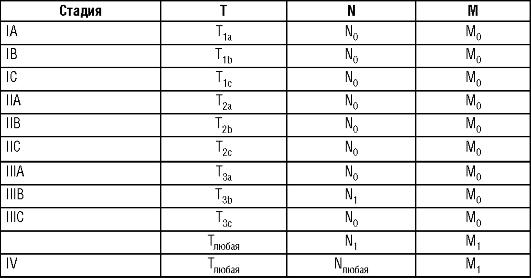
Таблица 18-2. Группировка злокачественных новообразований яичников по стадиям
Гистологическая классификация опухолей яичников (ВОЗ, 1996)
Гистологическая классификация опухолей яичников была создана в 1973 г. С.Ф. Серовым, Р.Е. Скалли в сотрудничестве с Л. Со-биным. В 1996 г. модифицирована и используется в настоящее время онкогинекологами всего мира. По этой классификации все опухоли яичников разделены на 11 групп.
• Эпителиальные опухоли:
Данная книга в списке рекомендаций к покупке и прочтению форума сайта https://meduniver.com/
серозные;
муцинозные;
эндометриоидные;
светлоклеточные (мезонефроидные);
опухоли Бреннера;
плоскоклеточные;
смешанные эпителиальные;
недифференцированные карциномы;
неклассифицируемые эпителиальные опухоли.
• Опухоли стромы полового тяжа:
гранулезостромальноклеточные;
андробластомы;
гинандробластомы;
неклассифицируемые опухоли стромы полового тяжа.
• Липидно-клеточные (липоидно-клеточные) опухоли.
• Герминогенные опухоли:
дисгерминомы;
опухоли эндодермального синуса;
эмбриональные карциномы;
полиэмбриомы, хориокарциномы;
тератомы;
смешанные герминогенные опухоли.
•Гонадобластомы.
•Опухоли мягких тканей, неспецифичные для яичников.
•Неклассифицированные опухоли.
•Вторичные (метастатические) опухоли.
•Опухоли неясного генеза.
•Опухоли сети яичника.
•Опухолевидные процессы.
Этиология и патогенез
До настоящего времени нет четко обоснованного представления о происхождении злокачественных опухолей яичников. Существуют три основные гипотезы возникновения и развития неоплазий гонад.
•Согласно первой теории опухоли гонад возникают в условиях гиперреактивности гипоталамо-гипофизарной системы, что приводит к хронической гиперэстрогении. Эстрогены непосредственно не приводят к опухолевой трансформации клетки, но создают условия, при которых резко повышается вероятность возникновения рака в эстрогенчувствительных тканях.
•В основе второй гипотезы лежит фактор непрекращающейся овуляции. При каждой овуляции происходит травма мезоте-лия и, при регенерации разошедшихся краев покрова, могут возникнуть инвагинаты, т.е. нарушение нормальной архитектоники покрова. И именно в этих кистах-включениях, сформировавшихся из инвагинатов, происходит процесс метаплазии, приводящий к развитию злокачественных эпителиальных новообразований.
•Третья (генетическая) теория развития злокачественных новообразований яичников заслуживает пристального внимания в свете последних генетических исследований. Понятие генетической предрасположенности к гормонозависимым опухолям означает наследование по аутосомно-рецессивному типу конституциональных и эндокринно-метаболических особенностей, таких как нарушение овуляции и метаболизма стероидных гормонов, ожирение, сахарный диабет и др.
Клиническая картина
Успех проводимого лечения зависит от ранней диагностики заболевания. Однако в связи с бессимптомным течением процесса злокачественные опухоли яичников в 70-80% случаев выявляют в распространенных (III-IV стадия) формах болезни. Патогномоничных симптомов для неоплазий гонад не существует. Могут встречаться следующие клинические проявления:
•боли и чувство дискомфорта в брюшной полости;
•диспепсия и другие нарушения деятельности желудочно-кишечного тракта;
•нарушения менструального цикла (чаще при гормонально-активных опухолях);
•увеличение размеров живота как за счет асцита, так и за счет опухолевых масс в области брюшной полости и малого таза;
•респираторные симптомы (одышка, кашель) за счет транссудации жидкости в плевральную полость, а также за счет увеличения внутрибрюшного давления (нарастание асцита и массы опухоли).
Диагностика
Данная книга в списке рекомендаций к покупке и прочтению форума сайта https://meduniver.com/
•Прецизионный сбор анамнеза (с учетом наследственных и других факторов риска). Полное физикальное обследование пациентки (с обязательной оценкой состояния молочных желез).
•Бимануальное ректовагинальное обследование с цитологическим контролем состояния шейки матки и эндометрия, пункция заднего влагалищного свода для морфологической верификации характера опухолевого процесса (с обязательным соблюдением правил абластики).
•Лабораторные тесты (включая развернутые биохимический и общеклинический анализы крови, анализ мочи).
•Рентгенологическое исследование грудной клетки.
•Абдоминальная (чувствительность - 62-100%) и трансвагинальная
(чувствительность - 100%, специфичность - 97%) ультрасонография с использованием цветной допплероме-трии.
•Компьютерная или магнитно-резонансная томография (с внутривенным контрастированием) органов брюшной полости и малого таза (во время лечения, в мониторинге для выявления рецидива). В процессе диагностики, лечения и мониторинга используют один и тот же метод визуализации.
•Обследование органов ЖКТ (эндоскопическое или рентгенологическое).
Исследование уровня опухолевых маркёров. Определение опухолевых маркёров СА 125, СА 19-9, СА 72-4 (по показаниям); ингибин В, эстрадиол (при гранулезоклеточных опухолях), α-фетопротеин, β-ХГЧ, ЛДГ (при герминогенных опухолях - перед началом лечения, перед началом каждого курса химиотерапии, перед хирургическим вмешательством, при I стадии - после хирургического лечения каждые 1-2 нед до нормализации или роста их уровня), РЭА. Определение уровня опухолевых маркёров рекомендовано для оценки эффективности проводимого лечения и дальнейшего мониторинга.
Для постановки окончательного диагноза требуется хирургическое вмешательство с процедурами адекватного хирургического стадирования, которое включает следующие манипуляции: срединная, нижнесрединная лапаротомия с обходом пупка слева для полноценной ревизии органов брюшной полости и обеспечения адекватного доступа к большому сальнику (в спе-
циализированных онкологических учреждениях, со срочным ин-траоперационным морфологическим исследованием, возможно выполнение операции лапароскопическим доступом), цитологическое исследование мазков с брюшины (в том числе с ее диа-фрагмальной поверхности, латеральных каналов и малого таза); производят биопсию подозрительных участков брюшины; выполняют пункцию и/или селективное удаление подозрительных по метастазированию тазовых и парааортальных лимфатических узлов, удаление большого сальника на уровне большой кривизны желудка, множественная биопсия париетальной
брюшины (абдоминальной поверхности диафрагмы, латеральных каналов с обеих сторон, пузырно-маточной и прямокишечно-маточной складок - минимум 10 биоптатов), биопсия подвздошных и па-рааортальных лимфатических узлов.
При выявлении метастазов в лимфатических узлах должна быть дополнительно выполнена тотальная подвздошная и/или парааортальная лимфаденэктомия.
При муцинозной форме рака показана аппендэктомия.
• Документирование в протоколе операции того, что было обнаружено и что оставлено.
При обнаружении плеврального выпота, асцита последние должны быть верифицированы морфологически с целью адекватного стадирования.
Скрининг
В настоящее время нет эффективных скрининговых программ по выявлению злокачественных опухолей яичников. У женщин с обычным риском развития этой нозологической формы заболевания достаточным бывает проведение бимануального осмотра с обязательной оценкой состояния ректовагинальной перегородки, УЗИ малого таза и определение уровня опухолевого маркёра СА 125 (в последние несколько лет предлагают использовать дополнительно маркёр НЕ4). Пациенткам с наличием в анамнезе семейного рака яичников и/или рака молочной железы необходимо проводить генетическое тестирование для определения мутаций BRCA1 и BRCA2.
Дифференциальная диагностика
Злокачественные опухоли яичников дифференцируют от следующих заболеваний:
•воспалительные объемные образования (тубоовариальные образования и абсцессы);
•опухолеподобные поражения яичников (функциональные кисты яичников);
•доброкачественные опухоли яичников;
•субсерозная миома матки;
•метастатическое поражение яичников;
•злокачественные опухоли маточной трубы.
Показания к консультации других специалистов
Все больные с подозрением на злокачественный процесс гениталий должны быть консультированы онкогинекологом для коррекции плана уточняющего обследования. При установленном диагнозе злокачественной опухоли яичников выработка индивидуального плана ведения пациентки определяется на консилиуме с участием химиотерапевтов и специалистов лучевой терапии.
Данная книга в списке рекомендаций к покупке и прочтению форума сайта https://meduniver.com/
Лечение Цели лечения
Выбор объема хирургического вмешательства и послеоперационной терапии (химиотерапия и/или лучевая терапия) определяется стадией заболевания и другими клинико-морфологическими прогностическими факторами. Основная цель органосохраняющих операций - ликвидация опухолевого процесса с соблюдением принципов онкологической радикальности и сохранением репродуктивной функции. При распространенном процессе или прогрессировании заболевания может быть достигнуто продление жизни (паллиативное лечение) и/или улучшение ее качества (симптоматическое лечение).
Показания к госпитализации
Госпитализация показана для осуществления хирургического лечения, химио- и лучевой терапии, в ряде случаев - для проведения сложных диагностических манипуляций (например, лапароскопии).
Хирургическое лечение
Ранние стадии болезни (IA и IB по FIGO)
Оперативное вмешательство должно включать гистерэктомию и двустороннюю сальпингоофорэктомию с удалением большого сальника и выполнением всех диагностических манипуляций, включенных в процедуру адекватного хирургического стадирования. У молодых женщин, желающих сохранить детородную функцию, с IA стадией заболевания и благоприятной морфологической формой опухоли G1 (кроме светлоклеточных неоплазий и новообразований, G2-3) допустимо выполнение односторонней сальпингоофорэктомии с обязательной клиновидной резекцией контралатеральной гонады и субтотальной резекцией большого сальника без существенного увеличения риска рецидивирования.
Распространенные стадии болезни (1С, II и III по FIGO) Оперативное вмешательство должно включать гистерэктомию и двустороннюю сальпингоофорэктомию с удалением большого сальника и выполнением биопсий брюшины и проведением всех диагностических манипуляций, включенных в процедуру адекватного хирургического стадирования. Оценка характера операции в зависимости от объема остаточной опухоли:
•оптимальная циторедуктивная операция - отсутствие визуальных признаков остаточной опухоли в брюшной полости, области малого таза и забрюшинном пространстве или наличие остаточной опухоли до 1 см в наибольшем измерении;
•субоптимальная циторедуктивная операция - наличие остаточной опухоли до 2 см в наибольшем измерении;
•неоптимальная циторедуктивная операция - наличие остаточной опухоли более 2 см в наибольшем измерении.
