
- •Министерство образования и науки
- •Предисловие авторов
- •Содержание
- •1 Химическая термодинамика
- •1.1 Первое начало термодинамики
- •1.1.1 Основные понятия и определения
- •1.1.2 Первое начало термодинамики
- •1.1.3 Теплоемкость
- •1.1.4 Работа и теплота термодинамических процессов
- •1.1.5 Типы тепловых эффектов
- •1.1.6 Способы определения тепловых эффектов при постоянной температуре
- •1.1.7 Зависимость теплового эффекта реакции от температуры
- •1.1.8 Примеры решения задач
- •1.1.9 Вопросы для самоконтроля
- •1.2 Второе начало термодинамики
- •1.2.1 Основные понятия и определения
- •1.2.2 Математическое выражение
- •1.2.3 Изменение энтропии как критерий обратимости и необратимости процессов
- •1.2.4 Критерии направленности процессов в реальных системах
- •1.2.5 Расчет изменения энтропии в различных процессах
- •1.2.6 Фугитивность и коэффициент фугитивности реальных газов
- •1.2.7 Химический потенциал идеального и реального газа
- •1.2.8 Примеры решения задач
- •1.2.9 Вопросы для самоконтроля
- •1.3 Химическое равновесие
- •1.3.1 Закон действующих масс
- •1.3.2 Способы выражения константы равновесия
- •1.3.3 Выражение состава равновесной смеси
- •1.3.4 Влияние различных факторов на смещение равновесия (на состав равновесной смеси)
- •1.3.5 Мера химического сродства. Направление самопроизвольного протекания химической реакции
- •1.3.6 Методы определения константы равновесия при различной температуре (из справочных данных)
- •1. Из термодинамических свойств веществ:
- •4. Из логарифмов констант равновесия реакций образования некоторых веществ, lgKaf.
- •1.3.7 Примеры решения задач
- •1.3.8 Вопросы для самоконтроля
- •2 Фазовые равновесия
- •2.1 Основные понятия и определения
- •2.2 Однокомпонентные системы
- •2.3 Примеры решения задач
- •2.4 Вопросы для самоконтроля
- •2.5 Двухкомпонентные системы
- •2.5.1 Термический анализ как часть физико-химического анализа
- •2.5.2 Равновесие раствор – кристаллический компонент
- •2.5.3 Кривые охлаждения
- •2.5.4 Диаграмма плавкости двухкомпонентной системы с простой эвтектикой
- •2.6 Диаграммы состояния с образованием химического соединения
- •2.6.1 Определение состава фаз и относительного количества фаз
- •2.6.2 Диаграмма состояния системы с устойчивым химическим соединением
- •2.6.3 Диаграмма состояния системы с неустойчивым химическим соединением (с перитектическим превращением)
- •2.7 Диаграмма состояния с ограниченной растворимостью в жидком состоянии (с монотектическим превращением)
- •2.8 Твердые растворы
- •2.8.1 Диаграмма состояния с полной растворимостью в жидком и твердом состоянии
- •2.8.2 Диаграмма состояния с ограниченной растворимостью в твердом виде
- •1. Диаграммы с эвтектическим превращением
- •2. Диаграмма с перитектическим превращением
- •2.8.3 Примеры разбора диаграмм
- •2.8.4 Вопросы для самоконтроля
- •Литература
2.8.1 Диаграмма состояния с полной растворимостью в жидком и твердом состоянии
При неограниченной растворимости во время кристаллизации образуется непрерывный ряд твердых растворов. Диаграмма состояния такой системы изображена на рисунке 2.10. Подобную диаграмму имеют системы: Cu – Ni, Fe – Ni, Fe – Cо, Bi – Sb и другие.

Рисунок 2.10 – Диаграмма состояния с образованием непрерывного ряда твердых растворов
Верхняя кривая - линия ликвидуса, отображает в любой точке состав жидкого раствора. Нижняя линия – линия солидуса, отвечает за состав твердого раствора (α). Области выше линии ликвидуса и ниже линии солидуса – однофазные. Область между этими линиями – область двухфазного равновесия жидкости и кристаллов α. При охлаждении сплава 1, достигнув температуры, отвечающей точке 2, начинается кристаллизация α – твердого раствора состава 2I . По мере охлаждения системы количество твердой фазы увеличивается, а жидкой - уменьшается. Так, в точке 3 количество твердой фазы отвечает участку конноды 3II – 3, а количество жидкой фазы участку 3I -3. Затвердевание заканчивается в точке 4, где имеются последние капли жидкости. Процесс кристаллизации сопровождается изменением состава как жидкости по линии ликвидуса (от точки 2 к точке 4II), так и твердого раствора (от точки 2I до точки 4).
Следует учесть, что, говоря о равновесии жидкости и твердой фазы при той или иной температуре, мы имеем в виду средний состав как всей выпавшей к этому моменту твердой фазы, так и оставшейся жидкости. В твердом состоянии кристаллы не будут однородны по составу: центральные области кристаллических зерен, закристаллизовавшиеся раньше, будут обогащены более тугоплавким компонентом, В. Однородность достигается за счет протекающей диффузии в твердом состоянии, которая происходит медленно.
Твердые растворы могут давать смеси, в которых состав жидкой и твердой фаз одинаков. Это отражается на диаграмме в виде экстремумов – минимума или, реже, максимума (рисунок 2.11).

Рисунок 2.11 - Диаграмма с образованием минимума на кривых ликвидуса и солидуса при образовании твердых растворов
2.8.2 Диаграмма состояния с ограниченной растворимостью в твердом виде
Весьма часто компоненты, взаимно неограниченно растворимые в жидкой фазе, обладают ограниченной растворимостью в твердом состоянии. При этом возможны два типа соотношений между составами жидкой фазы и выделяющегося из нее твердого раствора и два типа диаграмм.
1. Диаграммы с эвтектическим превращением
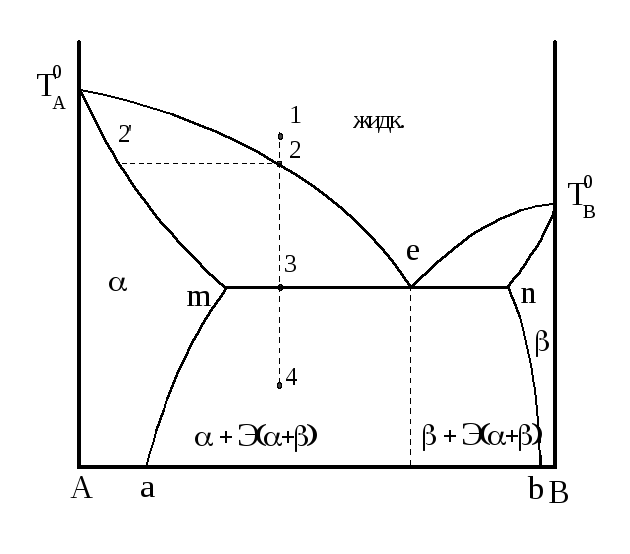
Рисунок – 2.12 – Диаграмма состояния системы с ограниченной растворимостью в твердом виде при наличии эвтектического превращения
Область АТ0Аma отвечает однородному твердому раствору В в А (α – твердый раствор). Линия Т0Ае – линия кристаллизации α – твердых растворов. Линия ma – линия предельной растворимости В в А (α – насыщенный твердый раствор) в зависимости от температуры. Линия Т0Аm – линия состава α – ненасыщенного твердого раствора.
Аналогично область Т0ВВbn – область растворов А в В (β – твердый раствор). Линия Т0Ве – начало кристаллизации β – твердого раствора. Т0Вn – линия состава ненасыщенных β – твердых растворов; nb – насыщенных β – твердых растворов.
Проведем охлаждение раствора 1. При понижении температуры в точке 2 жидкий раствор становится насыщенным и начинает кристаллизоваться α – ненасыщенный твердый раствор состава 2I. По мере охлаждения от точки 2 до точки 3 количество твердого раствора увеличивается, а его состав меняется от точки 2I до точки «m» и достигает предела растворимости В в А в точке «m». При этом состав жидкой фазы меняется по линии ликвидуса от точки 2 до «е». Раствор состава «е» является насыщенным по отношению к α - и β – твердым растворам (точка «е» принадлежит как линии Т0Ае так и линии Т0Ве), следовательно, из него кристаллизуются одновременно оба твердых раствора, т.е. эвтектика (α + β). Состав α и β в эвтектике отвечает точкам «m» и «n» соответственно.
При дальнейшем охлаждении системы растворимость А в В и В в А уменьшается и идет по линиям mа и nb, показывающим состав твердых растворов α и β (насыщенных).
В этой системе температура кристаллизации растворов всегда ниже температуры кристаллизации чистого компонента, который принимается за растворитель и чей тип кристаллической решетки сохраняется при образовании твердого раствора. Так, α – твердый раствор – это раствор В в А и тип кристаллической решетки вещества А сохраняется. Для β – твердого раствора растворителем является компонент В и его тип кристаллической решетки сохраняется при растворении в нем компонента А.; Тβ < Т0В.
Жидкая фаза любого состава в диаграммах этого типа содержит больше растворенного вещества, чем твердая фаза, т.е. СВжидк. > СαВ и САжидк. > СβА.
