
диссертации / 17
.pdf121
пы также выявлено отклонение от равновесия Харди-Вайнберга (HWE), обу-
словленное избытком гетерозигот (p=0,001).
Оксид азота, синтезируемый eNOS, оказывает мощное воздействие на реснитчатый эпителий бронхов, регулирует мукоцилиарный клиренс, участ-
вует в иммунной защите, участвует в регуляции тонуса сосудов и бронхов
[35, 134, 171].
В гене NOS3 проведен анализ мини-сателлитного полиморфизма, обу-
словленного варьирующим числом тандемных 27 п. н. повторов (VNTR) в 4
интроне; определялось два аллеля *4 и *5. Выявлена более высокая частота минорного аллеля *4 VNTR гена NOS3 в выборке агинских бурят, больных БА, по сравнению с контрольной группой (0,103 против 0,045; p=0,04);
ОШ =2,44; 95%ДИ [1,0–5,8]. Соотношение шансов для носителей генотипов
*4/4 и *4/5 гена NOS3 (VNTR) равно 2,72 (95%ДИ [1,1–7,0]; р=0,03), т.е. но-
сительство аллеля *4 VNTR гена NOS3 является маркером повышенного рис-
ка развития БА у подростков в изучаемой группе населения. Не установлено ассоциации данного полиморфизма с развитием БА у русских больных (табл.
30).
При изучении этнических особенностей распределения частот аллелей и генотипов показано, что среди больных БА частота минорного аллеля *4 у
русских подростков (0,236) выше, чем у бурят (0,103); частота аллеля *5 у
бурят (0,809) и русских (0,764) (р=0,01). Суммарная частота генотипов *4/4
+ *4/5 NOS3 (VNTR) у русских больных (0,472) также достоверно выше, чем у бурят (0,191) (р=0,005) (табл. 31).
Не выявлено достоверно значимых ассоциаций в частоте аллелей и ге-
нотипов полиморфизма VNTR гена NOS3 со степенью тяжести заболевания,
началом манифестации заболевания до 6 лет, повышенным уровнем IgE в
сыворотке крови у бурят и русских больных БА (р˃0,05).
122
Таблица 30. Частота аллелей и генотипов генов-кандидатов, ассоциированных с развитием бронхиальной астмы
у бурят и русских
|
Аллели, |
|
|
Буряты |
|
|
|
|
χ2, p |
|
|
ОШ |
|
Русские |
|
|
|
|
χ2, p |
ОШ |
||||||||
|
генотипы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[95%ДИ] |
|
|
|
|
|
|
|
|
|
|
[95%ДИ] |
|
|
|
БА |
|
|
Контроль |
|
|
|
|
БА |
|
Контроль |
|
|
|
|||||||||||||
|
n (%) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
n=68 |
|
|
n =100 |
|
|
|
|
|
|
|
n=36 |
|
|
n =50 |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
NOS3 (VNTR 27 п.н. в 4 интроне гена eNOS) |
|
|
|
|
|
|
|
|
||||||||||
|
Аллели |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
*4 |
|
14 (0,103) |
|
9 (0,045) |
|
|
4,26; |
|
|
2,44 [1,0–5,8] |
17 (0,236) |
|
15 (0,150) |
|
|
2,05; |
|
|||||||||||
*5 |
|
122 (0,897) |
|
191 (0,955) |
|
|
|
p=0,04 |
|
|
0,41 [0,2–0,98] |
55 (0,764) |
|
85 (0,850) |
|
|
|
р=0,15 |
|
|||||||||
|
Генотипы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
*4/*4+*4/*5 |
|
13 (0,191) |
|
8 (0,080) |
|
|
4.57; |
|
2,72 [1,1-7,0] |
17 (0,472) |
|
14 (0,280) |
|
|
3,35; |
|
||||||||||||
*5/*5 |
|
55 (0,809) |
|
92 (0,920) |
|
|
|
p=0,03 |
|
|
0,37 [0,1–0,9] |
19 (0,528) |
|
36 |
(0,720) |
|
|
|
р=0,07 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
HWE (χ2, р) |
|
0,03; p>0,05 |
|
|
1,26; p>0,05 |
|
|
|
|
|
|
2,63; p>0,05 |
|
0; p>0,05 |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NOS2А (CCTTT)n |
|
|
|
|
|
|
|
|
|
|
|
||
|
Аллели |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S 9-11 повторов |
32 |
(0,235) |
|
53 (0,265) |
|
|
0,38; |
|
|
|
21 (0,292) |
|
12 |
(0,120) |
|
|
7.96; |
3,02 [1,4–6,6] |
|||||||||
|
L 12-19 повторов |
104 (0,765) |
|
147 (0,735) |
|
|
|
р=0,54 |
|
|
|
51 (0,708) |
|
88 |
(0,880) |
|
|
|
р=0,005 |
0,33 [0,2 – 0,7] |
||||||||
*9 |
|
1 (0,007) |
|
|
|
|
- |
|
|
|
|
|
|
|
- |
|
|
|
- |
|
|
- |
|
|||||
*10 |
|
21 (0,154) |
|
21 |
(0,105) |
|
|
|
р=0,18 |
|
|
|
8 (0,111) |
|
6 (0,060) |
|
|
|
р=0,23 |
|
||||||||
*11 |
|
10 |
(0,074) |
|
32 |
(0,160) |
|
|
5,53; |
|
0,42 [0,2-0,9] |
12 (0,167) |
|
6 |
(0,060) |
|
|
5,08; |
3,11 [1,1-9,4] |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
p=0,02 |
|
|
|
|
|
|
|
|
|
|
|
|
p=0,024 |
|
|
*12 |
|
|
29 (0,213) |
|
|
|
36 |
(0,180) |
|
|
|
р=0,45 |
|
|
|
|
18 (0,250) |
|
|
24 |
(0,240) |
|
|
|
р=0,88 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
*13 |
|
|
21 |
(0,136) |
|
|
|
37 |
(0,185) |
|
|
|
0,53; |
|
|
|
|
10 (0,139) |
|
|
30 |
(0,300) |
|
|
|
6,09; |
0,38 [0,2-0,8] |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
р=0,47 |
|
|
|
|
|
|
|
|
|
|
|
|
р=0,014 |
|
|
*14 |
|
|
11 |
(0,081) |
|
|
|
20 |
(0,100) |
|
|
|
р=0,55 |
|
|
|
|
9 (0,125) |
|
|
17 (0,170) |
|
|
|
р=0,42 |
|
|
|
*15 |
|
|
15 (0,110) |
|
|
|
15 (0,075) |
|
|
|
р=0,27 |
|
|
|
|
4 (0,056) |
|
|
9 (0,090) |
|
|
|
р=0,40 |
|
|||
123
*16 |
13 (0,096) |
21 (0,105) |
|
р=0,78 |
|
7 (0,097) |
8 (0,080) |
|
р=0,69 |
|
|
*17 |
8 (0,059) |
7 (0,035) |
|
р=0,30 |
|
2 (0,028) |
- |
|
- |
|
|
*18 |
6 (0,044) |
11 (0,055) |
|
р=0,66 |
|
2 (0,028) |
- |
|
- |
|
|
*19 |
1 (0,007) |
- |
|
- |
|
|
- |
- |
|
- |
|
Генотипы |
|
|
|
|
|
|
|
|
|
|
|
SS+SL |
28 (0,412) |
44 (0,440) |
0,13; |
|
19 (0,528) |
11 (0,220) |
8.74; |
3,96 [1,6 – 10,1] |
|||
LL ≥12 повторов |
40 (0,588) |
56 (0,560) |
|
р=0,72 |
|
17 (0,472) |
39 (0,780) |
|
p=0,01 |
0,25 [0,1 – 0,6] |
|
HWE (χ2, р) |
0; p>0,05 |
0,50; p>0,05 |
|
|
|
0,35; p>0,05 |
0,04; p>0,05 |
|
|
|
|
|
|
|
|
GSDM B rs7216389 |
|
|
|
|
|
|
|
Аллели |
|
|
|
|
|
|
|
|
|
|
|
T |
107 (0,787) |
116 (0,580) |
14,59; |
2,66 [1,6–4,4] |
58 (0,806) |
62 (0,620) |
6,83; |
2,54 [1,3–5,2] |
|||
C |
29 (0,213) |
84 (0,420) |
|
р=0,00011 |
0,38 [0,2–0,6] |
14 (0,194) |
38 (0,380) |
|
р=0,009 |
0,39 [0,2–0,8] |
|
Генотипы |
|
|
|
|
|
|
|
|
|
|
|
TT |
45 (0,662) |
23 (0,230) |
31.32; |
6,55 [3,3–12,9] |
24 (0,667) |
20 (0,400) |
5,96; |
3,00 [1,2–7,3] |
|||
CC+CT |
23 (0,338) |
77 (0,770) |
|
p<0,0001 |
0,14 [0,08–0,3] |
12 (0,333) |
30 (0,600) |
|
p=0,01 |
0,33 [0,1-0,8] |
|
HWE (χ2, р) |
2,0; p>0,05 |
10,66; p<0,05 |
|
|
|
0,39; p>0,05 |
0,18; p>0,05 |
|
|
|
|
|
|
|
|
GSDMB rs2305480 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Аллели |
|
|
|
|
|
|
|
|
|
|
|
A |
77 (0,566) |
101 (0,505) |
1,22; |
|
30 |
(0,417) |
52 (0,520) |
1,79; |
|
||
G |
59 (0,434) |
99 (0,495) |
|
p=0,27 |
|
42 (0,583) |
48 (0,480) |
|
p=0,18 |
|
|
Генотипы |
|
|
|
|
|
|
|
|
|
|
|
AA |
26 (0,382) |
25 (0,250) |
4,17; |
|
4 (0,111) |
14 (0,280) |
3,64; |
|
|||
AG |
25 (0,368) |
51 (0,510) |
|
p=0,12 |
|
22 (0,611) |
24 (0,480) |
|
p=0,16 |
|
|
GG |
17 (0,250) |
24 (0,240) |
|
|
|
10 |
(0,278) |
12 (0,240) |
|
|
|
HWE (χ2, р) |
0,04; p>0,05 |
1,97; p>0,05 |
|
|
|
0,98; p>0,05 |
0,01; p>0,05 |
|
|
|
|
|
|
|
|
FCER2 (T2206C) |
|
|
|
|
|
|
|
Аллели |
|
|
|
|
|
|
|
|
|
|
|
T |
112 (0,824) |
159 (0,795) |
0,42; |
|
47 (0,653) |
78 (0,780) |
3,41; |
|
|||
C |
24 (0,176) |
41 (0,205) |
|
p=0,52 |
|
25 (0,347) |
22 (0,220) |
|
p=0,06 |
|
|
Генотипы |
|
|
|
|
|
|
|
|
|
|
|
124
T/T |
46 (0,676) |
62 (0,620) |
0,59; |
|
16 (0,444) |
31 (0,620) |
3,12; |
|
C/T |
20 (0,294) |
35 (0,350) |
p=0,75 |
|
15 (0,417) |
16 (0,320) |
p=0,21 |
|
C/C |
2 (0,029) |
3(0,030) |
|
|
5 (0,139) |
3 (0,060) |
|
|
HWE (χ2, р) |
0; p>0,05 |
0,21; p>0,05 |
|
|
0,16; p>0,05 |
0,24; p>0,05 |
|
|
|
|
|
ADRB2 (Arg16Gly) |
|
|
|
|
|
Аллели |
|
|
|
|
|
|
|
|
A |
77 (0,566) |
111 (0,555) |
0,04; |
|
37 (0,514) |
47 (0,470) |
0,32; |
|
G |
59 (0,434) |
89 (0,455) |
p=0,84 |
|
35 (0,486) |
53 (0,530) |
p=0,57 |
|
Генотипы |
|
|
|
|
|
|
|
|
A/A |
22 (0,324) |
38 (0,380) |
3,25; |
|
8 (0,222) |
7 (0,140) |
1,01; |
|
A/G |
33 (0,485) |
35 (0,350) |
p=0,2 |
|
21 (0,583) |
33 (0,660) |
p=0,6 |
|
G/G |
13 (0,191) |
27 (0,270) |
|
|
7 (0,194) |
10 (0,200) |
|
|
HWE (χ2, р) |
0; p>0,05 |
4,09; p<0,05 |
|
|
0,69; p>0,05 |
2,66; p>0,05 |
|
|
|
|
|
ADRB2 (Gln27Glu) |
|
|
|
|
|
Аллели |
|
|
|
|
|
|
|
|
C |
89 (0,654) |
139 (0,695) |
0,61; |
|
44 (0,611) |
51 (0,510) |
1,73; |
|
G |
47 (0,346) |
61 (0,305) |
p=0,43 |
|
28 (0,389) |
49 (0,490) |
p=0,19 |
|
Генотипы |
|
|
|
|
|
|
|
|
C/C |
33 (0,485) |
49 (0,490) |
2,36; |
|
12 (0,333) |
13 (0,260) |
2,38; |
|
C/G |
23 (0,338) |
41 (0,410) |
p=0,31 |
|
20 (0,556) |
25 (0,500) |
p=0,3 |
|
G/G |
12 (0,176) |
10 (0,100) |
|
|
4 (0,111) |
12 (0,240) |
|
|
HWE (χ2, р) |
2,24; p>0,05 |
0,07; p>0,05 |
|
|
0,38; p>0,05 |
0; p>0,05 |
|
|
|
|
|
TNFA (-308G˃A) |
|
|
|
|
|
Аллели |
|
|
|
|
|
|
|
|
A |
17 (0,125) |
15 (0,075) |
2,35; |
|
9 (0,125) |
11 (0,110) |
0,09; |
|
G |
119 (0,875) |
185 (0,925) |
p=0,13 |
|
63 (0,875) |
89 (0,890) |
p=0,76 |
|
Генотипы |
|
|
|
|
|
|
|
|
A/A |
2 (0,029) |
- |
3,60; |
|
2 (0,056) |
1 (0,020) |
0,98; |
|
A/G |
13 (0,191) |
15 (0,150) |
p=0,17 |
|
5 (0,139) |
9 (0,180) |
p=0,61 |
|
G/G |
53 (0,779) |
85 (0,850) |
|
|
29 (0,806) |
40 (0,800) |
|
|
HWE (χ2, р) |
0,49; p>0,05 |
1,04; p>0,05 |
|
|
1,03; p>0,05 |
0,04; p>0,05 |
|
|

125
делеционный полиморфизм гена GSTM1
Генотипы |
|
|
|
|
|
|
|
|
*0/*0 |
24 (0,353) |
42 (0,420) |
0,76; |
|
17 (0,472) |
21 (0,420) |
0,23; |
|
N (*0/*1 +*1/*1) |
44 (0,647) |
58 (0,580) |
p=0,48 |
|
19 (0,528) |
29 (0,580) |
p=0,63 |
|
Примечание: аллели гена NOS2 с числом повторов меньше одиннадцати - «короткие» аллели (S), аллели с числом повторов более двенадцати - «длинные» аллели (L) (выделены в таблице серым цветом)
126
Таблица 31. Значимые межэтнические различия в частотах аллелей и ге-
нотипов генов NOS3 (VNTR), GSDMB rs 2305480, FCER2 (T2206C), THOI
(STR) у больных бронхиальной астмой
Аллели, гено- |
БА |
|
χ2, p |
|
типы |
Буряты |
|
Русские |
|
n (%) |
(n=68) |
|
(n=36) |
|
NOS3 (VNTR 27 п.н. в 4 интроне гена eNOS) |
||||
Аллели |
|
|
|
|
*4 |
14 (0,103) |
|
17 (0,236) |
6,58 |
*5 |
122 (0,897) |
|
55 (0,764) |
p=0,01 |
Генотипы |
|
|
|
|
*4/*4+*4/*5 |
13 (0,191) |
|
17 (0,472) |
10,53 |
*5/*5 |
55 (0,809) |
|
19 (0,528) |
p=0,005 |
HWE (χ2, р) |
0,03; p>0,05 |
|
2,63; p>0,05 |
|
|
GSDMB rs 2305480 |
|
||
Аллели |
|
|
|
|
A |
77 (0,566) |
|
30 (0,417) |
4,21 |
G |
59 (0,434) |
|
42 (0,583) |
p=0,04 |
Генотипы |
|
|
|
|
A/A |
26 (0,382) |
|
4 (0,111) |
8,44 |
A/G +G/G |
42 (0,618) |
|
32 (0,889) |
p=0,004 |
HWE (χ2, р) |
1,97; p>0,05 |
|
0,98; p>0,05 |
|
|
FCER2 (T2206C) |
|
||
Аллели |
|
|
|
|
T |
112 (0,824) |
|
47 (0,653) |
7,62 |
C |
24 (0,176) |
|
25 (0,347) |
p=0,006 |
Генотипы |
|
|
|
|
T/T |
46 (0,676) |
|
16 (0,444) |
5,26 |
C/T +C/C |
22 (0,324) |
|
20 (0,556) |
p=0,02 |
HWE (χ2, р) |
0; p>0,05 |
|
0,16; p>0,05 |
|
|
THOI (STR) |
|
||
Аллели |
|
|
|
|
S 6-9 повторов |
126 (0,926) |
|
59 (0,819) |
5,48 |
L 9.3 повторов |
10 (0,074) |
|
13 (0,181) |
р=0,02 |
*8 |
25 (0,184) |
|
4 (0,056) |
6,36; p=0,011 |
*9.3 |
10 (0,074) |
|
13 (0,181) |
5,48; р=0,02 |
Генотипы |
|
|
|
|
SS ≤9 повторов |
59 (0,868) |
|
25 (0,694) |
4,76 |
SL |
8 (0,118) |
|
9 (0,250) |
р=0,09 |
LL=9.3 повто- |
1 (0,015) |
|
2 (0,056) |
|
ров |
|
|
|
|
*6/*7 |
6 (0,044) |
|
10 (0,278) |
6,50; p=0,011 |
HWE (χ2, р) |
1,06; p>0,05 |
|
0,55; p>0,05 |
|
127
Полученные нами данные у русских больных БА согласуются с данны-
ми литературы, не выявившими ассоциации гена NOS3 (VNTR) с развитием БА и уровнем IgE у британских и чешских больных [93, 190, 211]; с тяже-
стью заболевания [253].
Однако в ряде других исследований выявлена ассоциация БА с VNTR
полиморфизмом гена NOS3. Так, в работе Смирновой И.Ю. с соавторами
(2009) генотипы *4/4 и *4/5 встречались чаще при БА по сравнению с кон-
тролем и подверженность к болезни была выше у носителей этих генотипов
(ОР=2,89; 95%ДИ [1,2-7,1]; р=0,01; ОР=4,11; 95%ДИ [1,4-11,6]; р=0,007, со-
ответственно).
Продукт гена индуцибельной синтазы оксида азота регулирует ба-
ланс TH1/TH2, обладает противомикробной и цитотоксической активностью,
влияя на количество продуцируемого NO, поддерживает и усиливает воспа-
лительный процесс в дыхательных путях [134].
Аллели с восемью или девятью повторами CCTTT имеют более низкие уровни транскрипционной активности, чем аллели с 12-15 повторами. У ин-
дивидов – носителей аллелей с более низким числом повторов продуцируется меньше iNOS и, как следствие, вырабатывается меньше оксида азота II (NO),
чем у индивидов – носителей аллелей с более высоким числом повторов
[384].
При изучении микросателлитного полиморфизма (CCTTT)n в промо-
торной области гена NOS2А у бурят идентифицировано 11 аллелей с числом повторов CCTTT от *9 до *19 и 34 генотипа; у русских подростков – 9 алле-
лей от *10 до *18 и 22 генотипа. Ввиду большого числа установленных гено-
типов по гену NOS2A аллели с числом повторов меньше одиннадцати обо-
значены как «короткие» аллели (S), аллели с числом повторов более двена-
дцати как «длинные» аллели (L), а генотипы – соответственно как SS, SL, LL.
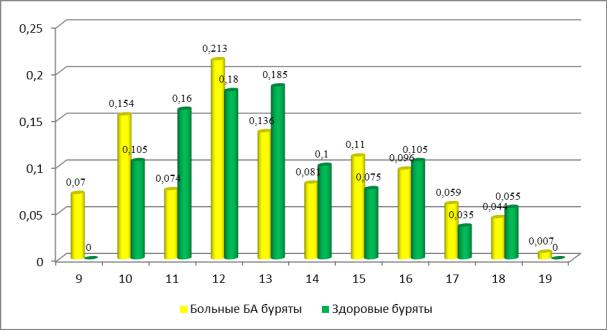
При рассмотрении каждого аллеля гена NO2А отдельно выявлена более низкая частота аллеля *11 в группе бурят-больных БА по сравнению с кон-
трольной группой (0,074 против 0,160; p=0,02; ОШ=0,42 [0,2–0,9]; рис. 7).
128
Однако, различий в частоте аллелей с низким и высоким числом повторов
(CCTTT)n, как и генотипов по гену NO2А между выборками больных и здо-
ровых бурят не установлено (табл. 30). Таким образом, ассоциация гена
NO2А с развитием БА у подростков бурятской национальности в настоящем исследовании не выявлена.
Рис. 7. Частота аллелей NO2А (CCTTT)n у бурят, больных бронхиальной аст-
мой и здоровых.
У больных БА и здоровых русских подростков выявлены статические различия в частоте аллелей S гена NOS2А (0,292 и 0,120, соответственно;
р=0,005, ОШ=3,02; 95%ДИ [1,4-6,6]). Отношение шансов для носителей ге-
нотипов S/S и S/L гена NOS2А (CCTTT)n равно 3,96 (95%ДИ [1,6–10,1];
р=0,003), т. е. носительство аллеля S, содержащего короткое число тандем-
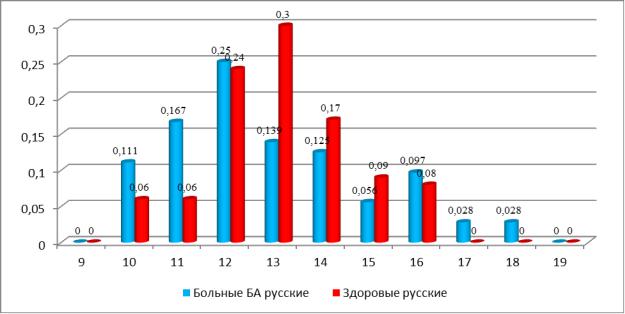
ных повторов CCTTT в гене NOS2А, является маркером повышенного риска развития БА у русских подростков (рис. 8).
129
Рис. 8. Частота аллелей NO2А (CCTTT)n у русских, больных бронхиальной астмой и здоровых.
При анализе частоты каждого аллеля (CCTTT)n гена NO2А выявлено статистически достоверное различие в частотах аллеля *11 и *13 у русских подростков. Частота аллеля *11 выше у больных БА по сравнению со здоро-
выми (0,167 и 0,060, соответственно; p=0,024; ОШ=3,11; 95%ДИ [1,1–9,4]).
Частота аллеля *13 у больных оказалась ниже (0,139) по сравнению со здоро-
выми (0,300) (p=0,014; ОШ=0,38; 95%ДИ [0,2–0,8]) (рис. 8).
При сравнении выборок больных БА межэтнических различий в часто-
те аллелей и генотипов микросателлитного полиморфизма (CCTTT)n гена
NO2А отмечены различия лишь в частоте аллеля *11: у русских больных ал-
лель *11 встречался чаще (0,167) по сравнению с бурятами (0,074; р=0,04)
(табл. 31).
Не выявлено достоверно значимых ассоциаций в частоте аллелей и ге-
нотипов полиморфизма (CCTTT)n гена NO2А со степенью тяжести заболева-
ния, возрастом манифестации заболевания (до 6 лет), повышенным уровнем
IgE в сыворотке крови у бурят и русских больных БА (р˃0,05).
Полученные данные по отсутствию ассоциации развития БА с микро-
сателлитным полиморфизмом (CCTTT)n гена NO2А у бурят согласуются с
130
данными литературы. У китайских детей больных БА также не выявлено ас-
социации полиморфизма (CCTTT)n гена NO2А с БА, с уровнем сенсибилиза-
ции к аэроаллергенам и содержанием NO в выдыхаемом воздухе [258]. Ана-
логично у индийских детей не установлено ассоциации с БА и тяжестью за-
болевания [135]. У японских, китайских, английских, испанских и россий-
ских (из Томска и Башкоркостана) больных также ассоциация с БА не опре-
делена [89, 96, 190, 243, 258, 310].
По данным Смирновой И.Ю. с соавторами [2009] у российских детей с БА не установлено ассоциации (CCTTT)n NO2А с контролируемым течением заболевания на фоне лечения ИГКС. Но показано, что высокое содержание
IgE в сыворотке крови у больных БА ассоциировано с аллелем *14 гена
NO2А (р=0,02); раннее начало болезни (до 2 лет) характерно для пациентов с БА, имеющих гомозиготный генотип *14/*14 по гену NO2А (р=0,02); позд-
нее начало болезни (после 5 лет) чаще отмечается у пациентов, не являю-
щихся носителями аллеля *14 (р=0,04) [96].
Ген GSDMB кодирует гасдермин B, входящий в семейство белков с га-
сдерминовым доменом. Известно, что ген гасдермина В принимает участие в регуляции клеточной дифференциации, клеточного цикла и экспрессии генов цитокинов [293, 332]. Ввиду выявляемых ассоциаций активно ведутся иссле-
дования по изучению его роли в развитии БА.
Анализ однонуклеотидного полиморфизма rs7216389 гена GSDMB вы-
явил ассоциации данного ДНК-локуса с бронхиальной астмой у подростков
(агинских бурят и русских). Частота аллеля T полиморфизма rs7216389 у
подростков-бурят, страдающих БА, значительно выше (78,7%), чем в кон-
трольной группе (58,0%; p=0,00011) (табл. 30). Показатель отношения шан-
сов (ОШ) для аллеля T полиморфизма rs7216389 составил 2,66 (95%ДИ [1,6–
4,4]), для аллеля С – 0,38 (95%ДИ [0,2–0,6]). Гомозиготный генотип T/Т по полиморфизму rs7216389 гена GSDMB встречался в группе больных БА до-
стоверно чаще, чем в контроле (соответственно 0,662 и 0,230; p<0,0001). Но-
сительство гомозиготного генотипа T/Т полиморфизма rs7216389, очевидно,
