
- •Глава 1.
- •1.1. Тенденции и проблемы вэжх
- •1.2. Физико-химические критерии совместимости компонентов системы
- •1.3. Хроматографические свойства сорбатов
- •1.3.1. Полярность и гидрофобность
- •1.3.2. Строение сорбата и растворимость
- •1.3.3. Оптические свойства
- •1.3.4. Рефракционные свойства
- •1.4 Сорбенты для вэжх
- •1.4.1 Сорбенты для нормально-фазовой хроматографии
- •1.4.2. Привитые сорбенты для нормально-фазовой хроматографии
- •1.4.3. Сорбенты для обращенно-фазовой хроматографии
- •1.4.4. Сорбенты для эксклюзионной хроматографии
- •1.4.5. Количественная оценка полярных свойств сорбентов
- •1.5. Хроматографические свойства индивидуальных растворителей
- •1.5.1. Оптические свойства
- •1.5.2. Полярность и элюирующая сила
- •1.5.3. Смешиваемость. Миксотропный ряд
- •1.5.4. Обобщенные критерии полярности растворителей
- •1.5.5. Обобщенные критерии элюирующей силы растворителей
- •Глава 2
- •2.1. Плотность и объемные свойства
- •2.2. Вязкость
- •2.3. Показатель преломления
- •2.4. Оптические свойства
- •2.5. Элюирующая сила
- •2.5.1. Элюирующая сила в нормально-фазовой хроматографии
- •2.5.2. Элюирующая сила в обращенно-фазовой хроматографии
- •Глава 3. Изобары температуры кипения бинарных
- •3.1. Азеотропные составы бинарных растворителей, перспективы применения в вэжх
- •3.2. Инвариантное описание изобар температур кипения бинарных
- •Глава 4. Общие закономерности удерживания сорбатов
- •4.1. Нормально-фазовая система сорбат – элюент – сорбент
- •4.2. Нормально-фазовая хроматография гидрофобных сорбатов
- •4.3. Разделение и идентификация таутомерных форм гидрофобных
- •4.4. Обращенно-фазовая система сорбат – элюент – сорбент
- •4.5. Обращенно-фазовая хроматография некоторых гликозидов
- •Глава 5. Хемометрические приемы оптимизации методик вэжх
- •5.1. Принципы построения поисково-аналитических систем для вэжх
- •5.3. Оценка оптимальности состава бинарной подвижной фазы
- •Список литературы
- •394006 Воронеж, ул. 20-летия Октября,84
1.3.3. Оптические свойства
Способность сорбата поглощать излучение в УФ (190-360 нм) и видимом диапазоне (360-800 нм) электромагнитного спектра определяет возможность применять УФ- или спектрофотометрический детекторы (СФД). Количественные измерения сигнала этого типа детектора основаны на законе Бера – Ламберта - Бугера
A=εlc, (3)
где А – оптическая плотность; l – толщина слоя жидкости в оптической ячейке (обычно l=1 см при диаметре светового канала около 0.1 см и рабочем объеме ячейки около 8 мкл); с – концентрация (моль/л), ε – молярный коэффициент экстинкции, л/(моль·см).
Для регистрации хроматографического пика необходимо, чтобы сорбат имел достаточно интенсивное поглощение при длинах волн больших, чем предел пропускания ПФ. Предел пропускания λ*– длина волны, при которой оптическая плотность некомпенсированного слоя растворителя толщиной 1 см достигает 1.0. Наиболее прозрачные ПФ, приготовленные из спектрально чистых растворителей, имеют предел пропускания в области 190-210 нм. Чаще всего обеспечивается предел пропускания ≈230 нм, так как детектирование достаточно большого количества практически значимых сорбатов проводят в области ≥254 нм.
Таблица 3. Полосы поглощения несопряженных хромофоров в неполярных растворителях
Соединение |
λmax, нм |
R-OH |
180-185 |
R-Cl |
170-175 |
R-Br |
200-210 |
R-I |
225-260 |
R-CH=CH2 |
163, 174 |
R-C≡CH |
185, 223 |
R-COCl |
235, 280 |
R-C(O)OH, R-C(O)OR |
195-210 |
R-C(O)NH2 |
175 (214 в воде) |
R-C≡N |
170 |
R3N |
199, 227 |
RC(O)NHC(O)R |
230-240 |
R-NO2 |
270-280 |
R-NO |
600-650, 300 |
R-N=N-R |
347-370 |
R-CHO |
290 |
R-C(O)-R |
270-290, 180-190 |
В табл. 3–7 приведены максимумы поглощения ряда органических соединений, по которым можно ориентироваться при выборе аналитической длины волны [1]. В зависимости от состава ПФ возможны сдвиги полосы поглощения веществ с несопряженными хромофорными группами на 1-11 нм. Батохромный (красный) сдвиг – сдвиг полосы в сторону длинных волн связан с увеличением длины хромофорной системы, приводит к снижению энергии возбуждения. Гипсохромный (синий) сдвиг – сдвиг полосы в сторону коротких волн. Изменение состава ПФ может приводить к гиперхромному и гипсохромному эффектам – соответственно повышению или понижению молярной экстинкции.
Таблица 4. Поглощение ароматических соединений
Соединение |
λmax, нм |
Растворитель |
Бензол |
204, 256 |
Циклогексан |
Нафталин |
190, 220, 286, 312 |
Этанол |
Антрацен |
221, 256, 375 |
Циклогексан |
Азулен |
193, 236, 269, 357 |
Циклогексан |
Фенантрен |
222, 252, 292, 345 |
Циклогексан |
Хинолин |
228, 270, 315 |
Циклогексан |
Изохинолин |
218, 265, 313 |
Циклогексан |
Акридин |
250, 358 |
Этанол |
Пиридин |
195,251,270 |
Гексан |
Пиримидин |
243,298 |
Циклогексан |
Пурин |
220,263 |
Вода |
Пиррол |
210,240 |
Гексан |
Фуран |
205 |
Гексан |
Тиофен |
231 |
Гексан |
Индол |
225, 265 |
Этанол |
Таблица 5. Поглощение монозамещенных производных бензола Ph-R
Заместитель R |
λmax, нм |
Растворитель |
OH |
210.5, 270 |
Вода |
O- |
235, 287 |
Вода |
OCH3 |
217, 269 |
Вода |
NH2 |
230, 280 |
Вода |
NH3+ |
203,254 |
Вода |
NO2 |
252,280,330 |
Гексан |
СНО |
244, 280, 328 |
Этанол |
СООН |
230,270 |
Вода |
СОО- |
224,268 |
Вода |
С(О)СН3 |
240, 278, 319 |
Этанол |
СN |
224,271 |
Вода |
F |
204,254 |
Этанол |
Сl |
210,264 |
Вода |
Br |
210,261 |
Вода |
I |
207,257 |
Вода |
CH3 |
207,261 |
Вода |
CH=CH2 |
244,282 |
Этанол |
С6H5 |
246 |
Этанол |
Таблица 6. Аналитические длины волн природных аналитов
Соединения |
λ, нм |
Растворитель |
Аминокислоты |
200, 210, 215 |
Буферные растворы |
Пептиды и белки |
200-220 |
Буферные растворы |
Нуклеозиды |
240, 254, 260 |
Буферные растворы |
Каротиноиды |
436, 445, 480 |
Гексан - модификатор |
Триглицериды |
203-213 |
Гексан - модификатор |
Эфирные масла |
220 |
Ацетонитрил – вода |
Фосфолипиды |
203-213 |
Ацетонитрил – метанол – вода |
Моно-, дисахариды |
190-200 |
ацетонитрил – вода |
Пуриновые алкалоиды |
280 |
Метанол – буферные растворы |
Жирорастворимые витамины |
292, 320, 365 |
Метанол – вода, гексан - модификатор |
Водорастворимые витамины |
254 |
Метанол – буферные растворы, ацетонитрил – буферный растворы |
Антоцианы и флавоноиды |
280, 300, 520 |
Метанол – вода, ацетонитрил – вода – уксусная кислота |
Нуклеозиды |
254 |
Метанол – вода – буферный раствор |
Таблица 7. Аналитические длины волн для прямого анализа пестицидов, экотоксикантов и других антропогенных веществ
Соединения |
λ, нм |
Растворитель |
Алкилфенолы |
254 |
Ацетонитрил – вода, гексан - модификатор |
Афлатоксины |
365 |
Метанол – ацетонитрил - вода |
Антрацен |
355 |
Метанол – буферные растворы |
Взрывчатые вещества (гексаген, пикриновая кислота) |
213, 220, 280 |
Метанол – буферные растворы |
Взрывчатые вещества (нитробензолы, нитротолуолы) |
254, 260, 330 |
ИПС - вода |
Галловая кислота |
270 |
Буферные растворы |
Гиббереллины |
210, 240 |
Метанол – буферные растворы |
Диаминопиримидины |
260, 267 |
Буферные растворы |
2,4-динитроанилин |
236 |
Метанол – буферные растворы |
2,4-динитрофенол |
293 |
Метанол – буферные растворы |
Дифениламин |
285 |
Гексан - модификатор |
Дибутилфталат |
255 |
Гексан - модификатор |
Диэтилфталат |
275 |
Гексан - модификатор |
Металлоцианиды |
214 |
Ацетонитрил – вода |
Консерванты (типа сорбиновой и бензойной кислоты) |
228, 230 |
Ацетонитрил – буферные растворы |
Кумарин |
273 |
Метанол – буферные растворы |
Продолжение таблицы 7. |
||
Соединения |
λ, нм |
Растворитель |
Мочевина |
285 |
Буферные растворы |
Метилкарбаматы |
206, 254 |
Метанол – вода |
Нафтиламины |
220, 235 |
Изооктан - модификатор |
Никотин |
260 |
Буферные растворы |
Производные анилина |
210, 290 |
Гексан - модификатор |
Нафтойные кислоты |
235, 290 |
Метанол – буферные растворы |
Нитрозамины |
230 |
Ацетонитрил – буферные растворы |
Нитрофенолы |
254 |
Метанол – вода |
Нитробензойная кислота |
260 |
Гексан - модификатор |
Парабены |
254 |
Метанол – вода |
Пирокатехин |
278 |
Метанол – буферные растворы |
ПАУ |
254 |
Ацетонитрил – вода |
Триазины |
220, 254 |
Изооктан – ИПС |
Тиокарбаматы |
207, 254 |
Метанол – вода |
Тиоцианаты, тиосульфаты |
210 |
Буферные растворы |
Тиофенол |
235 |
Изооктан - модификатор |
Фенилкарбаматы |
254 |
Метанол – вода |
Фенилмочевины |
237, 254 |
Гексан - модификатор |
Феноксикарбоновые к-ты |
280 |
Буферные растворы |
Фталевые эфиры |
235 |
Ацетонитрил – вода, |
Хинолин |
265 |
Изооктан - модификатор |
Хлорорганические соединения (типа ДДТ) |
254 |
Изооктан - этилацетат |
Хлорфенолы |
280 |
Метанол – растворы СН3СООН |
Эфиры феноксикарбоновых кислот |
254 |
Буферные растворы |
Зачастую аналитические длины волн, используемые для прямого детектирования соединений, не всегда соответствуют максимумам поглощения, а являются компромиссным решением для анализа смеси аналитов. Для увеличения чувствительности спектрофотометрического детектирования и смещения λ в область свободную от влияния растворителя, применяют, например, предварительную дериватизацию сорбатов.
Электронные спектры органических веществ приобретают в количественной ВЭЖХ еще большую актуальность в связи с внедрением в аналитическую практику фотодиодных матричных детекторов, позволяющих получать либо спектр хроматографического пика, либо хроматограмму в поливолновом режиме, или трехмерную спектрохроматограмму, в которой по одной оси откладывается tR, по другим – оптическая плотность и длина волны (рис. 9).
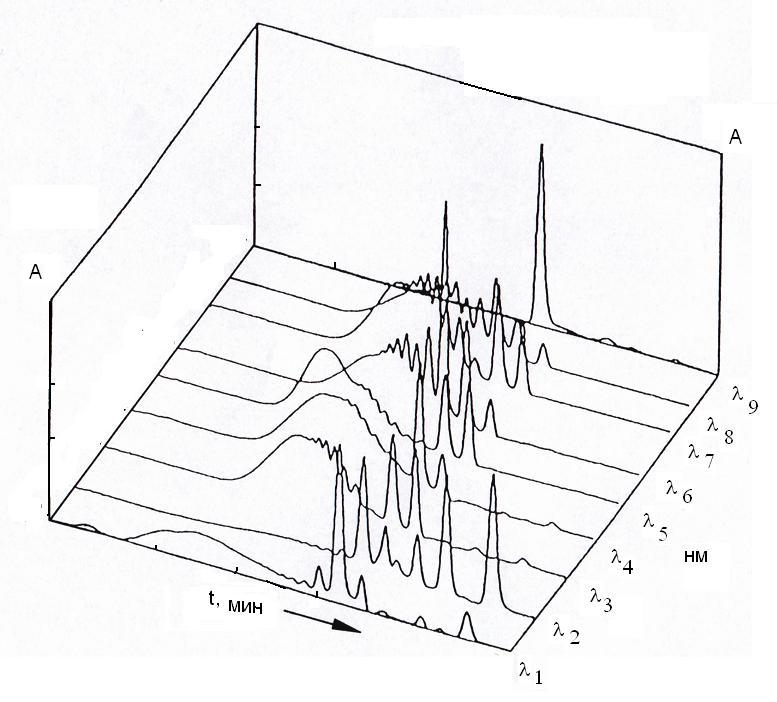
Рис. 9. Хроматограмма смеси сорбатов при 9 аналитических длинах волн
