
- •Химия и токсикология агрохимических препаратов
- •1 Введение
- •2 Пути поступления в организм ксенобиотиков и меры токсичности
- •3 Фитоактивные соединения
- •3.1 Средства воздействия на фотосинтетические процессы
- •3.1.1 Блокаторы транспорта электронов в фотосистеме II
- •3.1.2. Акцепторы электронов фотосистемы I
- •3.1.3. Ингибиторы биосинтеза хлорофилла
- •3.1.4. Ингибиторы биосинтеза каротиноидов
- •3.1.5. Фотодинамические гербициды и противораковые средства
- •3.1.6. Ингибиторы клеточного деления
- •3.1.7 Ингибиторы биосинтеза липидов
- •3.1.8 Ингибиторы образования пластохинона
- •3.1.9 Гербицидные фосфорорганические ингибиторы метаболических превращений
- •3.1.10 Гербициды, нарушающие биосинтез алифатических аминокислот
- •3.2 Гербициды и регуляторы роста растений с фитогормональным механизмом действия
- •3.2.1 Гиббереллины и ингибиторы их образования
- •3.2.2 Синтетические аналоги ауксинов
- •3.2.3 Синтетические аналоги цитокининов
- •3.2.4 Продуценты этилена
- •3.2.5 Другие регуляторы роста и антидоты гербицидов
- •4 Фунгициды
- •5 Инсектициды
- •5.1 Хлорорганические инсектициды
- •5.2 Инсектицидные органические производные кислот фосфора
- •5.3 Карбаматные инсектициды
- •5.4 Пиретрины и пиретроиды
- •5.5 Неоникотиноиды
- •5.6 Ингибиторы биосинтеза хитина
- •5.7 Агонисты ювенильного гормона
- •5.8 Инсектициды с различными механизмами действия
- •5.9 Репелленты и аттрактанты членистоногих
- •5.10 Метод стерильных насекомых
- •Заключение
3.1.5. Фотодинамические гербициды и противораковые средства
Поиски новых фитоактивных соединений, основанные на детальном изучении протекающих в клетках растений биохимических процессов, привели к так называемым фотодинамическим гербицидам. Большие надежды были связаны с первым представителем этой группы фитоактивных соединений ‑аминолевулиновой кислотой, поскольку с неё начинается биосинтез тетрапиррольных соединений, к которым относятся хлорофиллы и гемы. В организме животных ‑аминолевулиновая кислота образуется из сукцинил-кофермента А и глицина при катализе аминолевулинатсинтазой по схеме:

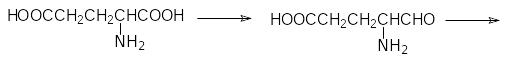
В растениях для биосинтеза этого соединения реализуется другой механизм, основанный на реакции внутримолекулярного переаминирования. Сначала глютаминовая кислота восстанавливается до соответствующего -моноальдегида, а затем карбонильная группа и аминогруппа меняются местами с участием пиридоксальфосфатзависимого фермента:
![]()
Механизм образования пиррольного цикла из этого предшественника точно не установлен, но вероятнее всего в циклизации принимают участие две молекулы аминолевулиновой кислоты в соответствии со схемой:
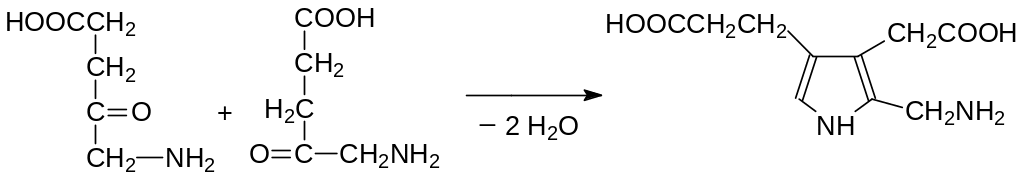
При биосинтезе порфириновых гетероциклов, которые лежат в основе гемов и хлорофиллов, 4 молекулы этого пиррольного соединения – порфобилиногена – вступают в многоступенчатые реакции конденсации с образованием в конце концов циклической молекулы, включающей четыре связанных метиновыми группами пиррольных структурных элемента. Соединяющие пиррольные циклы метиновые линкеры образуются из аминометильных групп порфобилиногена. В дальнейших превращениях остатки пропионовой кислоты сохраняются или превращаются в этильные или винильные группы, а остаток уксусной кислоты может декарбоксилироваться и превращаться в метильную группу.
При поступлении в клетки растений экзогенной -аминолевулиновой кислоты она, как и эндогенная, превращается в хлорофилл. Однако светособирающие молекулы хлорофилла уже плотно упакованы и ориентированы в мембранах тилакоидов так, чтобы их электронные облака перекрывались для обмена электронами. Поэтому «лишнему» хлорофиллу там места нет, и он сорбируется поверхностью клеточных мембран, а энергия его возбужденных поглощением света электронов чаще всего идёт на активацию молекул кислорода с уже известными нам последствиями.
Не исключено, что первоначальная идея использования ‑аминолевулиновой кислоты в качестве фитоактивного соединения состояла в получении регулятора роста растений, интенсифицирующего фотосинтез. Но эффект получился прямо противоположным – образующийся из ‑аминолевулиновой кислоты хлорофилл становится генератором супероксида и синглетного кислорода, которые вызывают оксидативный стресс. ‑Аминолевулиновая кислота является естественным метаболитом, и в соответствии с этим она могла претендовать на роль гербицида четвёртого поколения, но удовлетворительных способов получения этого вещества в больших количествах не найдено, кроме того, она нестабильна и поликонденсируется при хранении по реакции между аминными и карбонильными группами.
В тесной связи с вышеизложенным находится одна из современных областей фармакологии – разработка средств для фотодинамической терапии рака. В основе этого подхода к лечению онкологических заболеваний лежит способность злокачественных клеток избирательно накапливать как эндогенные, так и экзогенные порфирины и многие другие окрашенные вещества. При облучении светом сорбировавших краситель клеток происходит активация электронов окрашенных веществ (их называют сенсибилизаторами для фотодинамической терапии) и перенос возбужденных электронов на кислород. Образующийся при этом активный кислород окисляет прежде всего остатки ненасыщенных кислот в липидах мембран, на которых сорбированы окрашенные вещества. Это в конце концов приводит к появлению карбоксилатых функциональных групп в липидном слое мембран, которые стремятся покинуть гидрофобное окружение. Следствием этого становится появление дефектных участков в мембранах и растворение (лизис) злокачественных клеток. Конечно, от оксидативного стресса страдают и нормальные клетки, но задача синтетиков, разрабатывающих фотосенсибилизаторы для фотодинамической терапии рака, состоит в том, чтобы получить окрашенные вещества, которые сорбируются только злокачественными клетками. Для облучения сорбировавших фотосенсибилизаторы клеток опухолей в недоступных для внешних источников света органах и тканях могут быть использованы лазеры со световодами.
Предъявляемые к фотосенсибилизаторам требования трудно совместить в одном соединении и идеального препарата до сих пор не найдено, но наиболее перспективные соединения получены на основе хлорофиллов и их синтетических аналогов.
Сама -аминолевулиновая кислота оказалась хорошим средством для лечения рака кожи. Обратная связь в биосинтезе порфириновых тетрапиррольных структур действует на этапе образования ‑аминолевулиновой кислоты, то есть при выработке достаточного количества протогема, из которого далее образуются гемы для цитохромов, каталазы, гемоглобина и др., блокируется синтаза -амино-левулиновой кислоты. Поэтому при её поступлении в ткани в готовом виде образуется избыточное количество порфиринов, связывающихся со злокачественными клетками. При лечении рака кожи мазями с ‑аминолевулиновой кислотой с облучением даже обычной лампой накаливания успех достигается в четырех случаях из пяти. В последнее время разрабатываются методики лечения и других видов рака при пероральном введении этого вещества.
