
- •Химия и токсикология агрохимических препаратов
- •1 Введение
- •2 Пути поступления в организм ксенобиотиков и меры токсичности
- •3 Фитоактивные соединения
- •3.1 Средства воздействия на фотосинтетические процессы
- •3.1.1 Блокаторы транспорта электронов в фотосистеме II
- •3.1.2. Акцепторы электронов фотосистемы I
- •3.1.3. Ингибиторы биосинтеза хлорофилла
- •3.1.4. Ингибиторы биосинтеза каротиноидов
- •3.1.5. Фотодинамические гербициды и противораковые средства
- •3.1.6. Ингибиторы клеточного деления
- •3.1.7 Ингибиторы биосинтеза липидов
- •3.1.8 Ингибиторы образования пластохинона
- •3.1.9 Гербицидные фосфорорганические ингибиторы метаболических превращений
- •3.1.10 Гербициды, нарушающие биосинтез алифатических аминокислот
- •3.2 Гербициды и регуляторы роста растений с фитогормональным механизмом действия
- •3.2.1 Гиббереллины и ингибиторы их образования
- •3.2.2 Синтетические аналоги ауксинов
- •3.2.3 Синтетические аналоги цитокининов
- •3.2.4 Продуценты этилена
- •3.2.5 Другие регуляторы роста и антидоты гербицидов
- •4 Фунгициды
- •5 Инсектициды
- •5.1 Хлорорганические инсектициды
- •5.2 Инсектицидные органические производные кислот фосфора
- •5.3 Карбаматные инсектициды
- •5.4 Пиретрины и пиретроиды
- •5.5 Неоникотиноиды
- •5.6 Ингибиторы биосинтеза хитина
- •5.7 Агонисты ювенильного гормона
- •5.8 Инсектициды с различными механизмами действия
- •5.9 Репелленты и аттрактанты членистоногих
- •5.10 Метод стерильных насекомых
- •Заключение
5.3 Карбаматные инсектициды
Появление устойчивых к действию фосфорорганических соединений рас насекомых вредителей стимулировало исследование близких по механизму токсического действия карбаматных препаратов.
Метилкарбаматная группировка входит в состав высокотоксичного алкалоида физостигмина или эзерина:

Небольшие дозы этого вещества усиливают перистальтику кишечника и усиливают деятельность желез внутренней секреции. Его применяли в качестве противоядия при отравлениях атропином и кураре. Активность физостигмина основана на подобии структуре ацетилхолина, при этом метилкарбаматная группа соответствует ацетатной, а аминные группы связываются в активном центре фермента с анионным центром, предназначенным для связывания с четвертичной аммонийной группой ацетилхолина.
В отличие от органических производных кислот фосфора метил-карбаматы вызывают обратимое ингибирование холинэстеразы. Активность блокированного метилкарбаматами фермента практически полностью восстанавливается через несколько часов после ингибирования. Не исключено также непосредственное действие гидролитически устойчивых эфиров карбаминовой кислоты на рецепторы ацетилхолина. Во всяком случае карбамат холина (карбахол) является агонистом ацетилхолина, связываясь с рецептором на этот нейромедиатор:


В ходе изучения биологической активности, различных производных карбаминовых кислот были получены соединения с инсектицидными свойствами. Практический интерес представляют ариловые эфиры метилкарбаминовой кислоты, продукты взаимодействия гидроксилсодержащих гетероциклов с диметилкарбамоилхлоридом и карбамоилированные оксимы.
Одним из способов получения метилкарбаматов является взаимодействие гидроксипроизводных с метилизоцианатом, который образуется при термическом фосгенировании гидрохлорида метиламина:
![]()
![]()
Равновесие в системе N-метилкарбамоилхлорид/метилизоцианат и хлористый водород практически полностью сдвинуто в сторону образования карбамоилхлорида. Высококипящие изоцианаты легко отделяются от хлористого водорода отдувкой его из реакционной массы инертным газом при нагревании, тогда как метилизоцианат с температурой кипения около 40 °С приходится выделять из карбамоилхлорида с помощью акцепторов хлористого водорода, в роли которых могут выступать оксиды металлов, третичные амины и даже тетраметилмочевина.
Метилизоцианат может быть также получен в результате взаимодействия метилхлорида или метилбромида с цианатом калия в смеси полярного и неполярного растворителя, например, в бензоле, к которому добавлено до 10 % диметилформамида. При более высоком содержании полярного растворителя идёт полимеризация образующегося метилизоцианата. Реакция мептилгалогенидов с цианатом калия ускоряется в присутствии йодидов натрия или калия или же в присутствии безводного хлорида цинка. Известны и другие способы получения метилизоцианата.
Метилизоцианат очень токсичен. В 1984 г. в индийском городе Бхопал на предприятии американской компании Юнион Карбайд в ёмкость с 42 т метилизоцианата стала поступать вода из течи в обратном холодильнике. Экзотермическая реакция метилизоцианата с водой, протекающая с образованием диметилмочевины и диоксида углерода, привела к выбросу всего содержимого ёмкости. Облако испаряющегося метилизоцианата накрыло город, вызвав смерть около 3 тысяч человек. Ещё около 15 тысяч умерли в течение нескольких лет после аварии из-за поражения лёгких.
Кроме взаимодействия гидроксипроизводных с метилизоцианатом, для синтеза метилкарбаматов могут использоваться также реакции метилкарбамоилхлорида с фенолятами и реакции арилхлорформиатов или диарилкарбонатов с метиламином.
Инсектицидными свойствами обладают ариловые эфиры метилкарбаминовой кислоты с электронодонорными заместителями. Эти вещества применяются для борьбы с вредителями риса и в ветеринарии для уничтожения клещей и других эктопаразитов.
Широким спектром инсектицидной действия отличается 2‑изопропоксифенил-N-метилкарбамат – действующее начало таких препаратов, как Байгон, Блатанекс, Агрокарб, Пропоксур, ЛД50 100 мг/кг. Исходным продуктом для его синтеза служит 2-изопропоксифенол. Перевод этого замещенного фенола в карбамат может проходить, например, через хлоркарбонат:

Пропоксур обладает системным действием, но чаще всего он применяется в быту в аэрозольных составах и в приманках для борьбы с мухами, комарами, муравьями и тараканами. В закрытых помещениях пропоксур сохраняет активность в течение нескольких дней, тогда как в полевых условиях он быстро разлагается с образованием безопасных соединений. Сроки применения пропоксура для обработки культурных растений ограничиваются его высокой токсичностью для пчел.
В ряду ариловых эфиров N-метилкарбаминовой кислоты широким спектром биологической активности отличается карбофуран – 2,2‑диметил-2,3-дигидробензофуран-7-илметилкарбамат (Фурадан, ЛД50 8 мг/кг), он является также нематоцидом и акарицидом системного действия. В дозах около 0,5 кг/га карбофуран применяется для уничтожения вредителей на листьях, а в дозах до 16 кг/га в качестве почвенного инсектицида и нематоцида. Даже в таких высоких концентрациях карбофуран не повреждает обрабатываемые растения и стимулирует их рост. К недостаткам карбофурана относят вызываемую им гибель дождевых червей и птиц. Синтез карбофурана начинается с алкилирования пирокатехина металлилхлоридом. Полученный непредельный эфир циклизуется по схеме внутримолекулярного алкилирования в присутствии кислот, а образующееся гидроксильное производное реагирует с метилизоцианатом с образованием карбофурана:


Разрешено применение для обработки наземных частей культурных растений и для борьбы с эктопаразитами инсектоакарициднго α‑нафтилового эфира метилкарбаминовой кислоты (карбарил, Севин, ЛД50 около 140 мг/кг):

Невысокая токсичность для теплокровных позволяет вводить его в состав инсектицидных препаратов для использования в быту и для санитарной обработки скота и домашних животных. Однако в настоящее время производство карбарила сокращено из-за сложившегося после аварии в Бхопале отрицательного к нему отношения.
Высокой биологической активностью отличаются оксимы, замещенные по гидроксильной группе остатком метилкарбаминовой кислоты. Очень токсичен для насекомых и для теплокровных N‑метилкарбамоилоксим 2-метил-2-метилтиопропиональдегида (альдикарб, Темик, Амбич, ЛД50 1 мг/кг). Исходным продуктом для его получения служит изобутен. Он реагирует с нитрозилхлоридом с образованием нитрозотретбутилхлорида, который изомеризуется в оксим хлоризомасляного альдегида. Далее в реакции с метилмеркаптидом натрия это соединение превращается в оксим α-метилмеркаптоизомасляного альдегида, который действием метилизоцианата перводят в альдикарб:
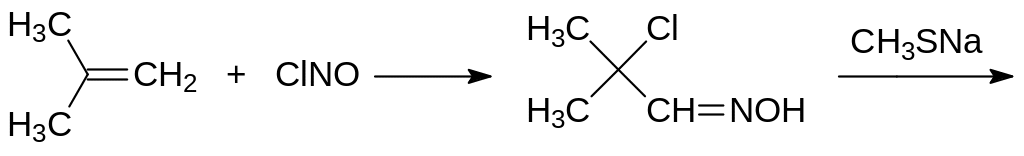

Оксим хлоризомасляного альдегида может быть получен также хлорированием и оксимированием изомасляного альдегида, который образуется в качестве побочного продукта при получении масляного альдегида гидроформилированием пропилена (оксосинтез).
Альдикарб имеет высокую дермальную токсичность (5 мг/кг) и поэтому применяется только в виде гранул в качестве почвенного и системного инсектицида и акарицида.
Компания Дю Понт продолжает производство структурного аналога альдикарба Ланнат (метомил, ЛД50 17 мг/кг, дермально ЛД50 1000 мг/кг). Его получают хлорированием оксима ацетальдегида с последующим замещением атома хлора на метилмеркаптогруппу и взаимодействием образующегося в этой реакции оксима 1-метилмеркаптоуксусного альдегида с метилизоцианатом:


Ланнат - это контактный и системный инсектицид и акарицид широкого спектра действия с нематоцидной активностью.
Ещё одна группа инсектицидов получена в результате модификации природного токсина простого строения, продуцируемого морскими многощетинковыми червями нереидами, нереистоксина:

Исходным соединением для получения структурных аналогов нереистоксина служит 2-аминопропан-1,3-диол, один из способов получения основан на реакции нитрометана с формальдегидом в присутствии триэтиламина и на восстановлении образующегося 2‑нитро-пропан-1,3-диола гидрированием на никеле Ренея:
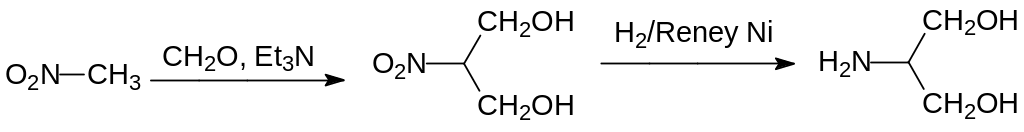
Его метилируют действием смеси формальдегида и муравьиной кислоты (реакция Лейкарта–Валлаха) и замещают гидроксильные группы на атомы хлора действием тионилхлорида:

Образовавшийся в этой реакции 2-диметиламино-1,3-дихлорпропан реагирует с солью бензолтиосерной кислоты с образованием дибензотиосульфоната – контактного и кишечного инсектицида с тривиальным названием бенсултап (Банкол, ЛД50 1100 мг/кг)

Ещё один аналог нереистоксина инсектицид Картап с токсичностью на обезьянах 100-200 мг/кг получают, например, действием роданидов на 2‑диметиламино-1,3-дихлорпропан с последующей гидратацией нитрильной группы в метаноле в присутствии хлористого водорода:

Активность нереистоксина и его синтетических аналогов основана на блокировании холинорецептора, а не холинэстеразы, из-за чего эти биологически активные соединения более безопасны.
