
Тимин биохимия
.pdfОбщпутиологичеокисленияского |
|
|
|
|
|
|
|
90 |
||
|
|
|
|
|
|
|||||
|
|
III КОМ ПЛЕКС . КО Q-ЦИТОХРОМС |
– ОКСИДОРЕДУКТАЗА |
|
|
|||||
|
III комплекс – комплекс цитохромов b-c1,кромецитохромовнемжелезоеются2 |
|
|
|
- |
|||||
серныхбелка. |
|
|
|
|
|
|
|
|
|
|
|
Функция |
|
|
|
|
|
с. |
|
|
|
1Принимает. электро |
|
ныоткоэнзQипередаетинамацитохром |
|
|
|
|
|
|||
2Переносит. |
2иона |
Н+ наружнуюповерхностьвнутреннмитохонде.мбйриальнойаны |
|
|
|
|
|
|||
|
|
IV КОМ ПЛЕКС , ЦИТОХРОМС |
– КИСЛОРОД -ОКСИДОРЕДУКТАЗА |
|
|
|||||
|
IV комплекс – цитохромы аа3 или цитохромоксидаза, содержит 2ионамеди. |
|
|
|||||||
|
Функция |
|
с ипередаетихнакисобразованиемлорводы. |
|
|
|
|
|||
1Принимает. электротцитохроманы |
|
|
|
|
|
|||||
2Переносит. |
4иона |
Н+ наружнуюповерхностьвнутреннмитохонде.мбйриальнойаны |
|
|
|
|
|
|||
|
|
|
|
V КОМ ПЛЕКС |
|
|
|
|
||
|
V комплекс – этофермент |
АТФ-синтаза,состоящийиз |
множества белковыхцепей, |
|
||||||
подразделенныхна |
двебольшиегруппы:Однагруппаформирует |
|
|
|
субъединицуоF |
(произн о- |
||||
ситсясозвуком"ане, ноль""т. |
|
|
олигомицин-чувствительная) |
– еефункцияканалообр |
|
а- |
||||
зующая,понейвыкачанныенаружупротоныводородастремляютсямат.Д иксугая |
|
|
|
|
|
|
|
|||
группаобразует |
субъединицуF |
1 – еефункцкаталитическая, менноона,используяэне |
|
|
|
р- |
||||
гиюпротонов,синтезируетАТФ. |
|
|
о прохождение приблизительно 3-х ионов Н+, |
|||||||
|
Длясинтезамолекулы1 АТФнеобходим |
|
||||||||
ещеодинпротонтребуетсядляперч мембрануносарезнеорганфосфата,АТФического |
|
|
|
H+. |
|
|
||||
АДФ.Такимобразом,дляполученияАТФизАДФвцеломтребуетсяиона4 |
|
|
|
|
|
|
||||
|
|
Р А БКОТМДАПЫЛХЕ К С О В |
|
А Т ЕЦЛЕЬПНИО Й |
|
|
||||
|
Наоснованвышепоиизложстрохемаенаного |
|
|
окислительногофосфорилиров |
|
а- |
||||
ния: |
|
|
|
|
строгоопредепоследователнной |
|
ь- |
|||
|
1Ферменрасположены. дыхацепительнойв |
|
|
|
||||||
ности: каждыйпослбеобладаетдующийлокбольшимсродствомкэлект,чемп едонам |
|
|
|
|
|
ы- |
||||
дущийон(боэлеек |
|
троположит,.е.обладаболеположеоктленислительнотельным |
|
|
|
|
- |
|||
восстановитпотенциалом)Этообеспечи. одль онаправленноеымд ижениеаетэлектр |
|
|
|
|
|
о- |
||||
нов. |
|
|
|
|
|
|
|
|
|
|
|
Способностьокислительно |
-восстановительнойпарыобратимоотдаваэлек рон |
|
|
|
|
|
|||
|
выражаютокислительно |
-восстановительнымпотенциаломЕ |
|
0'.Вбиохимиипр |
и- |
|
||||
|
нятопользоватьсяпонятием |
|
восстановительныйпотенциал |
|
.Чем ботрицлее |
а- |
|
|||
|
тельной величинойвыражаетсявосстановительныйпотенциалсистемы, |
|
|
|
|
выше |
|
|||
|
ее способность отдавать элект.Присравнениионывосстановительногопотенц |
|
|
и- |
|
|||||
|
алапНАДНры |
/ НАД = -0,32 ВипарыН |
2О / 1/2О2 = +0,82 Ввидно,чтоэлектр |
о- |
|
|||||
|
ныбудутпереходитькво.Вдействительностимеждуназвадо нымиором |
|
|
|
|
|
|
|||
|
акцепторомэлектронимеетсямногопр межуточныхвсое |
|
|
динений. |
|
|
||||
|
2Все.атомыводорода,отщепленныедегидрогсубстваэнруслобныхатовзами |
|
НАДН или ФАДН2. |
о- |
||||||
виях, достигаютвнутреннеймембраныитохондрийсоставе |
|
|
|
|||||||
|
3Здесь. |
атомыводородаот(НАДНиФАДН |
|
2) передаютсвои |
|
электроны вдыхател |
ь- |
|||
нуюферментативну юцепь,покоторойэлектроныдвижутся |
|
(50-200 шт/ сек) ксвоемуконе |
ч- |
|||||||
номуакцептору |
– кислороду.Врезультатеобразу тся |
|
вода. |
|
|
|
|
|||
|
4Поступающие. вдыхательнуюцепь |
|
электрбогатысв эбоднойыергией |
|
|
.Пом |
е- |
|||
ре их продвиженияпоцепионтеряютэнерг.Этаэнергияспользуетсяю |
|
|
|
I, III, IV комплек- |
||||||
самидыхатефермепльяремещенияыхтов |
|
ионов водорода черезмембрану |
вмежме |
м- |
||||||
бранноепространство. |
|
|
|
|
|
|
|
|
||

biokhimija.ru |
ТиминО.А. |
Лекции по общей биохимии (2018г) |
91 |
|
|
|
|
|
|
|
Какизвестфизики,энергиейназываоспособностьсовершатьтсяла |
|
работу. |
|
|
|
|||
|
Приперемещеэлектричесзаряданэлектрииергияубываетогоичастичнонов |
|
|
|
|
превтеплотуращается. |
|
|
|
|
Другаячастьэнергиизатрачинавыкачиванодородааетсяизматриекса |
|
|
|
|
межмембтранствооепроисоздгр .диента |
|
|
|
|
|
|
|
|
5. Перенос ионов водорода черезмембранув( |
ыкачивание) происходитнеслучайно,в |
|||
строгоопределенныхучасткахмембр.Этиназсткинываются |
|
|
участкисопряжения |
|
(или,несовсемточно,пунктыфосфорилирования). |
|
Онипредставлены |
I, III, IV комплексами |
|
дыхательферме. ныхтов |
Врезультатеработыэтихкомплексовформируградиенттся |
|
ионов |
|
водородамеждувнутренннаружнойи поввнутреннейрхностямимитохондриальной |
|
|
|
|
мембраны.Такой |
градиентобладает |
потеэнергиейциальной. |
|
|
Градиентполучилназвание |
электрохимический или протонный градиент (Δµ, "дел ь- |
|||
тамю")Онимесоставляющие. две |
– электрическую( |
ΔΨ,дельта"пси")концентрацио |
н- |
|
ную ( рН): |
|
Δµ = ΔΨ+ рН |
|
|
|
|
|
|
|
6Прото. теряютсвоюэны,прчерезгиюоходя |
|
АТФ-синтазу. Частьэтойэнергии |
|
|
тратитсяна |
синтезАТФ |
. |
|
|
Такжекакв |
случаеэлектр,энергияонводородаамиовпрото( градиента) ного |
|
|
|
|
расхпо.Двигапдупосеэлектрохимическомуусясьградиенту,ионыводородавыделяют |
синтезАТФ |
|
|
|
|
энерг,частькоториспю наользуетсяй |
|
. |
|
|
|
Р Е Г У Л Я Ц И Я О К И СФЛОИСТФЕ ЛОЬ Н О Г О |
Р И Л И Р О В А Н И Я |
|
|||
Работадыхфетельрмеегулируетсянпомощьюыхтовэффекта,кот рыйлучил |
|
|
|
|
|
названиедыхательныйконтроль. |
|
|
|
|
|
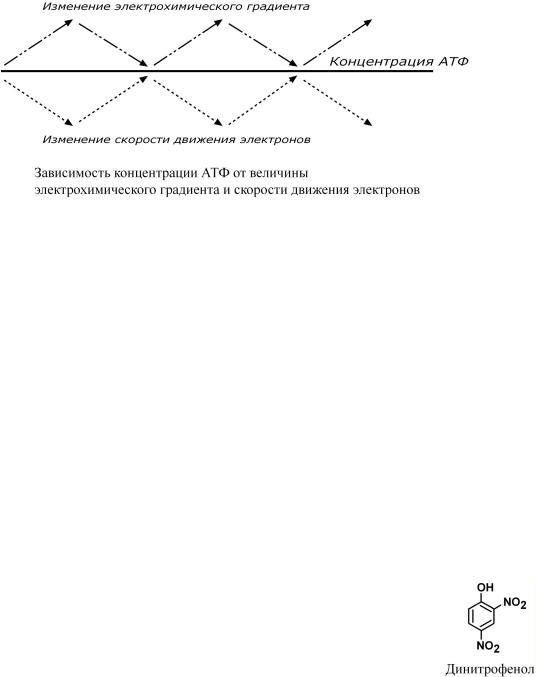
Дыхательныйконтроль |
– этопрямоевлияние |
электрохимическогоградиента |
на |
||
скоростьдвиженияэлектроновподыхательнойцепи |
|
(величидыхания) у |
. Всвоюочередь, |
|
|
Общпутиологичеокисленияского |
|
|
|
|
|
|
92 |
|
|
|
|
|
|
||||
величинаградиента |
|
напрямую завиотсоотношенияитАТФАДФ,количественнаясумма |
|
|
||||
которыхвклеткепостоянна( |
|
|
[АТФ] + [АДФ] = const). |
|
|
|
||
Возрастание протонногоградиента |
возникаетприисчерпаниизапасовАДФнако |
+ непроникаютвма |
п- |
|||||
ленииАТФ,т..когдаАТФ |
|
|
-синтазалишенасвоегосубстратаионыН |
|
т- |
|||
риксмитохондрии. |
Приэтом |
нгибирующеевлияние |
градиента усиливается ипродвижение |
|||||
электроновпоцепизамедляется. |
|
|
|
Ферментныекомплексыостаютввосстановленномя |
|
о- |
||
стоянии. |
Следствиемявляетсяум |
|
|
еньшениеокисленияНАДНФАДН |
|
2 на I и II комплексах и |
||
замедлениекатаболизмавклетке |
|
|
|
. |
|
|
|
|
Снижение протонногоградиента |
|
возникает, нап, ример риинтенсивнойработем |
ы- |
||||
шечной илиинойклетки,когда |
количествоАТФ |
ней начинает уменьшаться.Вэтомслучае |
|
||||
АТФ-синачинаеттазараб, оНтатьны |
|
|
+ чернеез |
устремляютсявматрикс |
, ивеличина |
||
электрохимичградиентаснижа тсяского |
|
|
.В результате повышается выкачиваниеионовН |
+ |
|||
|
|
|
|||||
ферментамидыхательнойцепи |
вмежмембпространстное |
|
во. Ферментные комплексы I и |
||||
II усилокислениевают |
НАДНиФАДН |
|
2 (какисточников |
электронов) и снимаетсяингиб |
и- |
||
рующеевлиянНАДНнацлимоннойклекислоты |
|
|
|
|
пируватдегидрогеназныйкомплекс |
– |
|
активируютсяреакци |
икатаболуглеводовижировзма |
|
|
|
. |
|
|
Такимобразом, |
количествоАТФ |
остнается |
постоянном уровне. |
|
|||
|
|
|
|
||||
|
Р А З О Б Щ И Т Е Л И |
|
|
||||
Разобщители – этовещества,которые |
|
снижают величинуэлектрохимическогоград |
и- |
||||
ен,чпритаокувелодскоростидвижениячениюэлектроновпофермендыхательнойам |
|
|
|
|
|
|
|
цепи.ВрезультатеэтогоуменьшаетсясинтезАТФво карастает |
|
|
|
таболизм. |
|
||
Таккакэлектрохградсостоитдвухмическийзкомпонентовэлектрического( |
|
|
|
|
|
|
|
химического),тосуществуютдвапринципиалспособаегоуменьныхшить |
|
|
|
|
– нивелировать |
||
разностьарядовилиразностьконцеиоводородантрацииов. |
|
|
|
протонофоры" |
|
|
|
Кразобщителямв |
первуюочередьотносят" |
|
|
– |
|
||
вещества, перенионыв .сящиедорПриэтумомдаобаньшаются |
|
|
|
|
|
|
|
компонентаэлектрохимическогоградиента |
|
(pH изаряд) |
.Классическим |
|
|||
протонофоромявляется |
динитрофенол,жирорастворимоесоединение, |
|
|
||||
присоединяющиеионыводо |
роданавнешнейповерхностивнутренней |
|
|
|
|
||
митохондмемботдрихнавнутреннейныающиельнойповерхн |
|
|
|
|
о- |
|
|
сти.Протоодновременнофоры |
снижают электрическуюхимич |
е- |
|
||||
скуюсоставляющую |
протонного градиента,энергиякоторогора |
ссеи- |
|
||||
ваевидетсяепла. |
|
|
|
|
|
|
|
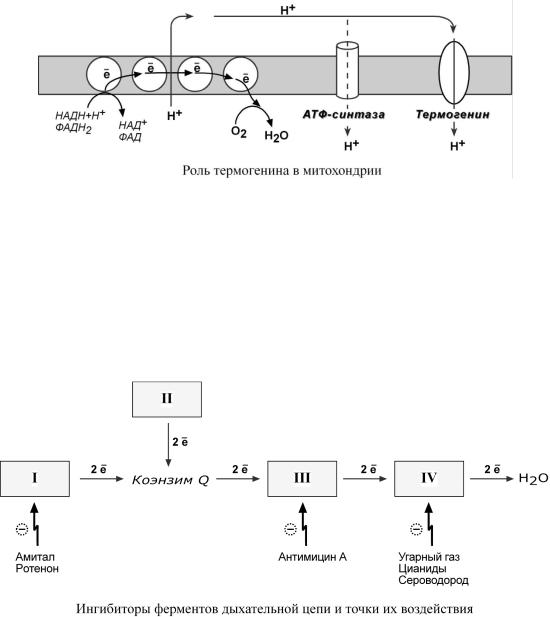
Физиологическим протонофоромявляетсябелок" |
|
|
термогенин",визобилиииме |
ю- |
|||
щийсявклеткахбуройжировойтканидо(15%отвсбемитохондрийлков)Существенным. |
|
|
|
|
митохондрий,кот о- |
||
отличбуройжитканиемотбелойвойявляетсябольшоеколичество |
|
|
|
|
|||
biokhimija.ru |
|
ТиминО.А. |
Лекции по общей биохимии (2018г) |
|
93 |
||
|
|
|
|
|
|
||
рыепридаюткл |
еткамбуро |
-красныйцвет.Приохлажденииорганизмаэтиклеткиполучают |
|
липолиз. |
|||
сигналыпосимпатическимнервам, нихактивируетсярасщеплениежира |
|
|
|
– |
|||
ОкислениежипровполучениюодНАДНФАДНт |
|
|
2,активизацииработыдыхательной |
и- |
|||
цепивозрастаниюэле |
ктрохимград.ОднакоиАТФческогоента |
-синтазывмембранах |
|||||
тохондрийэтихклетокмало,затомного |
|
|
|
термогенина.Благодаряему,б |
ольшаячастьэне |
р- |
|
гиионовводородарассеивавидетепла,об поддержаниетсяспечиваятемпературытела |
|
|
|
|
|||
приохлаждении. |
|
|
|
|
|
|
|
|
Бураяжи |
ровткшиаяньпрокоедствверхнейчастиспивлеуживотных,а |
|
|
|
||
|
впадающихзимнийсонме( ),удетенышейведиж |
|
|
вотныхичеловеческихмл |
а- |
||
|
денцев.О |
тдельныескоплбурыхжировыхклетния |
|
окестьиувзрослогочеловека, |
|
|
|
|
онирасположвверхнчастиспи,ейны |
|
|
междуло,пмышкамиодаток,походу |
|
|
|
|
крупныхкровеносныхсосудов. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кромединитермогенинаофенола |
протонофорами,кпримеру,являютсясалицил |
а- |
ты,жирныекислотытрийодтиронин. |
|
|
|
|
|
И Н ГФИЕБРИМТ ЕОНРТЫО В |
Д Ы ХЦАЕТПЕИЛ Ь Н О Й |
|
|
|
|
Рядвеществможетингибироватьферме |
нтыд хательнойцепиблокироватьдвижение |
|
элекотНАДНироновФАДН |
2 накислород. |
|
|
Выделяюттриосновгруппыингибиторовых: |
амитал (успокаивающееснотворносре |
|
||
o |
действующиена |
I комплекс,например, |
д- |
||
|
ство), ротенон (пестшиспектрарокогоцид |
), |
|
|
|
o |
действующиена |
III комплекс,например, |
антимицинА |
(антигрибковый пестицид) |
, |
Общпутиологичеокисленияского |
|
|
|
|
|
|
94 |
|||
|
|
|
|
|
|
|||||
o |
|
действующиена |
IV комплекс,например, |
сероводород (H2S), угарныйгаз |
(СО), циа- |
|||||
|
ниды (-CN). |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
К О ЭРФ/ОФ И Ц И Е Н Т |
|
|
|||
|
Энергетическуюценностьвыгодность |
|
|
окислениявеществаможноподсчитать. |
|
Коли- |
||||
чествозапасенной |
энепокригитогосленииинлиогоединенияхарактеризует |
|
|
|
количе- |
|||||
ствоАТФ |
, аэффективност |
ь использования энергиивещзахватаства |
– коэффициент |
|||||||
P/O. |
|
|
|
|
|
|
неорганическогофосфата |
|
|
|
|
КоэффициентР/О |
– этоотношениеколичества |
|
,включенн о- |
||||||
говмолекулуАТФ |
АТФ-синтазой кколичестатомову |
кислорода,включенногомолек |
у- |
|||||||
луН |
2О,припереносе |
|
однойпарыэлектронов |
|
подыхательнойцепи. |
кисления веществ. |
||||
|
Внастоящеевремяимеется |
|
дветочкизрения |
|
наэффективность |
|||||
Попервойверсии, |
в реакциях сучастием НАД-зависимыхдегидрогеназсоотношение |
|
P/O |
|||||||
соответствует 3,0,п оболее |
современнымданным |
|
этот коэффициентдляНАДНравен |
|
2,5. |
|||||
Анадлогичноя |
ФАД-зависимыхдегидрогеназкоэффициентP/O |
|
либо принимается 2,0,либо |
|||||||
посовременнымданным |
|
равен 1,5. |
|
|
|
|
|
|||
|
ДлярасчетаР/Оприокислениикакой |
|
|
-либомолнеобходимокулызнать: |
|
|
||||
o |
|
восстаноэквимо( валенкулнтый |
|
|
а НАДН или ФАДН2)передаетвцепьперен |
о- |
||||
|
саэлектроновпо |
|
2электрона . |
|
|
|
|
|
||
o |
|
длявосстановления |
кислорода в воду необходимапараэлектронов1 |
, |
|
|||||
o |
|
припрохождпарыэлектч ниирезонов |
|
|
|
всю дыхацепьт..(ельную |
через I, III, IV |
|||
|
комплексы)выкачиваетсястолько |
ионовН |
+,скольконеобходимодлясинтеза |
|
2,5 молей |
|||||
|
АТФ. |
|
только через III и IV комплексыдыхательных |
|
o |
припрохождениипарыэлектронов |
+ |
||
|
ферментов ионовН |
выкачиваетдлястолько,скольконе бходимоинтеза |
1,5 молей |
|
|
АТФ. |
|
|
|
Далее прасчиэнергтахценноокислениятичвеществтиской |
|
|
|
будет использоваться |
|||||
величина P/O дляНАДНравн |
|
ая 2,5,дляФАДН |
2 равная 1,5. |
|
|
|
|||
|
|
|
|
||||||
|
Г И П О ЭСН Е Р Г Е Т И Ч Е С К И Е О С Т О Я Н И Я |
|
|
||||||
|
|
|
|
|
|
|
|||
|
Причинамиг |
ипоэнергетическихсостм яний |
жет бытьследующ |
ее: |
|
|
|||
o |
гиповитаминозы экзогенныеи/илиэндогенные |
– снижаетскороэффектисять |
|
в- |
|||||
|
ностькислительреакций.Возникаетобычнопринеыхватке |
|
|
|
|
витаминов группыВ |
– |
||
o |
В1,В 2,никотиновойки |
слоты,В |
6,пантотеновой кислоты иаскорбиновойкислоты. |
|
|
||||
дефицит белка впище |
– снижасинтвсехфтсярментовзи |
|
ферментов катаболизма, |
||||||
|
вчастности. |
|
|
|
|
|
|
|
|
o |
снижение потребления углеводов и липидов какосновныхисточниковэнергии. |
|
|
||||||
o |
дефицит кислорода – отсутствиеакцепторадляэлектронов |
|
вызываетпереполнение" " |
|
|
||||
|
дыхательферме,повышениеэлектрохимическогоыхтовградиента,накоплениеНАДН |
|
|
|
|
|
|||
o |
иФАДН 2 вклеткеипре атаболращен. иезма |
|
|
|
меди – |
||||
дефицит железа – компонента цитохро,миоглобинагемоглобина, в |
|
||||||||
компонентацитохромоксидазы.

biokhimija.ru |
ТиминО.А. |
Лекции по общей биохимии (2018г) |
95 |
|
|
|
|
|
|
|
|
ИС П О Л Ь З ОАВТФАН И Е
ИЕПГОРЕ Д Ш Е С Т В Е Н Н И К О В ВМ Е Д И Ц И Н Е
1Внутримышечные. инъекции |
раствора АТФ используют примышечндистройфии |
и |
||||
атрофии,спазмепериферическихсосудовбол( Р,облитерирующийзньотромбоанг |
|
|
иит), |
|||
длястимулирродеятельностиовой. вания |
|
|
|
|
|
|
2. Фосфаден – |
лекарственноеназваниеАМФ. |
|
Особенностьюпрепараявляеего ася |
|
|
|
сосудорасширяющийэффектспособносулучшатьпериферическое |
|
|
кровообращение. |
|||
Фосфаденприменяютсвинцотра, стройвперемежающейсяомлениипорфирии, |
|
|
|
сосу- |
||
дистыхнарушениях |
шемической болезни сердца,болпе.зняхчени |
|
|
|||
3. Рибоксин или Инозин являетсянепосредственнымшественникомАТФ |
|
.Инозин |
||||
споспробен |
никатьвклеткиповышатьихэнергетическийбаланс.Имеютсяданныеосп |
|
|
о- |
||
собностипрепаратаповыш |
|
аактивностьферментов |
ЦТК,стимулироватьсинтезнуклеот |
|
и- |
|
довиулучшатькоронарноекровообращение.

ОБМЕН АМИНОКИСЛОТ И БЕЛКОВ
А З ОБТАИЛСАТНЫСЙ
|
Вовсехклеткоргпостояннозмаахидутпроцессы |
|
анаболизма икатаболизма .Также |
||||||
какилюбыедругиемол,б молекулылковыеорганизменепрерывнораспадаются |
самообновлениябелков |
|
|
|
|
||||
синт,.е.идетзируютпроцесся |
|
.Вздоровомганизмемужчины |
|
|
|||||
массой70кгвеличинаскоростира оответствуетпадаскорости |
|
|
синтезаравна500гбелка |
|
|
||||
всутки. |
|
|
|
|
|
азотистыйбаланс |
|
|
|
|
Ескоростьлисинтезабелковравнаскоихраспадаости,наступает |
|
|
|
, |
||||
или, подруг,этсостоян,мукогдаколвыводимчествоазотаравнк личествуполго |
|
|
|
|
у- |
||||
чаемого( |
Vпоступ = Vвывод). |
|
|
|
|
|
|||
|
Есинтезлибелков |
превышаетскоихраспадаость,токоличествовыводимогоазота |
|
|
|
|
|||
сниразностьжаетсямеждупоступающазотомивыводимым( |
|
|
Vпоступ – Vвывод) становит- |
||||||
сяположительной.Вэтомслучаеговорят |
|
положительном азотистомбалансе.Полож |
|
и- |
|||||
тельныйазотистыйбаланснаб |
людаетсяуздоровыхдетей, |
принормальнойбеременности, |
|
|
|||||
выздоравливбольных,спортсмприафбющихор,те..новтмыехслучаях,когдаус |
|
|
|
|
|
и- |
|||
ливаесинструктурныхсяезифункциональныхбелковклетках. |
|
|
отрицательный азотистыйб |
|
|||||
|
Привозрастдоливыводимогоазотанаблюдаетсяии |
|
а- |
||||||
ланс.Отрицательныйбалансотмечаетсяубольныхголодающих. |
|
|
менее42г |
пол- |
|||||
|
Всемирнаяорганизацияздравоохрекомеп ианимаениядуеть |
|
|
||||||
ноценного белка всутки |
– это физиологическийминимум |
.Тольковэтомслучаеворг |
|
|
а- |
||||
низменаст |
|
упаетазобалансистый. |
|
|
|
|
|
|
|
|
Вреальностинормыпотрб устлкаблеан,исходяавливаютсяияизпредставленийо |
|
|
|
|
||||
белковомсоставепищпросоотнош,выхдуктполвинеоценполниибеноценных |
|
|
|
|
л- |
||||
коврационе. |
В Россиинормы |
суточного поступления пищевого белка для взрослых уста- |
|||||||
новленынауровне |
100-120г ,длядетейгода1жизни |
– 2-3 гнакгвеса |
тела,устарших |
|
де- |
||||
тей – около 1,5-2г/кгвеса |
. Животнбелковдолжноыменеетьх60%общеготколич |
|
|
|
е- |
||||
ства. |
Основнойтрудностьюп асчетеинормативовпотрбеявлковбразнооенияяется |
|
|
|
|
б- |
|||
|
|
|
|
|
|||||
разиеихаминсоставакислотнеодинаковпотребностьоргразныханизмаминя |
|
|
|
|
о- |
||||
кислотах. |
|
Всвязиэт м |
введеныкритериикачб:ствалка |
|
|
|
|
||
o |
соотношение заменимыхнез инокислотимых |
– вбелкедолжнобытьнем |
|
е- |
|||||
|
нее32%незамеинокислот, имых |
|
|
|
|
|
|
||
o |
близость аминсоставакислотногобелк |
аминокислотномусоставуусредненного |
|
|
|
||||
|
белка телачеловека, |
|
|
|
|
|
|
||
o |
легкость перевариванияЖКТ |
. |
|
|
|
|
|||
|
Строениенекоторыхбелковсн |
|
ижаетилидажесключаетихусвоеннапример: , |
|
|
|
|||
|
плохоперевариваетсяколлаген,кератбелок( волосшерстин)вообщенегидр |
|
|
о- |
|
|
|||
|
лизуетсявЖКТ,таккаксодержиточедисульфидныхмного( |
|
S-S)связей,для |
|
|
||||
|
расщеплениякоторыхуживонетферментов.ных |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
Существуетпоняоптиповсеммальногопараметрам |
идеальногобелка |
, кнему |
|
наиболееблизокбелоккуриногояйца. |
|
Растительныебелкисчитаюнеполноценными, акся |
|
каквихсоставемалонезамеинокислот, имых |
итакже долятехилииныхаминокислотв |
|
|
растительномбел |
керезкоотличается |
таковой животногобелка . |
|
biokhimija.ru |
|
|
ТиминО.А. |
|
Лекции по общей биохимии (2018г) |
97 |
|||||
|
|
|
|
|
|
|
|
||||
|
Такмикнеобходимыокислотывопределеннсоо,твозникаетшениим |
|
|
|
|
|
я- |
||||
тие" |
лимитаминокислотырующей |
|
",т.е.поступающейвминимальномнедостаточном |
|
|
||||||
количестве. |
Отсутствие этойаминокпрепятствуетиспользоваслвключе(ты нию |
|
|
|
о- |
||||||
ставбелка)других |
|
аминокислот,котможетбытьрыхдостаточно. |
|
|
|
|
|||||
|
Принедостбелкавпищезадерживаетсяткерост |
|
|
|
удетей ,отстает физическое |
ум- |
|||||
ственноеразвитие,изменяесоставкосткани, нойся |
|
|
|
|
|
нижается актиммуннойвность |
и- |
||||
стемыи |
сопротивкзаболяемостьеваниям |
|
,тормозится |
деятельность эндокринныхжелез. |
|
||||||
Выраженным арушениемпотрб явлковбенияяется |
|
|
|
квашиоркор – нехваткабелков, |
|
||||||
особенножи,впищеотных.Врезультвозникаетдисбалансте |
|
|
|
|
|
минокислотногосостава |
|
||||
пинедостатокщинезаминокислот.Заболеваниеимыхнаиболеарактернодляслаб |
|
|
|
|
|
о- |
|||||
развитых странАзииАфрики |
иегоначалосовпадаетотнятиемребенкагрудиматери |
|
|
|
|
||||||
(1,5-3годика), онлишаетсягдаполноценнбелкапереходго |
|
|
|
|
итнаскудноерастительное |
|
|||||
питаниевзрос.Убонаблюдаетьныхистоще,остароста,отечностьовкаяие, немия, |
|
|
|
|
|
|
|||||
нарушинтипамятиеллекние,умсотсталвенная,гипопротеинемиястьаминоацидурия. |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
||||||
|
В НОЕ БШАМИНЕ НЙН О К |
|
|
И СИБЛЕОЛТК О В |
|
||||||
|
Переварибелкование |
начинаетсявжелудке,продвенолжадцатиперстнойется |
|
|
|||||||
киштонкомишечнике.Распадбелковаминпроисходитьжеткислтакжевто |
|
|
|
|
|
л- |
|||||
стомкишечнвлияниемпод ик. рофлоры |
|
|
|
|
|
экзопепти- |
|||||
|
Протеолитическиеферментыподразделяютособенностиихдействияна |
|
|
|
|
||||||
дазы,отщепляющиеконцевыеаминокислоты, |
|
эндопептидазы,действнавнутреющие |
н- |
||||||||
ниепептидныесвязи. |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
Ж Е Л У Д О К |
|
|
|
|
|
Вжелудкепищаподвоздейергаетсяжелудочного,твиюка чающего |
|
|
|
|
соляную |
|||||
кислоту иферменты.Кферментамжелуотносятсядвегруппыкапротеа |
|
|
|
|
зсразнымоптим |
у- |
|||||
момрН,котоупрназываютыеощенно |
реннин. |
|
пепсин и гастриксин.Угрудныхдетейосновным |
|
|||||||
ферментомявляется |
|
|
|
|
|
|
|
||||
|
|
|
|
РЕ Г УЖЛЕЛУДОЧНОГОЯ Ц И Я |
ПИЩ ЕВАРЕНИЯ |
|
|||||
|
Осуществляется нервными (безусловныеи рефлексы)и |
|
|
гуморальными ме- |
|||||||
ханизмами. |
|
|
|
|
|
|
|
гастрин и гистамин. |
|
||
|
Кгумораль нымрегуляторамжелудочнойсекрецииотносятся |
|
|
|
|
||||||
|
Гастрин выделяетсяспецифичными |
|
G-клетками: |
|
|
|
|||||
o |
|
вответнараздражение |
механорецепторов, |
|
|
|
|
||||
o |
|
вответнараздражениехеморецпродукты( первичногоптогидбелковро) лиза |
|
|
|
|
|
, |
|||
o |
|
подвлиянием |
n.vagus. |
|
|
|
|
|
|
||
|
Гастрин стимулирует главные,обкладочнидобавочнкле,чтоыкисекрзывает |
|
|
|
е- |
||||||
циюжелудочногосока |
|
,вбольшеймересолянойкислоты.Такжегастринобеспечивает |
|
|
|
сек- |
|||||
рециюгистамина. |
|
|
|
|
|
|
|
|
|
||
|
Гистамин, образующийсяв |
энтерохромаффиноподобныхклетках( |
ECL-клетки, |
при- |
|||||||
надлефунджелезам)т ьным |
|
|
|
слизистойоболочкижелудка, |
|
|
взаимодействует с |
||||
Н2-рецептораминаобкладочныхклеткахжелудка,увеличиваетх |
|
|
|
|
синтезвыделение |
о- |
|||||
лянойкислоты. |
|
|
|
|
|
|
|
|
|
||
|
Закисжелсодержимогоудочногоениеподавляетактивность |
|
|
|
|
G-клетокипомеханизму |
|
||||
обратнойотрицательнойсвязиснижасекрецию |
|
|
гастрина желудочногосока. |
|
|||||||

Обамениибелковокислот |
|
|
|
98 |
|
|
|
|
|
|
|
|
|
|
Солянаякислота |
|
|
|
Однимизкомпонентовжелудочногосокаявляется |
|
соляная кислота. Вобразовании |
||
солянойкислотыпринимаютучастие |
+ ипереносящиеионы |
париетальные (обкладочные) клетки желудка,обр |
а- |
||
зующиеионыН |
Сl– изкровиполостьжелудка. |
|
|||
|
Фунсолянойкции |
слоты |
|
|
|
o |
денатурация белковпищи |
, |
|
|
|
o |
высвобжелезаизкомпждениесбелпереексакамиеговдводухвалентнуюфо |
|
р- |
||
|
му,чт онеобхдляегвсасыванияодимо. |
|
Аналогично высвобождаютсяидругиемета |
л- |
|
|
лы, |
|
|
|
|
o |
высвобождениеразличорганичмолекулых,прочносвязазнныхскихбелковойч |
|
а- |
||
|
стьюгем(,коферменты |
- тиаминдифосфат,ФАД,ФМН,кобаламин,био),чп зв |
о- |
||
|
ляет им впоследствиивсасываться, |
|
|
|
|
|
o |
бактерицидноедействие, |
|
|
|
|
|
o |
превращение неактивногопепсиногена |
|
вактивныйпепсин |
, |
|
|
o |
снирНжелудочногониесодержимого1,5 |
|
|
-2,5 и созданиеоптимумарНдляраб |
о- |
|
|
тыпепсина, |
|
|
|
|
|
o |
послепереходав12 |
-перстнуюкишку |
– стимулясекрецияи |
кишечныхгормонов, |
|
|
|
следовательно,панкреатического |
|
сокаижелчи |
. |
|
|
|
Совокупностьвсехжщелудочнствсока,способныхбытьгонорамипрот |
|
|
|
|
о- |
||
|
нов,составляют |
|
общуюкислотность |
.Солянуюки,связаннуюлотусбелками |
|
|
||
|
продуктамиихпереваривания,называют |
|
связанной солянойкислотой,анаход |
я- |
||||
|
щуювнесвязанно |
мвиде |
- свободной солянойкислотой. |
|
|
|||
|
|
|
|
|
Пепсин |
|
|
|
|
Пепсин – эндопептидаза,тоестьрасщепляет |
внутренние пептидныесвязимолекулах |
|
|||||
белковипептидов |
. |
главных клетках желуввинеактивногодкапрофермента |
|
пепсино- |
||||
|
Синтезируетсяв |
|
||||||
гена,вкоторомактивныйцентр |
|
|
"прикрыт" |
N-концевымфрагментом |
. Приналичии |
соляной |
||
кислоты конформацияпепсиногенаизментакимобразом,чтораскрывается" "активный |
|
|
|
|
||||
центрфермента,которыйотщепляет |
|
|
остаточныйпептид |
(N-концевойфрагмент |
),блокир у- |
|||
ющийрабофермента,..происходу |
|
|
ит аутокатализ. Врезультатеобразуактивныйтся |
|
||||
пепсин,активирующдругиемолп псиногенакулый |
|
|
. |
|
|
|||

biokhimija.ru |
ТиминО.А. |
Лекции по общей биохимии (2018г) |
99 |
|
|
|
|
ОптимумрНдляпепсина1,5 -2,0Пепсин.гидролизуетпептидныесвязи,образованные аминогруппами ароматических аминокислот (тирозина, фенилаланина, триптофана),и значительнохуже,карбокси - иаминогруппами лейцина,глутаминовойкислотыпр.
|
|
|
Гастриксин |
|
|
Гастриксинпосвоимфункциям |
|
близокпепсину,еголичествожелудочномсоке |
|
|
|
составляет20 |
-50%отколичествапепсин. |
Синтезируетсяглавнымиклеткамижелудка |
|
и- |
|
депроферментаиактивируетсясолянойкислотой. |
|
ОптимумрН |
гастриксина соответствует |
||
3,2-3,5 и значениеэтотфермприеетитнтмолочноании |
|
-растпищей,слабтельной |
ее |
||
стимулирующейвыдесокислотыяниеой |
|
одновременнонейтрализующейеепросвете |
|
||
желудка.Гастриксин |
является |
эндопептидазой игидролизует |
связи, образованные |
кар- |
|
боксильнымигруппами |
|
дикарбоновых аминокислот. |
|
|
|
