
Тимин биохимия
.pdf
Строениеобменуглеводов |
190 |
|
|
Патогенез. |
Избытокгалактозыпревспиртращается |
галактитол (дульцитол),нака |
п- |
||
ливающийсяхрусталикеосмотпр влесюдачесводу.Изменякиющий |
|
|
етсолевойяс |
о- |
|
став, нарушаетсяконформация |
белков хрусталика,чтоприводиткатмолодомрактево |
|
|
з- |
|
расте.Катарактавозможнадажеуплодовматерей |
,котбольнырые |
галактоземией и упо- |
|||
треблявших молокововремябеременности. |
|
|
|
|
|
|
|
Придефектегалактозо |
-1-фосфат-уридилтрансферазы АТФпостояннорасходуетсяна |
|
|
||||
фосфоргалактозыдефицитлированэнергиие |
|
|
угнетает активность многихферментов |
, |
|||
"токсически" действуя на всеклетки,особеннона |
нейроны,гепа |
тоциты,нефроциты |
.Какр |
е- |
|||
зультат, возможнызадержкапсихомотразвитиятсталостьнекроз,умственнаяо , геп |
|
|
|
|
|
а- |
|
тоципеченитоврроз.Впочкахшечнизбытокгалаееметозытаболитовинг |
|
|
|
|
|
и- |
|
бирует всасывание аминокислот. |
|
|
|
|
|
|
|
Основылечения |
. Исключениеизрационамолокадругихисточникгалактпо озыв |
|
|
|
|
з- |
|
воляетпредотразпатологичесвитиератсимптть.Однахранностьмовинтеллектаих |
|
|
|
|
|
|
|
можетбытьдостигнутатолькопр , позднпервыхнейм2 жизнисяцев,диагнос |
|
|
|
|
|
тике |
|
ивовремяначатомлечении. |
|
|
|
|
|
|
|
|
П Р Е ВФРРАУЩКЕ Н И Е |
Т О З Ы ВГ Л Ю К О З У |
|
|
|||
Реакциипереходафруктвглюкозузыстаточнопросты.Сначпроисходитлакт |
|
|
|
|
|
и- |
|
вацияфруктозыпосредствомфосфорилирования |
|
: 6-го атомауглерода |
припомощи |
гексоки- |
|||
назы или 1-го атомауглеродапри |
участии фруктокиназы. Приэтомг |
ексокиназаимеетг |
|
о- |
|||
раздоболеенизкоесродствофруктозе.Фруктозо |
|
-6-фосфатдалее |
|
изомеризуетсяи |
глюкозо- |
||
6-фосфатаза отщепляет ужененуж |
ный фосфат. |
|
|
|
|
|
|
Еслиобразуется |
фруктозо-1-фосфат,тоонприучастии |
альдолазы разделяетсяна |
|||||
глицеральдегдиокси.Д лиеецеральдегидтонфосфатфосфорилируется |
|
|
|
триозоки- |
|||
назой. |
|
|
|
|
|
|
|

biokhimija.ru |
ТиминО.А. |
Лекции по общей биохимии (2018г) |
191 |
|
|
|
|
|
Уполученныхтриозофосфатовестьал :тернатива |
|
|
|
|
|
o |
либоспользоватьсягликолизе, |
|
|
|
|
|
o |
лиобоъединявофруктозоься |
|
|
-1,6-дифосфат,дефосв руктозоорилироваться |
-6- |
|
|
фосфат,изомеризвглюкозоваться |
|
-6-фосфатидалеепревсвободнуюращатьсяглюк |
о- |
||
|
зу. |
|
|
|
|
|
|
Припервомвариантефруктиспопеченильзузакакэнергетическийтсясубстратили |
|
|
|
||
длясинтез ажирвариант.Втопойдразумполучглюкозоеваетние |
|
-6-фосфатаилиглюк |
о- |
|||
зыиихиспользованиекаких |
|
-либоцелях. |
|
|
|
|
|
Особенностью мышц являетсяотсутствиефруктокиназы,поэтомуфруктозавнихпр |
|
е- |
|||
вращсразуфруктозоется |
|
-6-фосфатипоступаетвреакциигли |
колсинтезаилигликог |
е- |
||
на. |
Особменностьютаболизмафрукявляетсячто, ферментзы |
|
|
фруктокиназа являет- |
||
|
|
|
||||
ся инсулин-независимым.Врезультате |
впечени |
превфращениевуктозыпировиногра |
д- |
|||
нуюкислоацетуил |
-SКоАпроисходитбыстрее,чемдляглюк.Этозы |
объясиг" няется |
о- |
|||
рированием"лимитирующейреакцииметаболиглюко,катализируемоймаы |
|
фосфофрук- |
||
токиназой.Дальнейшметаболизмацет й |
-SКоАвданнможетслучаепркизбвести |
|
ы- |
|
точному образованиюжирныхкислот |
итриацилглицеролов. |
|
|
|
НА Р УПРЕВРАЩШ Н И Я ЕНИЯ |
ФРУКТОЗЫ |
|
|
|
|
Эссенциальнаяфруктозурия |
|
|
|
Генетическийдефект |
фруктокиназы приводиткдоброкачественной |
эссенциальной |
||
фрукт,пробтзуриивсякихезокающейтрицательныхсимптомов. |
|
|
|
|
|
Наследственнаяфруктозурия |
|
|
|
Заболеформируевследсаниеаследственаутосомвиесяных |
|
о-рецессивныхдефе |
к- |
|
товдругихферментовобменафруктозы. |
|
|
|
|

Строениеобменуглеводов |
|
|
|
|
|
192 |
|
|
|
|
|
||
Дефект фруктозо-1-фосфат альдолазы,котвнормеприсутствуетаяпечени,к |
|
|
|
и- |
||
шечнивеществекорковомпочек, |
прояпослевведениялярационтсямладенцасоков |
снижениеммобилизации |
|
|||
фруктов,соде жащихуктозу |
исахарозу |
. Патогенезсвязансо |
|
|||
гликогена из-заингибглиркофруктозогеванфосфорилазыия |
|
-1-фосфатоми |
ослаблением |
|||
глюконеогенеза,т.к.дефектныйферментспособучаствоватьренкцияхналогично |
|
|
|
|
|
|
фруктозо-1,6-дифосфат альдолазе.Пр оявляетсязаболеваниеснижениемконцентрации |
|
|
|
|
||
фосфатов вкрови,гиперфруктоземией,тяжелойпосле ищевойогликемией. |
|
|
|
Отмечается |
||
вялость,нарушениясознания,почечныйканацидозльцевый. |
|
|
|
|
|
|
Дефект фруктозо-1,6-дифосфатазы проявлясходнопредыдущим,нотся |
|
|
етак |
я- |
||
жело. |
|
|
|
|
|
|
П Р Е ВГРЛАЮВЩКЕОНЗИЫЕ |
Ф Р У К Т О З У |
|
|
|
||
Превращениеглюкозыфруктозупроисходит |
полиоловомпути |
метаболизмагл |
ю- |
|||
козы.Дляобеспеченреакцийэтогопутвклеткахприсутствуетяфермент |
|
|
альдозоредукта- |
|||
за,котораяпревращаетглюкозусорбитол. |
|
Обычно вданнуюреакциюпопадаетнеболее |
|
глюкозами- |
||
1%глюкозы,ионаисподполяьзфруктозыченияетсявпроцессесинтеза |
|
|
|
|
||
нов. |
|
|
|
|
|
|
Отдельноезначениепутьимвс етменныхпузырьках,которыесинтезируютфруктозу |
|
|
|
|
|
|
для семеннойжидкости |
.Сперматозоиды,находящиесязд |
есь,используютфруктозувкач |
|
|
е- |
|
ствеосновногоэнергетичсубстрата,ноприереходевскогоженскиеполовыепутипер |
|
|
|
|
е- |
|
ключаютсянаглюкозу.Счи, использованповышаетаетсяфруктозыстабильность |
|
|
|
|
|
|
предотвпреждевремращазрушениеакрососпт мноеыи |
|
|
я. |
|
|
|
Клизначимостьиеская |
полиолпутипровинсулинявляетсявого |
независимыхтк |
а- |
нях,вкоторыеглюкозапоступает |
неконтролируемо поградиентуконцентрации |
– эндоте- |
|
лий,хрустаглаза,клеткиклубочикпоче,но ков |
, впервуюочередь,нейроны |
. Путь активи- |
|
руетсяпри |
гипергликемиях,когдапотокглюкозывклеткиувеличиваетсяскоростьсинт |
|
е- |
|
за сорбитола резковозрастает. |
|
инозитола, |
||
Наксоплрбитвнейронахпниедсинтезлавляет |
циклическогоспирта |
|||
входящегосоставфосфолипидов |
ииспользуемогопри |
передачегормональногосигнала, |
и |
|
снижаетактивность |
Na+,K+-АТФазы,что нарушапроведениенервногоимпульсат. |
Избыток |
||
вклетке осмотическиактивных |
сорбитолафрудерживаетктозыводу,изменяетформу |
|
|
|
|||
клетокиих |
функциональную активность. |
|
|
|
|
||
Такжеи |
збыточнаяработа |
альдозоредуктазыприводит |
|
расходованию НАДФНвкле |
т- |
||
ках,чтоснижаетактивность |
ряда процессов,например,восстановление |
|
глутатиона вработе |
||||
антиоксистемидантных |
, синтез вазодилататора оксидаазот |
(NO),нейтрализация аммиа- |
|||||
ка вреакциивосстан |
овительногоаминирования |
α-кетоглутарата, |
микросомальное окисле- |
||||
ние. |
|
|
|
|
|
|
|

biokhimija.ru ТиминО.А. Лекции по общей биохимии (2018г) 193
|
С У Д Ь Б А ИИ С Т О Ч Н И К И |
Г Л ЮВК ЛКОЕТЗКЫЕ |
|
|
|||
|
Наличиеглюкозывклеткеобес,впеочервуючивается,п едьоникновениемее |
|
|
|
|
из |
|
крови.Такжепочтивсклеткиимеют |
|
запасыгликогена |
,которыйиспользуетсякак |
|
внут- |
||
риклеточный резерв глюкозы. Втожевремяп |
еченочныеклеткипобладаютчкиспосо |
|
б- |
||||
ностьюсинтезирглюкозуизнеуглеводкомпонентоввать( ых |
|
|
глюконеогенез). |
|
|||
|
Послепроникновенияклеткуглюкозаспособнапреврразличщаться |
|
|
|
нымнапр |
ав- |
|
лениям: |
|
|
|
|
|
|
|
o |
частьглюкозыобязатеиспользувэнергнобменет,онасгораетсяичв ском |
|
|
|
|
е- |
|
|
акциях катаболизма длясинтезаАТФ |
, |
|
|
гликогена,к |
||
o |
придостатбольшомк личествечноклеткеглюк |
|
|
озапасаввидется |
|||
|
синтезугликспособныбольшинствогена |
тканей, |
|
|
|
||
o |
вгепатоцитахпри(высокойконцентра) адипоглюкозаперенаправляетсяциитах |
|
|
|
|
||
|
на синтез триацилглицеролов и, например, |
впечени , на синтез холестерола, |
|
||||
o |
приопределенныхусловчастьглюкозыидетяхв |
|
|
реакции пентозофосфатного у- |
|||
|
ти,вкотообраом |
зуются рибозо-5-фосфатиНАДФН |
, |
|
|
||
o |
некдогтораялюкозыисподльзуется |
|
синтезагликозаминов |
идалееструкту |
р- |
||
|
ныхилииныхгетерополисахаридов. |
|
|
|
|
|
|
ФО С Ф О Р И Л И Р О В А Н И Е -Д Е Ф О С Ф О Р И Л И Р О В А Н И Е
ГЛ Ю К О З Ы
|
Попав любую клетку,глюкоза |
немедленно фосфорилируется ферментом гексокина- |
|||||
зой иуженеможетвыйтиизклетки.Поэтомугексп киназаназваниелучилаловушка" для |
|
|
|
|
|||
глюкозы". |
Фосфоглюкозырешилированиесрнесколькоетзузадач: |
|
|
|
|
||
o |
фосэфглюкозыатныйир |
невсостоянклеткивыйтиз |
,таккакмолекулаотр |
и- |
|||
|
цательно заряженаиотталкиваетсяфосфп липиднойверхностимембраны |
|
правильнуюориентацию |
, |
|
||
o |
наличиезаряженнойгруппыобеспечивает |
|
молекулыва |
к- |
|||
|
тивномцентфермента |
, |
|
|
|
|
|
o |
уменьшаетсяконцентрациясвободной |
|
|
(нефосфорилированной) |
глюкозы,чтосп |
о- |
|
|
собствует диффузиин |
овыхмолекулизкрови. |
|
|
|
|
|

Строениеобменуглеводов |
194 |
|
|
Дефосфорилирование глюкозыосуществляется |
глюкозо-6-фосфатазой.Этотфермент |
|
|||||||||
естьтольковпечени.Вэпителиичкахканальцевпочекработафермента |
|
|
|
|
тесно связана |
||||||
реабсорбциейглюкозы |
иразныхамино |
- икетокислотсм(Глюконео" |
генез") |
.Вгепатоцитах |
|
||||||
ферментнеобходим, |
т.к. печеньподдерживает |
постконцентрацииянство |
|
глюквкровизы |
|
|
|||||
приголоданиимышечныхнагрузках |
|
. |
|
|
|
|
|
|
|
||
|
|
|
Особенностигексок |
иназы |
печени от другихтк |
|
|||||
Существуютпринципиотличияметглюкоаболильныев змаы |
|
|
|
а- |
|||||||
ней.Этообъясняетрядомпричин,вчастности, я |
|
|
|
наличием втканях различныхизофе |
|
р- |
|||||
ментов гексокиназы. Для печени характерен особый изофермент гексокиназа IV,пол у- |
|||||||||||
чившийсобственназваниеое |
|
– глюкокиназа. Отличиями этогоферментаотгексокиназ |
|
|
|
||||||
другихтканей |
являются: |
|
|
|
|
|
|
|
|
|
|
o |
низкоесродство |
кглюкозе |
(в1000разменьше) |
,чтоведеткзахватуглюкозыпеч |
|
|
|
е- |
|||
ньютолькоприеевысокойконцентрациикровипосле( еды) |
|
|
|
.Инымисловами, |
|
печень |
|||||
не будет использовать глюкозу,еслиеё |
|
концентрация вкрови |
невнорм(ысокальном |
|
|
||||||
диапазоне) |
. |
|
|
|
|
|
|
|
|
|
|
o |
продукт реакции (глюкозо-6-фосфат) неингибирует фермент,втовремякакдр |
|
|
|
у- |
||||||
гихтканяхгексокиназачувсттакомувлияниюительна. |
|
|
|
Этоп зволяетгепатоциту |
|
|
|
||||
единицувременизахватыватьглюкозыбольше,че |
|
|
|
монмосразужеутилизоватьет, |
|
|
|
|
|||
o |
чувствительностьк |
действию инсулина – ферментактивируется |
этимгормоном |
. |
|
||||||
Благодаря таким отличиямгепатоцитможетэффективнозахватыватьглюкпослезу |
|
|
|
|
|
|
|||||
еды,накапливать |
глюкозо-6-фосфат и,неторопясь" ", |
метаболизировать его влюбомнапра |
|
в- |
|||||||
лении – синтезгликогена,пентозофосфатныйпуть,окислдоац тил |
|
|
|
-SКоА , CO2 и H2O, и |
|||||||
синтезлипидов. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
М Е Т АГБЛОИЛКИОЗГМЕН А |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|||||
Наибольшиезапасыглимеютсякогв на |
|
|
печени и скелетныхмышцах |
|
,новообще |
|
|||||
гликспосинтгенсобензироваться |
|
почти вовсехтканях.Резервыгликогенаклетках |
|
|
|
|
с- |
||||
пользуютсявзависимостиот |
их функциональныхособенностей. |
7 |
|
|
|
|
|
||||
В мышцах количествогликогена |
снижается обычнотолько |
вовремя |
физической |
||||||||
нагрузки – длительной |
/или напряженной. |
Накопление гликогена здесь отмечаетсявпер |
и- |
||||||||
одвосстановления ,особенно , есливосстановлениесопровождается |
|
приемом богатойуглев |
|
о- |
|||||||
дамипищи. |
И,конечно,количествогликогенамиоцитеснижается |
|
|
|
(к акивовсехдругих |
|
|
||||
клетках) вовремяголодания. |
|
|
|
|
|
|
|
|
|
||
Гликоген печени расщепляприснижконцентрацииглюктсяниивкр,преждевизы |
|
|
|
|
|
|
|||||
всегомеждуприемамипищи.Через12 |
|
|
-18часовголодзапгликоганиясывпечполнениа |
|
|
|
|
о- |
|||
стьюистощаются. |
Накапгликогенвается |
|
в печени только послееды |
,пригипергликемии |
. |
||||||
Этообъясняется |
особенностямиглюк,котораяимееткиназынизкоесродствоглюки зе |
|
|
|
|
|
|
||||
можетработать |
исключительно приеевысокихконцентрациях |
вкрови . |
|
|
|
|
|||||

biokhimija.ru |
|
ТиминО.А. |
Лекции по общей биохимии (2018г) |
|
195 |
|
|
|
|
|
|
||
|
|
С И НГ ТЛЕИЗК О Г Е Н А |
|
|
||
Синтезгликогенаначинаетсяобразованияглюкозо |
|
|
-6-фосфатаподдействием |
глюко- |
||
киназы впечениилидругих |
гексокиназ востальныхтканях.Какужеговорилось, |
|
глюкоки- |
|||
наза обладаетнизкимсродствглюкозем |
|
|
, ивгепатоцитглюкозбудетзадерживатьсях |
|
|
|
толькопри |
ее высокихконцентрациях. |
|
|
|
|
|
Непосредственно синтезгликогенаосуществляютследующиеферменты: |
|
|
|
|||
1. Фосфоглюкомутаза – превращаетглюкозо |
-6-фосфатвглюкозо |
-1-фосфат. |
|
|||
2. Глюкозо-1-фосфат-уридилтрансфераза – фермент,осуществляющийключевуюр |
|
е- |
||||
акциюсинтеза.Необэтойреакцииатимостьобеспечивг дролизомобраетсязующегося |
|
|
|
|
||
дифосфата. |
|
|
|
|
|
|
3. Гликогенсинтаза – образует α1,4-гликозидныесвязи |
иудлиняетгликогеновуюц |
е- |
|
почку,присоединяяактивированныйС |
1 УДФ-глюкозыС |
4-глюкозынаконцевомучастке |
|
гликогена. |
|
|
|
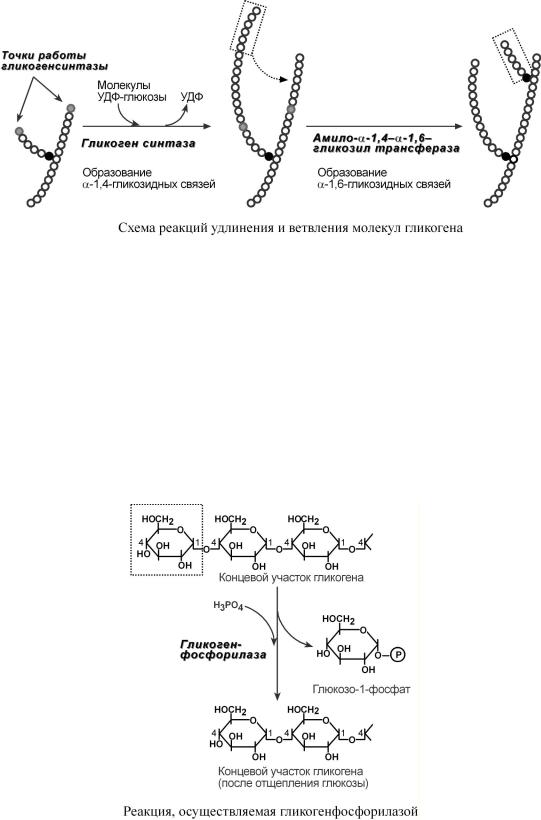
Строениеобменуглеводов |
196 |
|
|
4. Амило-α1,4-α1,6-гликозилтрансфераза, "гликоген-ветвящий" фермент – переносит фрагментсминимальнойдлинойвостатков6 глюкозы на соседнююцепьобразованием α1,6-гликозиднойсвязи.
|
М О Б ИГЛЛИИЗКАОЦГИЕ ЯН А |
|
|
|
|
||
Мобилизациягликогена |
(гликогенолиз)втканях |
активпрнедосируесвоботаткеся |
|
|
д- |
||
нойглюкозывклетке,азначитвкровиголодание( ,мышечнработ)Приэтом. уровеньая |
|
поддерживаеттолько печень,вкотор |
|
|
|
||
глюкозыкрови |
"целенаправленно" |
ой имеетсягл |
ю- |
||||
козо-6-фосфатаза,гидролизующ |
ая фосэфглюкозатныйир |
ы.Образуемая |
приэтом |
свобод- |
|||
наяглюкозавыходитчерезплазмембрануатическуювкровь.Остальоргаиспользные |
|
|
|
|
|
у- |
|
ютгликогентолькодлясобственныхнужд. |
|
Вгликогенолизенепосредственноучаству |
юттрифермента: |
1. Фосфорилазагликоген |
(кофермент пиридоксальфосфат) – расщепляет |
α1,4-гликозидныесвязиобразованиемглюкозо |
-1-фосфата.Ферментрабдтехопортает, |
покадоточкиветвленияα(1 |
-6)останетсяостатка4 глюкозы. |

biokhimija.ru |
ТиминО.А. |
Лекции по общей биохимии (2018г) |
|
197 |
|
|
|
||
2. α(1 -4)-α(1 -4)-Глюкантрансфераза – фермент, переносящийфрагмент |
изтрехоста |
т- |
||
ковглюкозы |
надругуюцепьсобразованиемновой |
α1,4 -гликозиднойсвязи.Прэтомна |
|
|
прежнеммеостодинаетсяостатокглюкозыи |
"открытая" доступная α1,6 -гликозидная |
|||
связь. |
|
|
|
|
3. Амило-α1,6-глюкозидаза, "деветвящий" фермент – гидролизует α1,6-гликозидную связьвысвобожднойением (нефосфорилированной) глюкозы.Врезультатеобраз у- етсяцепьбезветвлений,служащаясубстратдляфосфорилазы. м
|
|
Р Е Г УОЛБГЯМЛЦЕИИНКЯА |
|
О Г Е Н А |
|
||
|
Метаболизмгликогвпечениа |
регулируется нескгормонамилькими,одн |
иизкот |
о- |
|||
рых активируютферменты |
синтеза гликогена,адругие |
– ферменты распада гликогена.О |
с- |
||||
новныеф |
ерметаболизмнты |
а глиакогелтивныба |
овфосфорилированной,либод |
е- |
|||
фосфорилированнойформе. |
|
ам производят протеинкиназы,источником |
|
||||
|
Присфоединениесфатов |
кфермент |
фос- |
||||
фата являетсяАТФ: |
|
|
|
|
|
||
o |
фосфорилаза гликогена активируется послеприсоединенияфосфатнойгруппы, |
|
|
||||
o |
синтаза гликогенапослеприсоединенияфосфата |
|
инактивируется. |
|
|||
|
Фосфорилирование указанныхферментов |
начинается послевоздействиянаклеткуа |
д- |
||||
реналина,глюкагонанекотдругихор. моновых |
|
|
Врезультате |
адреналин и глюкагон |
|||
вызывают гликогенолиз,активируя фосфорилазу гликогена. |
|
|
|||||
|
Дефосфорилирование этих ферментовосуществляют |
протеинфосфатазы.Активат о- |
|||||
ром протеинфосфатаз,черезсложныйвнутриклеточныймеханпередачис ,гналазм |
|
высту- |
|||||
пает инсулин. Такимспособоминсулзапускаетингликогенатезсчет |
|
|
быстрой актива- |
||||
циигликогенсинактгликогенфосфорилазынтазывации. |
|
|
|
|
|||

Строениеобменуглеводов |
198 |
|
|
|
Одновременно инсулин и глюкокортикоиды увелсиглнтезчи,увеличваюткогена |
|
и- |
||||||
вая количество молекул гликогенсинтазы. |
|
|
|
|
|
||||
|
Длярегуляцииактивностифосфорилазысинтазыглиспкогенасобыйльзуется |
|
|
|
|
|
|
||
каскадныйаденилатциклазныймеханизм |
|
(смниже) |
. |
|
|
|
|
||
|
|
АК Т ФОСФОРИЛАЗЫВ А Ц И Я |
|
ГЛИКОГЕНА |
|
|
|||
|
Скоростьглико |
генолизалимитируетсятолькоскоростьюработы |
|
|
|
|
фосфорилазы глико- |
||
гена.Ееактивностьможетизменяться |
|
тремя способами: |
|
|
|
||||
o |
ковалентнаямодификация, |
|
|
|
|
|
|
|
|
o |
кальций-зависимаяактивация, |
|
|
|
|
|
|
||
o |
аллостерическаяактивацияпомощьюАМФ. |
|
|
|
|
|
|
|
|
|
|
Ковалентнаямодификация |
|
|
|
|
|
||
|
Придействии |
некготорыхрмоновнаклеткуп |
|
|
роисходит активация ферментачерез |
||||
аденилатциклазныймеханизм |
,который являетсятакназывакаскаднымремымгулиро |
|
|
ва- |
|||||
нием.Последовательностьсобытийданноммеханизмевключает: |
|
|
|
|
|
|
|
||
1М. |
олекула гормона (адреналин,глюкагон) |
взаимодействует сосвоим |
рецептором; |
||||||
2Активный. гормон |
-рецепткомплексв рздействуетнмембранныйа |
|
|
|
G-белок; |
|
|||
3. G-белок активируетфермент |
аденилатциклазу; |
|
цАМФ) – вторичныйпосредник |
||||||
4А. денилатциклпревращаетАТФциклическийАМФза( |
|
|
|
||||||
|
(мессенджер); |
|
|
протеинкиназуА |
|
|
|
||
5. цАМФаллостерическиактивируетфермен |
|
|
; |
|
|
||||
6П. ротеинкиназаАфосфорилиразличнывнутбелкииклеточные.уОднизэтихбем |
|
|
|
|
|
л- |
|||
|
ков является синтазагликогена |
, |
ееактивностьугнетается |
|
,другимбелком |
– киназа |
|||
|
фосфорилазы,котораяпри |
фосфорилактивируется; овании |
|
|
|
|
|
||
7К. иназафосфосфорилируетрилазы |
|
фосфорилазу" |
b" гликогена,послед няяврезультате |
||||||
|
превактивнуюращается |
фосфорилазу "а" ; |
|
|
|
|
|
||

biokhimija.ru |
|
ТиминО.А. |
Лекции по общей биохимии (2018г) |
|
199 |
|||
|
|
|
|
|
||||
8А. |
ктивная фосфорилаза "а" гликогенарасщепляет |
α1,4 -гликозидныесвязиког не |
|
|
||||
|
образованиемглюкозо -1-фосфата. |
|
|
|
|
|||
|
Кргормоновме,влияющихнаактивностьаденилатциклазычерезG |
|
|
|
-белки,существ |
у- |
||
ютиные способы регуляцииэтогомеханизма.Например, |
|
послевоздействия |
инсулина акти- |
|||||
вируется фермент фосфодиэстераза,котораягидролизуетцАМФ,следовательно, |
ликви- |
|||||||
дируетразвитаденимеханизмалатциклазндействияглюкагадреналина,свсемиого |
|
|
|
|
|
|||
вытекающимипоследствиями. |
|
|
|
|
|
|
||
|
|
|
Кальций-зависимая активация |
|
|
|||
|
Активкальцияионами |
|
заключаетсявактивации |
киназыфосфорил |
азы непрот |
е- |
||
инкиназой, |
ионами Ca2+ |
и кальмодулином. Этотпуработаетьприинициакальцийи |
|
- |
||||
фосфолипмеханидногозма |
(смГормоны" ") |
либоприотсутсвиистимуляцииаденилатцикл |
|
а- |
||||
зы. |
Это оправдываетсебя,например, |
|
вмышцах |
при умеренной нагрузке, |
когда влияниеа |
д- |
||
реналина чераденилатциклазу |
ещенепроизошлоили |
недостаточно, новцитоплазмупод |
|
|||||
влияниемнервныхимпоступаютульсовионы |
|
|
Ca2+. |
|
|
|||
|
Аллосактивацияерическая |
|
|
|
Такжесуществует |
ктивация фосфорилазыгликогена |
спомощьюАМФ |
– аллостериче- |
|
ская активацблагодаряприсоединениюАМФкмолекулефосфорилазы" |
|
b"Способ. раб |
о- |
|
таетвлюбойклетке |
– приувеличениирасходаАТФнакоплениипродуктовегораспада |
|
|
|
АДФиАМФ. |
|
|
|
|
|
|
|
|
|
|
Г Л И КБОГЛЕЕНЗОНВИЫ Е |
|
|
|
|
|
|
|
|
Этонаследствебусловленныезаб,олеванияедостаточностью |
|
каких-либофе |
р- |
|
ментов,отвечающихзаметаболизмгликогена. |
|
Средняячастотавстречаемостисоставляет |
|
|
1:40000. |
|
|
|
|
|
ГЛ И К О Г Е Н О З Ы |
|
|
|
Синдргликвомзникаетвгенозарезультадефесинтезарментак мобилиз |
|
|
а- |
|
цииглик,чтоприводитгенак |
накоплению или изменению структуры гликогенавразных |
|
||
тканях,чащевпеченимышцах. |
Внастоящгликогенвремяд попаляттогенетичзы |
|
е- |
|
скомупризнаку |
печеночные, мышечные и смешанные формы. |
|
|
|
Всуществуетего12типовгликогенозов.Попатогенетическомупризнакугликогенозы |
|
|
|
|
делят: |
|
|
|
|
• печеночные – 0, I, III,ХХIV, VI, VIII, IX, |
I типов, |
|
|
|
•мышечные – VиVIIтипов,
•смешанные – IIтипа.
