
- •Ответы по химии!
- •2 Химическая система (открытая, закрытая, изолированная). Внутренняя энергия.
- •5.Изобарный потенциал реакции (свободная энергия Гиббса). Критерий самопроизвольности реакций.
- •Принцип ле-шателье.Смещение химического равновесия.
- •1. Влияние температуры.
- •2. Влияние давления.
- •3. Влияние концентрации
- •10 Способы выражения концентраций растворов
- •13 Процесс электролитической диссоциации как взаимодействие веществ. Самоионизация.
- •14. Закон действующих масс в растворах электролитов. Сильные и слабые электролиты. Степень диссоциации.
- •15. Теория сильных электролитов. Активность. Коэффициент активности. Ионная сила растворов. Связь ионной силы раствора с коэффициентом активности.
- •16. Протолитическое равновесие. Кислоты, основания, амфолиты по Бренстеду.
- •17. Вода как растворитель. Дифференцирующие и нивелирующие растворители.
- •18. Автопротолиз. Ионное произведение воды. Рн
- •19. Гидролиз по катиону и аниону. Необратимый гидролиз. Константа и степень гидролиза. Расчёт pH.
- •Константа гидролиза.
- •Расчёт pH.
- •20. Буферные растворы, природные буферные системы. Расчёт pH буферных систем, буферная ёмкость.
- •21. Кислоты и основания по Льюису.
- •22. Гетерогенные равновесия. Произведение растворимости.
- •23. Химическая связь: типы связи, механизмы образования, характеристики.
- •24. Комплексные соединения (кс). Строение кс. Номенклатура кс. Классификация кс. Характер связи в кс.
- •Классификация
- •По заряду комплекса
- •По числу мест, занимаемых лигандами в координационной сфере
- •По природе лиганда
- •Химическая связь в комплексных соединениях.
- •25.Диссоциация комплексных ионов. Константа нестойкости. Комплексообразование в организме.
- •26.Изомерия кс. Комплексообразование в организме.
- •27.Строение гемма
- •28. Овр и их биологическая роль.
- •30. Коллоидные системы. Строение коллоидной частицы. Двойной электрический слой. Электрокинетические явления.
- •31. Методы очистки коллоидных растворов. Диализ, электролиз, ультрафикация.
- •32.. Получение и свойства дисперсных систем. Получение суспензий, эмульсий, коллоидных растворов.
- •33. Устойчивость дисперсных систем. Седиментационная , агрегативная и конденсационная устойчивость лиозолей. Факторы, влияющие на устойчивость лиозолей.
- •34. Коагуляция.Порог коагуляци и нго определение,правило Шульце-Гарди.Взаимная коагуляция.
- •35. Поверхностные явления и адсорбция. Адсорбционные равновесия и процессы на подвижных границах раздела фаз.Уравнение Гиббса
- •36. Поверхностно-активные и поверхностно-неактивные вещества. Изменение поверхностной активности в гомологических рядах (правило Траубе).
- •37. Поверхностное натяжение и методы его определения
- •38. Адсорбция из раствора на твёрдом адсорбенте
- •39. Адсорбционные равновесия на неподвижных границах раздела твёрдых фаз. Физическая адсорбция и хемосорбция
- •Типы адсорбционных взаимодействий
- •40.Адсорбция из растворов. Уравнение Ленгмюра. Зависимость величины адсорбции от различных факторов.
- •Зависимость величины адсорбции от:
- •41. Применения десорбциооных процессов в медицине Применение адсорбционных процессов в медицине
- •42. Хроматография
- •43. Специфические свойства вмс.
- •44. Понятие биогенности химических элементов.
- •45. Химия биогенных элементов s-блока.
- •46. Химия биогенных элементов d-блока.
- •47. Химия биогенных элементов p-блока.
- •49.Полифункциональные органические соединения
- •50 Полиамины: этилендиалин.Путресцин.Кадоверин.
- •51 Гетерофункциональные соединения
- •52 Б) Оксокислоты-адельгидо- и кетонокислоты
- •53 Гетерофункциональные производные бензольного ряда как лекарственные средства
- •54 Гетероциклическими называют циклические органические соединения, в состав цикла которых, помимо атомов углерода, входят один или несколько атомов других элементов (гетероатомов).
- •13.1.2. Номенклатура
- •13.2.1. Ароматические свойства
- •13.2.2. Кислотно-основные и нуклеофильные свойства
- •13.5.1. Гидроксипурины
- •55.Фолиевая кислота, биотин, тиамин. Понятие о строении и биологической роли. Представление об алкалоидах и антибиотиках
- •Эффекты биотина
- •Физиологические функции
- •Значение тиамина в спорте
- •Пищевые источники
- •Алкалоиды
- •Антибио́тики
- •56.Пептиды и белки
- •Свойства пептидов
- •R h2n—сн—соон
- •Биологическое значение углеводов
- •Виды углеводов
- •Гомополисахариды
- •Влияние мукополисахаридов на стабилизацию структуры коллагена дентины и эмали
- •58.Нуклеиновые кислоты
- •60.Полимеры. Понятие о полимерах медицинского назначения.
- •Полимеры медицинского назначения
10 Способы выражения концентраций растворов
Массовая доля вещества Массовая доля обозначается греческой буквой "омега" и равна отношению массы растворенного вещества к общей массе раствора
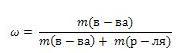
Выражают обычно в массовых долях или процентах (для этого в формуле правую часть домножают на 100%).
Молярная концентрация показывает, сколько моль вещества содержится в 1 литре (1000 мл.) раствора. Обозначается См. Единица измерения - [моль/л] (часто пишут просто М)
 ,
,
где n - количество вещества в молях, V - объём раствора, m - масса вещества, Mr - молярная масса вещества.
Моляльная концентрация число молей растворенного вещества в 1 килограмме (1000 г.) расторителя. Единица измерения - [моль/кг]
![]()
Нормальная концентрация это число эквивалентов в 1 литре раствора. Обозначают символом Сн
![]()
0,1 нормальный раствор - децинормальный.
Титр количество вещества (в граммах), растворённое в 1 мл. раствора. Различают титр по растворённому веществу (например, титр раствора соляной кислоты — THCl) или титр по определяемому веществу (например, титр раствора соляной кислоты по едкому натру — THCl/NaOH)
![]() ,
,
где Т - титр в г/мл, Р - масса навески, V - объём мерной колбы.
11Растворимость веществ в воде зависит от температуры. Как правило, растворимость твердых веществ в воде увеличивается с повышением температуры, а растворимость газов уменьшается, поэтому воду можно полностью освободить от растворенных в ней газов кипячением. Насыщенным называют такой раствор, в котором при данной температуре вещество больше не растворяется. Ненасыщенным называют такой раствор, в котором при данной температуре находится меньше растворяемого вещества, чем в его насыщенном растворе. Пересыщенным называют такой раствор, в котором при данной температуре находится в растворенном состоянии больше вещества, чем в его насыщенном растворе при тех же условиях. Прочитайте в учебнике §34 стр. 190 о приготовлении пересыщенных растворов. Классификация веществ по их растворимости в воде.
Хорошо растворимые - если при комнатной температуре в 100 г воды растворяется больше 1 г этого вещества.
Малорастворимые – если при таких условиях растворяется меньше 1 г вещества в 100 г воды.
Практически нерастворимые вещества – такие вещества, растворимость которых меньше 0,01 г в 100 г воды.
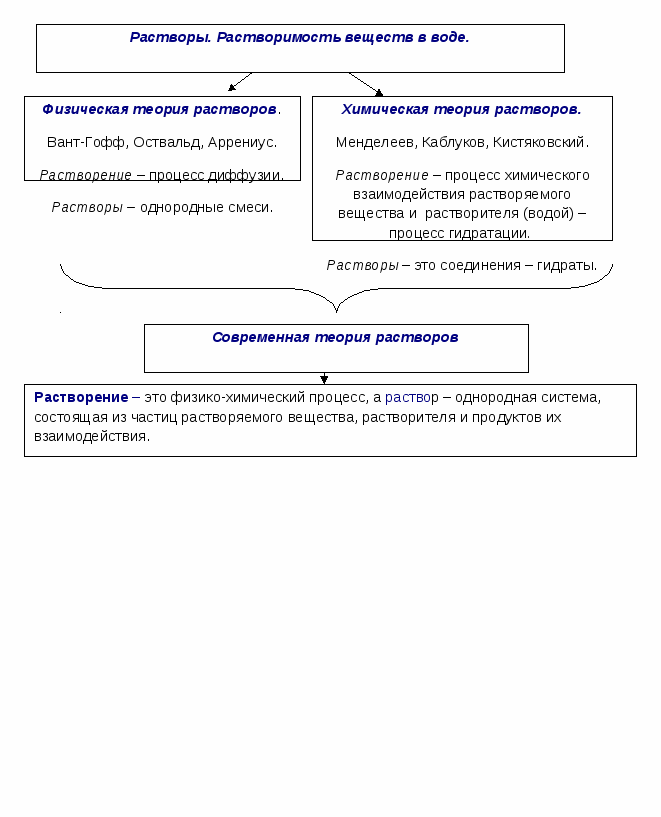
12Коллигативные свойства – это свойства растворов, зависящие от числа частиц растворенного вещества. К коллигативным свойствам растворов относят:
1) понижение давления насыщенного пара растворителя над раствором,
2) понижение температуры замерзания и повышение температуры кипения растворов по сравнению с температурами замерзания и кипения чистых растворителей.
3) осмотическое давление.
Идеальным раствором называют раствор, для которого выполняется первый закон Рауля.
Идеальными при любых концентрациях являются растворы, компоненты которых близки по физическим и химическим свойствам и образование которых не сопровождается объёмными и тепловыми эффектами. В этом случае силы межмолекулярного взаимодействия между однородными и разнородными частицами примерно одинаковы, и образование раствора обусловлено лишь энтропийным фактором.
Реальные растворы, компоненты которых существенно различаются по физическим и химическим свойствам, подчиняются закону Рауля лишь в области бесконечно малых концентраций.
Закон Рауля. Относительное понижение упругости пара растворителя над раствором равно мольной доле растворенного нелетучего компонента.
![]()
барометрическая формула Больцмана.
Следствия из закона Рауля:
1. Растворение нелетучего компонента в растворителе приводит к расширению температурной области существования жидкой фазы.
2. Понижение температуры замерзания и повышение температуры кипения прямо пропорциональны моляльной концентрации растворенного вещества.
3. Растворы, содержащие одинаковое число молей растворенных веществ в одинаковых молях растворителя, обнаруживают одно и то же понижение температуры замерзания и одно и то же повышение температуры кипения.
?tкип=Э x Смоляльн,
где Э – эбуллиоскопическая константа, +0,52.
?tзам=К x Смоляльн,
где К – криоскопическая константа, равная –1,86.
Эбуллиоскопическая константа – разница между температурой кипения раствора и температурой чистого растворителя.
Криоскопическая константа – разница между температурой замерзания раствора и температурой чистого растворителя.
Для решения задач об этих константах необходимо знать массу растворенного вещества и массу раствора. Например, масса хлороформа (трихлорметан CHCl3) рассчитывается по формуле:
ОСМОС (от
греч. ![]() -толчок, давление),
самопроизвольный перенос в-ва
через полупроницаемую
мембрану,
разделяющую два р-ра разл.концентрации или
чистый р-ритель и р-р.
-толчок, давление),
самопроизвольный перенос в-ва
через полупроницаемую
мембрану,
разделяющую два р-ра разл.концентрации или
чистый р-ритель и р-р.
