
- •Полимеризация
- •Классификация и номенклатура вмс
- •Синтез высокомолекулярных соединений
- •Радикальная полимеризация
- •Кинетика радикальной полимеризации
- •Методы изучения процесса радикальной полимеризации
- •Гель проникающая хроматография
- •Электронный парамагнитный резонанс (эпр)
- •Способы проведения полимеризации
- •Анионная полимеризация
- •Ионная (каталитическая) полимеризация
- •Кинетика катионной полимеризации
- •Анионная полимеризация
- •Кинетика анионной полимеризации
- •Стереоспецифическая полимеризация
- •Механизм смтереспецифическйо полимеризации
- •Сополимеризация
- •Определение констант сополимеризации. Их физический смысл.
- •Ингибирование и регулирование полимеризации
Радикальная полимеризация
Полимеризация ненасыщенных соединений в основном осуществляется по свободнорадикальному цепному механизму. Радикальная полимеризация инициируется свободными радикалами и рост макромолекулы начинается присоединением молекулы мономера к радикалу. Присоединение происходит по двойной связи мономера с образованием нового радикала, длина которого больше на одно элементарное звено
R+CH2=CHX RCH2CHX
Рост макромолекулы происходит результате дальнейшего присоединения молекул мономера к радикалу и в результате присоединения каждой последующей молекулы мономера образуется свободный радикал
RCH2CHX+CH2=CHX RCH2CHXCH2CHX
R(CH2CHX)n-2CH2CHX+CH2=CHX R(CH2CHX)n-1CH2CHX
Вновь образующиеся радикалы по свойствам аналогичны предшествующим и, таким образом, при присоединении молекулы к растущему радикалу происходит регенерация радикала. Как и всякая цепная реакция, полимеризация по свободнорадикальному механизму включает три стадии:
(R)22R - инициирование, или MM
R+MRM
RM+MRMM
RMn-2M+MRMn-1M
2RMn-1M
Исходный радикал, инициировавший полимеризацию, является составной частью образовавшейся макромолекулы.
ИНИЦИИРОВАНИЕ
Инициирование радикальной полимеризации может происходить любыми способами:
1. термической ПМ чистого мономера;
2. фотохимической ПМ при поглощении мономером кванта световой энергии;
3. радикальной ПМ под действием ионизирующих излучений (-лучи, рентгеновские лучи, ускоренные электроны).
Одним из наиболее распространенных методов ПМ является введение в мономер или смесь мономеров инициаторов – веществ, способных распадаться с образованием свободных радикалов.
Распад молекулы инициатора на свободные радикала требует намного меньшей затраты энергии, чем образование свободного радикала при непосредственной активации молекулы мономера.
В качестве инициаторов чаще всего используют перекись бензоила и динитрилазоизомасляной кислоты.
Рассмотрим ПМ под действием перекиси бензоила.
Перекись бензоила (ПБ) при реакции ПМ распадается по уравнению:
(C6H5COO)22C6H5COO
Скорость распада ПБ описывается уравнением
![]()
Заменив [(C6H5COO)2] на [И], получим
Wрасп=Красп[И] (1)
Радикал C6H5COO может распадаться с образованием финильного радикала:
C6H5COO C6H5+CO2
Инициировать ПМ могут быть оба радикала C6H5COO и C6H5 и скорость инициирования описывается уравнением
Wин=2*Wрасп=2*Красп[И] (2),
так как при распаде одной молекулы образуются два радикала, способных инициировать ПМ.
Не все радикалы способствуют росту цепи, часть из них гибнет в результате рекомбинации
C6H5 + C6H5C6H5C6H5
В связи с этим в уравнение (2) вводится коэффициент f, показывающий эффективность инициирования, т.е. долю первоначально образовавшихся радикалов, участвующих в инициировании ПМ.
Wин=2Kрасп[И]f, (3)
Заменив 2Kраспf на Кин, получим
Wин=Kин[И], (4)
В случае с ПБ эффективность f близка к единице.
При инициировании ПМ перкесью бензоила первоначально образовавшиеся радикалы C6H5COO будут расходоваться в ходе следующих реакций
![]() [I]
[I]
![]() [II]
[II]
а фенильный радикал будет расходоваться
![]() [III]
[III]
Экспериментально установить, что k1 и k2 и поэтому скорость инициирования ПМ фенильными радикалами будет определяться скоростью их образования, как более медленной стадией процесса. Скорость реакции [I] будет равна:
W1=K1[C6H5COO]
скорость реакции [II]:
W2=K2[C6H5COO]*[M]
Если долю радикалов C6H5COO, участвующих в инициировании полимеризации обозначить Х, то она будет равна:
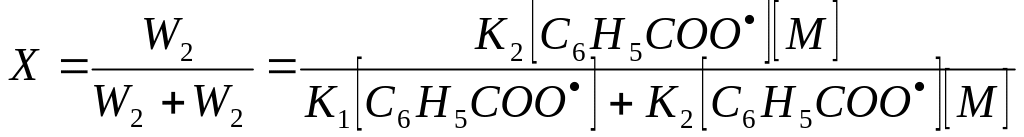 (5)
(5)
Преобразуем уравнение(5):
 (6)
(6)
![]() - соотношение
констант скоростей реакций радикалов
C6H5
и C6H5COO
с молекулами мономера. С уменьшением
концентрации мономера, происходит
уменьшение Х, т.е. возрастает скорость
реакции I.
- соотношение
констант скоростей реакций радикалов
C6H5
и C6H5COO
с молекулами мономера. С уменьшением
концентрации мономера, происходит
уменьшение Х, т.е. возрастает скорость
реакции I.
Содержание инициатора для полимеризации невелико и составляет 0,1 – 1 % от массы мономера.
В качестве инициаторов ПМ часто применяются: перекись бензоила, динитрил азоизомасляной кислоты, гидроперекись кумола, перекись третичного бутила, гидроперекись третичного бутила, гидроперекись ацетила, перекись водорода, персульфат калия K2S2O8; персульфат аммония (NH4)S2O8. Энергия активации инициирования определяется энергией, необходимой для распада инициатора, и зависит от его строения. Еин для перекиси бензола ~ 30 ккал/моль.
При термической ПМ образование свободного радикала происходит в результате раскрытия двойной связи мономера:
CH2=CHX
![]() CH2CHX,
CH2CHX,
и последующего взаимодействия образовавшегося радикала с молекулой мономера
CH2CHX + CH2=CHX CH2CHXCH2CHX
Термическая ПМ протекает медленно и скорость ее резко зависит от температуры, что связано с высокой энергией активации реакции инициирования.
Термическая полимеризация в чистом виде встречается редко, т.к. в мономерах практически всегда присутствуют примеси, взаимодействующие с мономером и образующие соединения, распадающиеся с генерированием свободных радикалов. Чаще всего такой примесью является кислород воздуха, который может реагировать с мономером с образованием перекиси.
Распадаясь, перекиси могут инициировать ПМ. Отсюда вытекает необходимость тщательного контроля чистоты исходных веществ и аппаратуры.
При фотохимической ПМ молекула мономера поглощает квант световой энергии и переходит в возбужденное состояние
CH2=CHX
![]() CH2CHX*.
CH2CHX*.
Чем большую энергию несет квант света, тем легче молекула мономера переходит в возбужденное состояние и поэтому наиболее активным является ультрафиолетовое излучение.
В результате мономолекулярного превращения возбужденная молекула образует радикал
CH2CHX* + CH2=CHX CH2CHXCH2CHX *
Т.к. образование активных центров при фотополимеризации протекает в результате прямого поглощения квантов энергии, фотополимеризацию можно проводить при температурах, при которых ПМ, инициируемая другими методами не происходит. Например, винилхлорид полимеризуется под действием УФ излучения при -35С.
При радиационной ПМ под действием -лучей, рентгеновских лучей, ускоренных электронов также происходит образование свободных радикалов, которые инициируют полимеризацию. При малых степенях превращений радиационная ПМ подчиняется закономерностям фотохимической ПМ, при глубоких степенях превращений процесс является более сложным.
РОСТ ЦЕПИ
Полимерная цепь растет в результате взаимодействия мономера с первоначально образовавшимся или растущим радикалом (см. выше).
Скорость роста цепи равна скорости исчезновения мономера.
![]() (7)
(7)
За одну секунду присоединяется 10000 молекул.
Рост цепи сопровождается выделением тепла за счет разности энергий двойной связи и двух простых связей и составляет ~ 22,5 ккал/моль.
Энергия активации роста цепи мала, она составляет ~ 4 ккал/моль.
ОБРЫВ ЦЕПИ
Обрыв цепи при радикальной полимеризации может происходить различными путями: реакции рекомбинации и диспропорционирования макрорадикалов, реакции передачи цепи через полимер, мономер, растворитель, инициатор, примеси и т.п. В большинстве случаев причиной обрыва являются реакции рекомбинации и диспропорционирования:
1. Реакция рекомбинации
2. Реакция диспропорционирования
В общем виде реакции обрыва можно записать:
Скорость обрыва цепи равна скорости исчезновения макрорадикалов:
Обрыв реакционной цепи, в котором принимают участие два радикала и скорость которого пропорциональна произведению их концентраций, называется квадратичным обрывом.
Энергия активации обрыва цепи практически равна 0.
Доля обрыва путем диспропорционирования или рекомбинации можно найти, определяя содержание остатка инициатора в полимере и его молекулярную массу.
![]() ~ 1 – диспропорционирования;
~ 2 – рекомбинация.
~ 1 – диспропорционирования;
~ 2 – рекомбинация.
