
- •Циклова комісія монтажних дисциплін Курс лекцій по теоретичним основам холодильної техніки
- •Лекція 1 вступ
- •1.1 Значення курсу “теоретичні основи холодильної техніки”
- •1.2 Короткий історичний огляд
- •1.3 Призначення холодильних установок
- •1.4 Промислові технології із застосуванням холоду
- •1.5 Класифікація холодильних установок
- •Питання для самоконтролю
- •Лекція 2 термодинаміка, як загальне вчення про енергетику
- •2.1 Фізичні основи одержання холоду
- •2.2 Термодинаміка, як загальне вчення про енергетику
- •2.3 Енергія, теплота, робота
- •2.4 Закон збереження енергії
- •2.5 Параметри стану
- •2.5 Рівняння стану
- •Питання для самоконтролю
- •Лекція 3 калоричні параметри стану
- •3.1 Рівноважний термодинамічний стан і рівноважні процеси
- •3.2 Зворотні і незворотні процеси
- •3.3 Кругові процеси Калоричні параметри стану: внутрішня енергія, ентальпія, ентропія
- •3.5 Робота й теплота процесу
- •Питання для самоконтролю
- •Лекція 4. Другий закон термодинаміки. Цикл карно
- •4.1 Другий початок термодинаміки
- •4.2 Цикл Карно
- •Питання для самоконтролю
- •Лекція 5 способи одержання низьких температур
- •5.1 Охолодження при фазових перетвореннях речовин
- •5.2 Охолодження шляхом розширення газів.
- •5.3 Термоелектричний метод
- •5.4 Холодильні установки з вихровою трубкою.
- •5.5 Способи охолодження камер
- •Питання для самоконтролю
- •Питання для самоконтролю
- •Лекція 7 холодоагенти
- •7.1 Основні визначення, короткий історичний огляд, позначення й торговельні марки
- •7.2 Критерії вибору і вимоги до холодоагенту
- •7.3 Холодильні агенти і охорона навколишнього середовища
- •7.4 Альтернативні однокомпонентні холодоагенти
- •7.5 Альтернативні багатокомпонентні холодоагенти групи гфв
- •7.6 Альтернативні багатокомпонентні холодоагенти групи гхфв
- •7.7 Який же холодоагент значніший ?
- •7.8 Особливості термодинаміки сумішей холодоагентів.
- •Лекція 8. Холодоносії
- •8.1 Призначення холодоносіїв та вимоги до них
- •8.2 Характеристика холодоносіїв
- •9.1 Вимоги до мастил
- •9.2 Типи мастил та їх характеристики
- •9.3 Циркуляція мастила у холодильній установці
- •Лекція 10 розширювальні та нагнітальні машини холодильних установок
- •10.1 Призначення та класифікація розширювальних та нагнітальних машин
- •10.2 Термодинамічні основи процесів стиску та розширювання.
- •10.3 Поршневі детандери
- •10.4 Процеси стиску у компресорі
- •10.5 Холодопродуктивність компресора
- •10.6 Потужність компресора й енергетичні втрати
- •11.7 Область застосування компресорів
- •Лекція 11 основи теорії компресійних холодильних машин.
- •11.1 Ідеальна парова компресійна холодильна машина
- •11.2 Дійсний цикл парової холодильної машини.
- •11.3 Побудова холодильного циклу
- •Питання для самоконтрою
- •Лекція 12 ексергетичний метод аналізу ефективності холодильних систем
- •12.1 Властивості оборотних і необоротних циклів. Математичне вираження другого закону термодинаміки
- •7.2 Максимальна робота. Ексергія.
- •7.3 Ексергетичний баланс парокомпресорної холодильної установки
- •Питання для самоконтролю
- •Лекція 13 основи теорії газових холодильних машин.
- •13.1 Повітряна холодильна машина
- •13.2 Холодильна машина Стірлінга
- •Питання для самоконтрою
- •Лекція 14 Цикли багатоступінчатих холодильних машин
- •14.1 Причини переходу до багатоступінчастого стиску.
- •14.2 Вибір проміжного тиску.
- •14.3 Двоступінчаста холодильна машина зі змійовиковою проміжною посудиною й неповним проміжним охолодженням.
- •14.4 Двоступінчаста холодильна машина зі змієвиковою проміжною посудиною й повним проміжним охолодженням.
- •14.5 Двоступінчаста холодильна машина з теплообмінниками.
- •Питання для самоконтрою
- •Лекція 15 цикли каскадних холодильних машин
- •15.1 Найпростіша каскадна холодильна машина.
- •15.2 Реальна каскадна холодильна машина.
- •Питання для самоконтролю
- •Лекция 16 абсорбційні та пароежекторні холодильні установки
- •16.1 Принцип дії абсорбційної холодильної установки.
- •16.2 Цикл пароежекторної холодильної установки
- •Питання для самоконтролю
- •Лекція 17 теплові насоси
- •17.1 Компресія низкопотенційного природного тепла
- •17.2 Схема і принцип дії теплового насосу
- •17.3 Розрахунок тепонасосної установки
- •17.4 Двоступінчасті тепло насосні установки
- •17.5 Геотермальні теплові насоси
- •17.6 Екологічні аспекти впровадження теплових насосів
- •Питання для самоконтролю
- •Лекція 18 Енергозбереження при виробництві холоду
- •18.1 Стратегія енергозбереження
- •18.2 Законодавство України про енергозбереження.
- •18.3 Основні принципи енергозбереження
- •18.4 Вплив компонентів системи на ефективність
- •18.5 Сучасні енергозберігаючі технології компанії Данфосс
- •18.6 Застосування теплових насосів в Украъні
- •Використана література
2.5 Рівняння стану
Рівняння F(P,T,v) = 0, що зв'язує між собою параметри стану, називається рівнянням стану даної речовини. Існування такої однозначної залежності засновується на тому, що параметри Р, Т, v визначаються тими самими величинами: швидкістю руху молекул і відстанню між ними, які для кожного конкретного стану мають цілком певне значення.
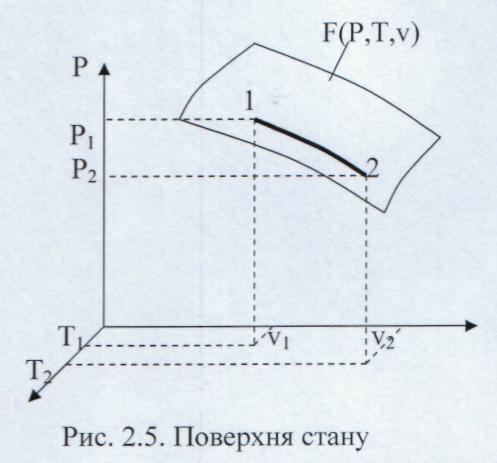
Кожен із параметрів стану системи є функцією інших її параметрів: Р = f( T,v ); T = φ( P, v ); v = ( P, T )
У системі координат Р, Т, v рівняння стану являє собою повер -хню, яку називають поверхнею стану або термодинамічною по - верхнею (Рис. 2.5).
Якщо хоча б один із параметрів стану змінюється, відповідно змі- нюється стан системи, т.б. відбувається термодинамічний процес.
Питання для самоконтролю
1. Яке значення має енергетика для сучасного суспільства?
2. Дайте визначення поняття енергії.
3. Які способи передачі енергії вивчаються у технічній термодинаміці?
4. Зобразіть принципову схему установки Джоуля і поясніть значення роботи у формулюванні першого закону термодинаміки.
5. Значення закону збереження енергії.
6. Наведіть аналітичний вираз першого початку термодинаміки.
7. Назвіть основні параметри стану.
8. Наведіть рівняння стану.
9. Яким чином можна змінити температуру випару?
10. За рухунок чого кипить холодильний агент у випарнику?
11. Від чого залежить температура кипіння?
Лекція 3 калоричні параметри стану
3.1 Рівноважний термодинамічний стан і рівноважні процеси
Рівняння стану має сенс тільки для рівноважних термодинамічних систем, у яких відсутній видимий обмін речовиною й енергією між різними частинами системи. При цьому необхідно мати на увазі, що на мікроскопічному рівні такий обмін відбувається завжди безупинно у зв’язку з наявністю теплового руху молекул. Однак, цей рух, при рівноважному стані системи, має однакову інтенсивність у протилежних напрямках і тому, на макроскопічному рівні, не сприймається.
Умовою рівноважності стану, є рівномірний розподіл по системі тих параметрів, розходження яких, є причиною обміну енергією. Так, для рівноваги термодинамічної системи у всіх її точках повинні бути однаковими температура й тиск. Відсутність рівноваги всередині термодинамічної системи приводить до складної залежності параметрів стану від часу й положення точки усередині системи, що унеможливлює застосування термодинамічних методів.
Будь яка ізольована система з часом приходить у рівноважний стан, що залишається незмінним доти, поки система не буде виведена з рівноваги зовнішнім впливом. Будь який процес зміни стану тіла являє собою відхилення від стану рівноваги.
Послідовна зміна стану тіла, що відбувається в результаті енергетичної взаємодії робочого тіла з навколишнім середовищем, називається термодинамічним процесом. Процес, що протікає настільки повільно, що в системі в кожен момент часу встигає встановитися рівноважний стан, називається рівноважним або квазистатичним (як би рівноважний).
Будь який реальний процес, в більшій або меншій мері, є нерівноважним. Однак, ця нерівномірність може бути зроблена як завгодно малою в результаті зменшення швидкості здійснення процесу. Таким чином, рівноважний процес є граничним випадком нерівно- важного процесу при прагненні швидкості цього процесу до нуля.
Якщо, наприклад, здійснюється процес стиску в циліндрі, то при русі поршня з кінцевою швидкістю, в першу чергу, будуть стискуватися ті шари газу, які розташовані поблизу поршня, тобто тиск у цих місцях буде більше, ніж середній тиск газу по всьому об’ємі циліндра. Поки збурювання, викликане переміщенням поршня і яке має кінцеву швид- кість, поширюється по всьому об’єму, поршень устигає переміститися на деяку відстань і тиск газу біля поршню знову зростає і т.д. Маємо нерівноважний процес стиску – тиск газу в циліндрі в міру переміщення поршня, буде різним у різних частинах об’єму, який займається газом. Природно, чим менше швидкість здійснення процесу, тим ближче цей процес до рівноважного, тому що при досить малій швидкості руху поршня підвищений тиск під поршнем буде встигати поширюватися по всьому об’єму газу. У цьому випадку, процес буде дуже близький до рівноважного, тому що тиск газу в різних точках об’єму циліндра буде розрізнятися досить мало.
