
- •Циклова комісія монтажних дисциплін Курс лекцій по теоретичним основам холодильної техніки
- •Лекція 1 вступ
- •1.1 Значення курсу “теоретичні основи холодильної техніки”
- •1.2 Короткий історичний огляд
- •1.3 Призначення холодильних установок
- •1.4 Промислові технології із застосуванням холоду
- •1.5 Класифікація холодильних установок
- •Питання для самоконтролю
- •Лекція 2 термодинаміка, як загальне вчення про енергетику
- •2.1 Фізичні основи одержання холоду
- •2.2 Термодинаміка, як загальне вчення про енергетику
- •2.3 Енергія, теплота, робота
- •2.4 Закон збереження енергії
- •2.5 Параметри стану
- •2.5 Рівняння стану
- •Питання для самоконтролю
- •Лекція 3 калоричні параметри стану
- •3.1 Рівноважний термодинамічний стан і рівноважні процеси
- •3.2 Зворотні і незворотні процеси
- •3.3 Кругові процеси Калоричні параметри стану: внутрішня енергія, ентальпія, ентропія
- •3.5 Робота й теплота процесу
- •Питання для самоконтролю
- •Лекція 4. Другий закон термодинаміки. Цикл карно
- •4.1 Другий початок термодинаміки
- •4.2 Цикл Карно
- •Питання для самоконтролю
- •Лекція 5 способи одержання низьких температур
- •5.1 Охолодження при фазових перетвореннях речовин
- •5.2 Охолодження шляхом розширення газів.
- •5.3 Термоелектричний метод
- •5.4 Холодильні установки з вихровою трубкою.
- •5.5 Способи охолодження камер
- •Питання для самоконтролю
- •Питання для самоконтролю
- •Лекція 7 холодоагенти
- •7.1 Основні визначення, короткий історичний огляд, позначення й торговельні марки
- •7.2 Критерії вибору і вимоги до холодоагенту
- •7.3 Холодильні агенти і охорона навколишнього середовища
- •7.4 Альтернативні однокомпонентні холодоагенти
- •7.5 Альтернативні багатокомпонентні холодоагенти групи гфв
- •7.6 Альтернативні багатокомпонентні холодоагенти групи гхфв
- •7.7 Який же холодоагент значніший ?
- •7.8 Особливості термодинаміки сумішей холодоагентів.
- •Лекція 8. Холодоносії
- •8.1 Призначення холодоносіїв та вимоги до них
- •8.2 Характеристика холодоносіїв
- •9.1 Вимоги до мастил
- •9.2 Типи мастил та їх характеристики
- •9.3 Циркуляція мастила у холодильній установці
- •Лекція 10 розширювальні та нагнітальні машини холодильних установок
- •10.1 Призначення та класифікація розширювальних та нагнітальних машин
- •10.2 Термодинамічні основи процесів стиску та розширювання.
- •10.3 Поршневі детандери
- •10.4 Процеси стиску у компресорі
- •10.5 Холодопродуктивність компресора
- •10.6 Потужність компресора й енергетичні втрати
- •11.7 Область застосування компресорів
- •Лекція 11 основи теорії компресійних холодильних машин.
- •11.1 Ідеальна парова компресійна холодильна машина
- •11.2 Дійсний цикл парової холодильної машини.
- •11.3 Побудова холодильного циклу
- •Питання для самоконтрою
- •Лекція 12 ексергетичний метод аналізу ефективності холодильних систем
- •12.1 Властивості оборотних і необоротних циклів. Математичне вираження другого закону термодинаміки
- •7.2 Максимальна робота. Ексергія.
- •7.3 Ексергетичний баланс парокомпресорної холодильної установки
- •Питання для самоконтролю
- •Лекція 13 основи теорії газових холодильних машин.
- •13.1 Повітряна холодильна машина
- •13.2 Холодильна машина Стірлінга
- •Питання для самоконтрою
- •Лекція 14 Цикли багатоступінчатих холодильних машин
- •14.1 Причини переходу до багатоступінчастого стиску.
- •14.2 Вибір проміжного тиску.
- •14.3 Двоступінчаста холодильна машина зі змійовиковою проміжною посудиною й неповним проміжним охолодженням.
- •14.4 Двоступінчаста холодильна машина зі змієвиковою проміжною посудиною й повним проміжним охолодженням.
- •14.5 Двоступінчаста холодильна машина з теплообмінниками.
- •Питання для самоконтрою
- •Лекція 15 цикли каскадних холодильних машин
- •15.1 Найпростіша каскадна холодильна машина.
- •15.2 Реальна каскадна холодильна машина.
- •Питання для самоконтролю
- •Лекция 16 абсорбційні та пароежекторні холодильні установки
- •16.1 Принцип дії абсорбційної холодильної установки.
- •16.2 Цикл пароежекторної холодильної установки
- •Питання для самоконтролю
- •Лекція 17 теплові насоси
- •17.1 Компресія низкопотенційного природного тепла
- •17.2 Схема і принцип дії теплового насосу
- •17.3 Розрахунок тепонасосної установки
- •17.4 Двоступінчасті тепло насосні установки
- •17.5 Геотермальні теплові насоси
- •17.6 Екологічні аспекти впровадження теплових насосів
- •Питання для самоконтролю
- •Лекція 18 Енергозбереження при виробництві холоду
- •18.1 Стратегія енергозбереження
- •18.2 Законодавство України про енергозбереження.
- •18.3 Основні принципи енергозбереження
- •18.4 Вплив компонентів системи на ефективність
- •18.5 Сучасні енергозберігаючі технології компанії Данфосс
- •18.6 Застосування теплових насосів в Украъні
- •Використана література
2.4 Закон збереження енергії
Необхідність вивчення процесів взаємного перетворення теплоти й роботи виникла з появою теплових двигунів. Відомо, що механічна робота значно простіше перетворюється на тепло, ніж тепло на механічну роботу. Для перетворення тепла в механічну роботу потрібне дотримання особливих умов та створення теплосилових установок. Тому, перед винахідниками й вченими Джеймс Уатт (1736 - 1819 рр), один з винахідників парової машини, порушив питання: скільки палива буде потрібно щоб одержати певну роботу, та якими засобами при заданій величині роботи можна звести до мінімуму витрату палива. Щоб відповісти на це непросте питання, було потрібно встановити зв’язок між механічною роботою й теплотою та прийняти ідею еквівалентності теплоти та механічної роботи. Найбільш складним з’явилося встановлення загального закону збереження енергії, включаючи дію диссіпативних (розпорошених) сил, що приводять до розсіювання роботи й перетворення її в теплоту.
Якби у 50-і роки 19-го сторіччя був поставлений пам'ятник невідомому вченому, то на ньому міг бути такий напис [16]: “ На згадку горя й розпачу тих, хто намагався створити вічний двигун.” Закон збереження енергії, що довів даремність цих спроб, пов’язаний з іменами трьох великих людей: корабельним лікарем на голландському військовому кораблі Юліусом Робертом Майєром (1814 – 1878 рр), англійським фізиком, у минулому манчестерським броварником, Джеймсом Прескоттом Джоулем (1818 - 1889 рр) і німецьким натураліс- том Германом Людвігом Фердинандом Гельмгольцем (1821 – 1894 рр). Слід зазначити, що ще мислителі стародавності (Демокрит й Эпікур) затверджували вічність і незнищуваність матерії й руху, а загальне формулювання закону збереження руху і матерії вперше дав М.В. Ломоносов. У 1744 році Ломоносов написав знамениті слова: “Всі зміни в натурі що трапляються, такого суть стану, що скільки чого в одного тіла відніметься, стільки додасться до іншого; так, коли де убуде трохи матерії, то помножиться в іншому місці ... цей загальний природний закон простирається й у самі правила руху, тому що тіло, що рухає своєю силою інше, стільки ж оної у себе губить, скільки передає іншому, котре від нього рух одержує.” Але, на жаль, і епоха була ще не та, та не було експериментальних даних, які з’явилися тільки після робіт Майєра й Джоуля, що дозволили встановити еквівалентність різних форм руху матерії і показати кількісний зв’язок між ними.
Оскільки закон збереження енергії, за словами Джона Бернала, був найбільшим фізичним відкриттям ХІХ століття, що з’єднав багато наук і став універсальною валютою фізики, то його творці заслу- говують на більш пильну увагу.
Юліус Роберт Майєр дійсно був генієм, що прийшов у наш світ з єдиною метою: зробити це велике відкриття. Герман Людвіг Фердинанд Гельмгольц назвав цей закон “Еrhaltung der Rraft”, тобто законом збереження енергії. Подібно Майєру, він почав свою діяльність як лікар, але прожив чудове життя як найбільший фізіолог і фізик того часу. Джеймс Прескот Джоуль працював більше сорока років над експериментальними дослідженнями еквівалентності роботи й теплоти. Батько Джоуля був власником пивоварного заводу. Тут були машинний цех і інші сприятливі для роботи Джоуля умови, що багато в чому сприяло дослідженням, які стали наріжним каменем сучасної термодинаміки.
До закону збереження енергії першим вдалося наблизитися Майєру, коли він звернув увагу на те, що в тропічних широтах у захворілих аборигенів венозна кров була не настільки темною, як у помірних широтах. Майєр припустив, що це може бути пов’язане з теорією Антуана Лорана Лавуазьє про окислювання крові у тварин. Із цієї теорії випливало, що в тропічних зонах процес окислювання крові може відбуватися повільніше через зменшення швидкості теплообміну організму тварини з навколишнім середовищем. Мейєр зрозумів, що при високій середній температурі повітря для підтримки життєдіяльності й необхідної температури організму потрібно менше живильних речовин і менше “згоряння” останніх. Ідеї Майєра носили настільки загальний й універсальний характер, що вони спочатку не були сприйняті сучасниками. Його життя перетворилося на безперервну боротьбу за ствердження свого принципу.
Класичні виміри механічного еквівалента теплоти провів в 1841 - 1843 роках Джеймс Джоуль. Цікаво відзначити, що й роботу Джоуля Британське королівське суспільство відмовилося опублікувати в повному обсязі, жадаючи від нього все нових і нових експериментальних уточнень.
Нарешті, Герман Гельмгольц у 1847 році в роботі ”Про збереження сили” дав у найбільш загальному змісті закон збереження енергії, показавши, що сума потенційної й кінетичної енергії залишається постійною. Велике значення мав наведений в тій же роботі доказ того, що процеси в живих організмах теж підкоряються закону збереження енергії.
Роботи Джоуля привели в підсумку до формулювання першого закону термодинаміки, що визначає величину, яка називається енергією та затверджує:
– еквівалентність взаємних перетворень теплоти й роботи (кіль- кісна сторона процесу);
 – сталість
енергії ізольованої термодинамічної
системи;
– сталість
енергії ізольованої термодинамічної
системи;
– взаємозв’язок між теплотою, внутрішньою енергією системи й роботою, чиненої нею, або чинену над нею навколишнім середовищем.
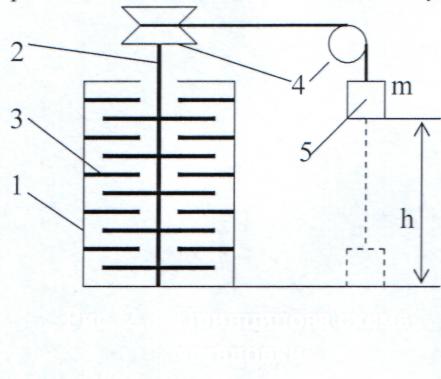
У знаменитих роботах Джоуля вантаж, що спускається через систему блоків 4, обертав мішалку занурену в різні рідини. Мішалка знаходиться в теплоізольованій мідній посудені 1 з лопатками 3. За рахунок дії сил тертя механічна робота перетворюється в тепло, причому кількості витраченої роботи завжди відповідала цілком певна кількость теплоти, що виділилась. Вантаж, спускаючись на висоту h ви-
конував роботу А = mh, рівну змен-
Рис. 2.3 Принципова схема шенню потенційної енергії вантажу
установки (рис. 2.3). Теплота, що виділилась в
посудені, визначалась по підвищенню температури рідини.
Для термодинамічних процесів, у яких енергія підводиться, або приділяється тільки у формі роботи й теплоти, а сама система перебуває в енергетичній взаємодії з навколишнім середовищем, маємо:
q =Δu +А, або ∂q = du + ∂А, Дж/кг, (2.4)
де q – теплота процесу; Δu – зміна внутрішньої енергії; А – робота процесу.
Записаний так загальний принцип збереження енергії в термоди- намічному процесі називається аналітичним вираженням першого початку термодинаміки. Рівняння збереження енергії в його характерній термодинамічній формі є тим наріжним каменем, на якому будується її своєрідний апарат. Апарат цей відрізняється високою ефективністю – його застосування створило можливість теоретичного встановлення безлічі кількісних залежностей, що зв’язують між собою різнорідні фізичні величини в умовах рівноваги. Незважаючи на те, що величини які входять в (2.4) мають однакову розмірність, фізичні поняття, що визначають ці величини, глибоко різні. Оскільки внутріш- ня енергія є параметром стану, про що поговоримо пізніше, то du – його повний диференціал і знак d означає “малу зміну будь чого”; ∂q й ∂А є нескінченно малими величинами, що залежать від шляху процесу, і тому не можуть бути повним диференціалом. Знак ∂ означає “мала кількість будь чого”.
