
- •Часть I
- •Содержание
- •Введение
- •Алканы, алкены, алкины. Способы получения, свойства
- •Получение алканов
- •2. Прямой синтез из элементов
- •Каталитическое гидрирование монооксида углерода
- •Синтезы индивидуальных парафинов
- •Химические свойства алканов
- •Г) Изомеризация, дегидрирование, ароматизация алканов
- •Получение алкенов
- •Химические свойства алкенов
- •Д) Реакции присоединения, протекающие против правила Марковникова
- •E) Окисление алкенов
- •З) Реакции полимеризации алкенов
- •Синтез ацетилена в промышленности, способы введения тройной связи
- •Химические свойства алкинов a) Реакции электрофильного присоединения
- •Б ) Присоединение галогенводородов по тройной связи идет по правилу Марковникова, труднее, чем к алкенам:
- •Д) Реакции с участием подвижного атома водорода в ацетилене
- •Е) Окисление ацетилена
- •В избытке окислителя может происходить полное разрушение молекулы алкина:
- •Ж) Димеризация и полимеризация ацетилена проходят каталитически.
- •Практическая работа № 1 получение и свойства метана, алкенов и ацетилена
- •2. Получение и исследование некоторых свойств алкенов
- •3. Получение ацетилена и исследование его свойств
- •Контрольные вопросы и задания
- •Реакции электрофильного замещения в ароматических соединениях
- •Типы электрофильных реагентов. Пути их образования
- •Эффекты замещения. Ориентанты I и II рода. Индуктивное и мезомерное влияние заместителей
- •Согласованная и несогласованная ориентация заместителей
- •Практическая работа № 2 свойства ароматических соединений получение мета-динитробензола
- •1. Окисление ароматических углеводородов
- •2. Качественная реакция на ароматические углеводороды
- •3. Синтез мета-динитробензола
- •Контрольные вопросы и задания
- •Реакции аренов, приводящие к неароматическим системам. Окислительные превращения
- •Практическая работа № 3 получение бензойной кислоты окислением арена
- •Контрольные вопросы и задания
- •Способы очистки твердых органических соединеий
- •Практическая работа № 4 очистка бензойной кислоты методом перекристаллизации, определение температуры плавления
- •1. Перекристаллизация
- •2. Определение температуры плавления
- •Контрольные вопросы и задания
- •Способы получения галогенпроизводных предельных углеводородов. Реакции нуклеофильного замещения
- •Практическая работа № 5 синтез бромистого алкила
- •1. Синтез бромистого алкила
- •2. Очистка вещества перегонкой при атмосферном давлении
- •Контрольные вопросы и задания
- •Правила техники безопасности при выполнении работ
- •Литература
- •Часть I
- •603950, Нижний Новгород, пр. Гагарина, 23
Д) Реакции присоединения, протекающие против правила Марковникова
Присоединение против правила Марковникова проходит если:
а) у углерода при двойной связи имеются группы с сильным отрицательным индукционным эффектом (но не галогены)
б) реакции инициируются светом, пероксидами и т.п.
Рассмотрим случай б).
Правило Марковникова соблюдается только при ионном (гетеролитическом) механизме присоединения галогенводородов. Для HBr (но не для HCl и воды) Хараш и Майо в 1939 г. установили радикальный (гомолитический) механизм присоединения к алкенам. В присутствии кислорода на свету или пероксидов HBr присоединяется против правила Марковникова.
hv
HBr + O2 Br + HOO или
ROOR 2 RO; RO + HBr Br + ROH
RCH=CH2 + Br RCHCH2Br
RCHCH2Br + HBr RCH2CH2Br + Br и т.д.
Образование конечного продукта цепной радикальной реакции объясняется конкурирующим образованием более стабильного вторичного радикала на первой стадии:
RCH=CH2 + Br RCHCH2Br более устойчив!
![]()
RCHBrCH2
E) Окисление алкенов
Алкены окисляются кислородом или другими окислителями. Направление окисления зависит от условий реакции и выбора окислителя.
1) Реакция Вагнера – окисление алкенов водным слабощелочным растворолм KMnO4. Продуктами реакции являются двухатомные спирты – гликоли.
3 RCH=CH2 + 2 KMnO4 + 4 H2O 3 RCH(OH)CH2(OH) + 2 KOH + 2 MnO2
Реакцию часто используют как качественную на кратную связь.
2) Деструктивное окисление
Под действием концентрированных растворов сильных окислителей (K2Cr2O7, KMnO4, HNO3) алкены окисляются с разрывом двойной связи. В результате получаются кетоны или кислоты:
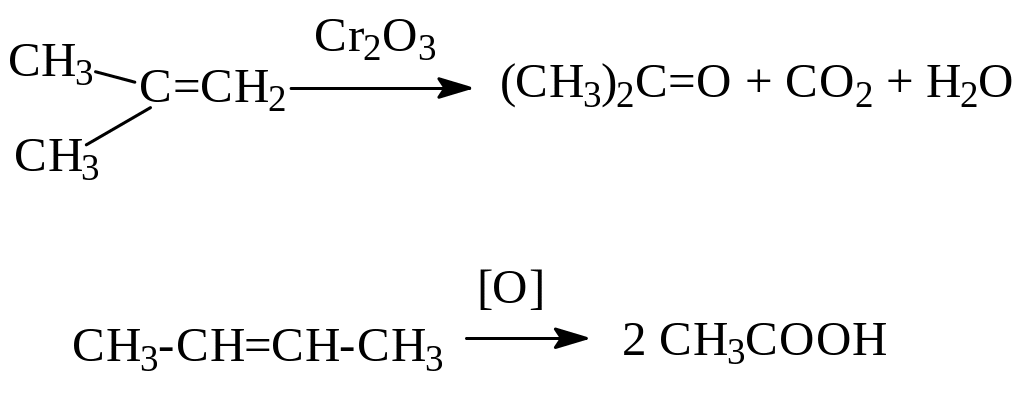
Реакция используется для определения строения алкенов, так как по образовавшимся кетонам и кислотам можно судить о строении и составе радикалов, связанных с углеродами двойной связи в исходном соединении.
3) Получение эпоксидов:
Реакция Зимакова: кислородом воздуха в присутствии серебряного катализатора алкены окисляются до эпоксидов:
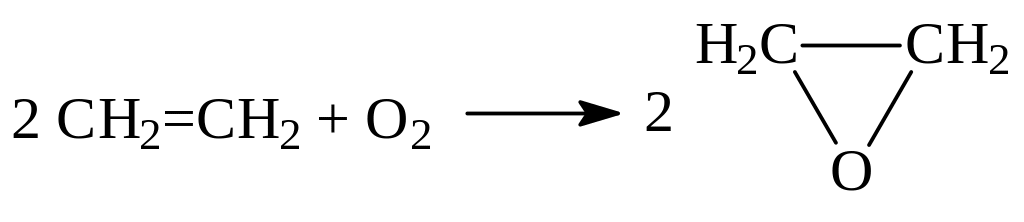
Аg
этиленоксид (окись этилена)
Реакция Прилежаева (1920):
А налогично
действуют перкислоты
(перуксусная и пербензойная):
налогично
действуют перкислоты
(перуксусная и пербензойная):
перкислота кислота
4) Озонирование
Д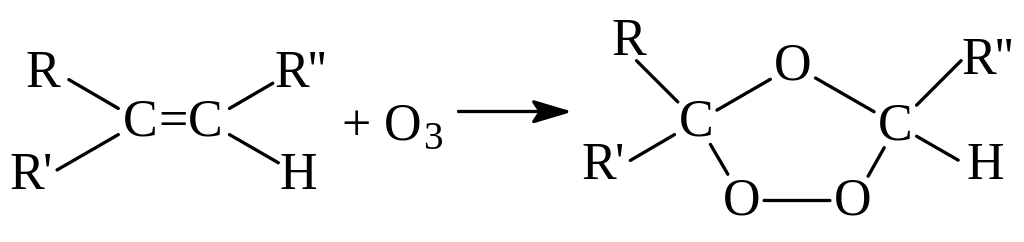 ля
установления строения алкенов важное
значение имеет реакция озонировани,
предложенная Гарриесом:
ля
установления строения алкенов важное
значение имеет реакция озонировани,
предложенная Гарриесом:
- озонид
Образующиеся озониды – вязкие жидкости или твердые вещества, чрезвычайно взрывчатые. Обычно их не выделяют, а сразу разлагают водой, при этом получаются пероксид водорода, альдегиды и кетоны:
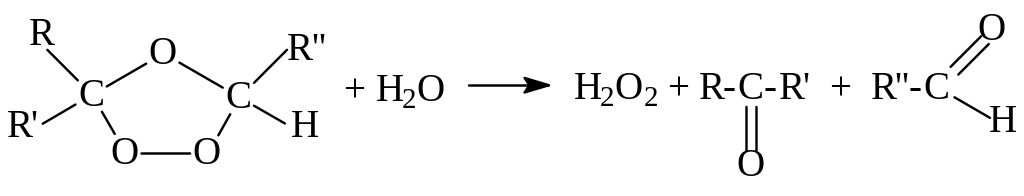
Идентифицируя полученные соединения, можно определить положение двойной связи в молекуле алкена.
ж) Реакции алкенов с сохранением двойной связи – это реакции замещения в аллильное положение.
1) Алкены легко окисляются в аллильном положении по радикальному механизму в присутствии пероксидов. Продуктами окисления являются аллильные гидропероксиды:

CH3-CH2-CH=CH2 + O2
2) При высокой температуре (> 500 С) пропилен хлорируется в аллильное положение (реакция Львова):
500 С
CH2=CH-CH3 + Cl2 CH2=CH-CH2Cl + HCl
Чтобы отщепить водород из аллильного положения, нужно затратить меньше энергии, чем для отрыва Н от алкана, так как образуется стабильный аллильный радикал.
