
- •Лекція 4
- •4.1. Теплоємність. Означення
- •4.1.1. Методи обчислення кількости тепла
- •1) Внутрішньої енергії
- •2) Ентальпії
- •3) Ентропії
- •4.1.2. Загальне означення теплоємности. Істинна і питома теплоємности
- •4.1.3. Обчислення кількости тепла за істинною і середньою теплоємностями
- •1 − Лінійна залежність; 2− нелінійна залежність
- •4.1.4. Геометричні образи істинної і середньої теплоємностей
- •4.2. Ізобарна та ізохорна теплоємности. Рівняння Майєра
- •4.2.1. Геометричні образи ізохорної та ізобарної теплоємностей
- •4.2.2. Зв’язок ізобарної та ізохорної теплоємностей
- •4.2.2.1. Рівняння Майєра для ідеального ґазу
- •1. Ізохорна та ізобарна теплоємности
- •2. Зв’язок між ізобарною та ізохорною теплоємностями
- •6. Рівняння Лежандра. Термодинамічна та ефективна робота
- •4.2.2.2. Рівняння Майєра для неідеального ґазу
- •4. Для неідеального ґазу, що підпорядковується рівнянню Ван-дер-Ваальса : (4.123)
- •5.3. Зв’язок теплоємности з коефіцієнтом стискуваности ґазу
- •4 .4. Теплоємність під час оборотнього політропного процесу ідеального ґазу
- •4.5. Диференціяльні рівняння теплоємности Виходячи з другого начала термодинаміки та визначення теплоємности
- •4.6. Залежність ізобарної та ізохорної теплоємностей від тиску та об’єму
- •4.7. Зв’язок теплоємности з ентропією. Диференціяльні рівняння ентропії
- •4.8. Залежність теплоємности ґазів від температури
- •4.8.1. Залежність ізобарної та ізохорної теплоємностей ґазів від температури
- •4.8.2. Залежність теплоємности від атомности ґазів і температури
- •4.9. Теплоємність рідин
- •4.10. Теплоємність твердих тіл
- •4.10.1. Молекулярно-кінетична теорія. Закон Дюлонґа і Пті
- •5.10.2. Квантова теорія Дебая
- •4 .10.3. Теплоємність шарових структур
- •4.10.3.1. Структура невзаємодіючих шарів
- •4.10.3.2. Структура із взаємодіючими шарами
4. Для неідеального ґазу, що підпорядковується рівнянню Ван-дер-Ваальса : (4.123)
![]() (4.124)
(4.124)
![]() .
(4.125)
.
(4.125)
5.
Для фотонного ґазу
![]() .
.
5.3. Зв’язок теплоємности з коефіцієнтом стискуваности ґазу
Із
співвідношенням
пов’язане співвідношення
![]() ,
,
де коефіцієнт адіабатної стискуваности:
![]() ,
(4.126)
,
(4.126)
а коефіцієнт ізотермної стискуваности:
![]() .
(4.127)
.
(4.127)
Так як
![]() ,
то КS,
Kt >
0. (4.128)
,
то КS,
Kt >
0. (4.128)
У рівняння адіабати
 (4.129)
(4.129)
підставимо вираз
![]() ,
(4.130)
,
(4.130)
отримаємо
![]() (4.131)
(4.131)
![]() .
(4.132)
.
(4.132)
Продиференціюємо рівняння (4.132) за dV при S=const, отримаємо:
![]() (4.133)
(4.133)
Звідки
![]() (4.134)
(4.134)
За допомогою рівняння
![]() (4.135)
(4.135)
запишемо для змінних x=V, y=p, z=T добуток частинних похідних:
![]() .
(4.136)
.
(4.136)
Представимо (4.136) у вигляді:
![]() (4.137)
(4.137)
і підставимо вираз (4.137) в рівняння (4.134), отримаємо:
![]() .
(4.138)
.
(4.138)
Звідки
 ;
(4.139)
;
(4.139)
 .
(4.140)
.
(4.140)
Враховуючи рівняння (4.126) і (4.127), отримаємо:
![]() .
(4.141)
.
(4.141)
Звідки
![]() .
(4.142)
.
(4.142)
4 .4. Теплоємність під час оборотнього політропного процесу ідеального ґазу
З рівняння
![]() (4.143)
(4.143)
для політропного кінцевого процесу 1→2 витікає (після інтегрування):
![]() .
(4.144)
.
(4.144)
Відомо,
що
![]() ,
або в інтегральній формі (при сV=const)
,
або в інтегральній формі (при сV=const)
![]() ,
(4.145)
,
(4.145)
то робота в політропному процесі
![]() .
(4.146)
.
(4.146)
Тоді (4.144) перетвориться у вираз:
![]() (4.147)
(4.147)
де
![]() − показник політропи. Коли
− показник політропи. Коли
![]() (випадок сталої
(випадок сталої
![]() )
і можливість інтеґрування рівняння
)
і можливість інтеґрування рівняння
![]() .
.
Врахуємо в (4.147) такі співвідношення:
![]() ;
;
![]() − показник ізоентропи (оборотньої
адіабати), коли
− показник ізоентропи (оборотньої
адіабати), коли
![]() (випадок
(випадок
![]() сталої
теплоємности) і можливістю інтеґрування
рівняння
сталої
теплоємности) і можливістю інтеґрування
рівняння
![]() .
.
Тоді
 .
(4.148)
.
(4.148)
Із
визначення теплоємности
![]() маємо:
маємо:
 (4.149)
(4.149)
![]() ,
(4.150)
,
(4.150)
де
−
показник політропи
![]() ;
;
![]() −
показник
адіабати
.
−
показник
адіабати
.
Як
видно з (4.150) величина теплоємности
ідеального ґазу, залежить від показників
політропи
![]() та адіабати для даного ґазу і заданого
інтервалу температур.
та адіабати для даного ґазу і заданого
інтервалу температур.
Проаналізуємо отримане співвідношення (4.150) для обчислення політропної теплоємности ідеального ґазу:
1) для групи політропних процесів розширення рівняння (4.150) представимо у вигляді:
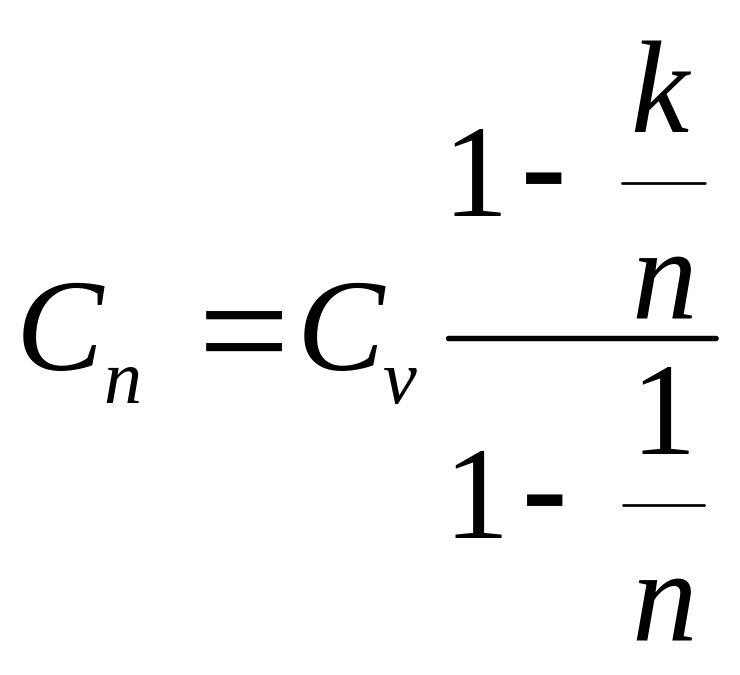 ,
(4.151)
,
(4.151)
а)
при
![]() ,
,
![]() ,
,
![]() ,
тоді
,
тоді
![]() .
(4.152)
.
(4.152)
З
рівняння
,
після перетворення
![]() ,
отримаємо
,
отримаємо
![]() ;
при
;
при
![]() ,
,
![]() ,
маємо ізохору
,
маємо ізохору
![]() .
.
З
![]() ═>
═>
![]() ,
,
![]() .
(4.153)
.
(4.153)
Для
політропного процесу з показником
![]() політропна теплоємність дорівнює
ізохорній
політропна теплоємність дорівнює
ізохорній![]() ;
;
б)
при
![]() ,
,
![]() ;
;
в)
з рівняння (4.150) при
![]() ,
,
![]() ,
а коефіцієнт Пуассона
,
то
,
а коефіцієнт Пуассона
,
то
![]() .
(4.154)
.
(4.154)
З
рівняння
,
![]() ,
,
![]() ,
,
![]() .
.
Для
політропного процесу з показником
політропи
політропна теплоємність дорівнює
ізобарній
![]() ;
;
г)
при
![]() ,
,
![]() ;
(4.155)
;
(4.155)
ґ)
при
![]() ,
,
![]() (4.156)
(4.156)
(І група політропних процесів розширення зображена на рис.4.8);
д)
при
![]() знаменник рівняння (4.150)
знаменник рівняння (4.150)
![]() ,
,
то![]() ,
,
![]() ,
,
![]() .
(4.157)
.
(4.157)
Для політропного процесу з показником політропи політропна теплоємність є ізотермна;
е)
при
![]() ,
,
![]() (ІІ група політропних процесів розширення);
у цих процесах розширення газ виконує
роботу, яка перевищує ту кількість
тепла, що підводиться до ґазу в процесі
розширення. Решту енергії на виконання
роботи витрачається за рахунок частини
внутрішньої енергії, що веде до зниження
температури ґазу. Тобто є випадок, коли
тепло до системи підводиться, але
температура системи зменшується:
(ІІ група політропних процесів розширення);
у цих процесах розширення газ виконує
роботу, яка перевищує ту кількість
тепла, що підводиться до ґазу в процесі
розширення. Решту енергії на виконання
роботи витрачається за рахунок частини
внутрішньої енергії, що веде до зниження
температури ґазу. Тобто є випадок, коли
тепло до системи підводиться, але
температура системи зменшується:
![]() ,
то
.
(4.158)
,
то
.
(4.158)









p
n<0 CV < Cn<Cp

n = 0 (p=const) Cn = Cp a
0 <n <1 Cn >Cp
n=1 (pV = const) Cn =Ct→ ± ∞
1<n<K Cn < 0
n > k n=k(pVk=const) Cn = CS = 0
n → ± ∞ (V = const)
Cn = CV
 V
V


 T
0<Cn<CV
Cn
= CV
(n→ ± ∞) V = const
T
0<Cn<CV
Cn
= CV
(n→ ± ∞) V = const


 CV
< Cn
<Cp
CV
< Cn
<Cp
 Cn
= Cp
(n = 0) p = const
Cn
= Cp
(n = 0) p = const

 Cn
> Cp
Cn
> Cp
b
 Ct
→ ± ∞ (n = 1) T = const
Ct
→ ± ∞ (n = 1) T = const
Cn < 0
Cn = 0 (n = K) S = const
 S
S
Рис.4.8. Політропні процеси, які зображені в р-v (a) і T-s (б) координатах
є)
при
![]() ,
,
![]() (4.159)
(4.159)
![]() – це рівняння адіабати, то для політропного
процесу з показником політропи
політропна теплоємність дорівнює
оборотній адіабатній (ізоентропній)
теплоємности;
– це рівняння адіабати, то для політропного
процесу з показником політропи
політропна теплоємність дорівнює
оборотній адіабатній (ізоентропній)
теплоємности;
ж)
при
![]() ,
,
![]() (4.160)
(4.160)
(ІІІ група політропних процесів розширення);
з)
далі
,
![]() і т.і. (4.161)
і т.і. (4.161)
Далі попередній зміст повторюється для груп політропних процесів стискання (рис.4.8).
Залежність теплоємности політропного процесу від величини показника політропи зображена на рис.4.9.
Тут
![]() ,
, ![]()
![]() (4.162)
(4.162)
,
![]()
