
- •Внутренняя энергия и энтальпия. 1 закон термодинамики. Термодинамические расчеты.
- •2) Энтропия, ее изменения при фазовых переходах и химических процессах. 2 и 3 законы термодинамики.
- •3) Энергия Гиббса. Термодинамическая оценка возможности реакций.
- •4) Понятия о химическом потенциале. Направление протекания процессов.
- •5) Химическое в гомогенных системах.
- •6) Константа равновесия. Зависимость константы равновесия от температуры.
- •7) Равновесие в гетерогенных системах.
- •8) Понятие скорости реакции.
- •9) Зависимость скорости реакции от концентрации реагентов. Закон действующих масс.
- •10) Температурная зависимость константы скорости.
- •11) Теория переходного состояния. Энергия активации. Суть теории переходного состояния (активированного комплекса):
- •13) Диффузия. Законы Фика.
- •12) Механизм и кинетика взаимодействия компонентов в гомогенных газообразных средах. Молекулярность и порядок реакций.
- •14) Особенности диффузионных процессов в твердых телах.
- •15) Влияние дефектов структуры на процесс диффузии. Кристаллизация сплавов. Процессы образования и роста зародышей новой фазы.
- •17) Правило фаз Гиббса.
- •19) Виды взаимодей-я компонентов в сплавах.
- •18) Условия равновесия фаз. Виды фазовых превращений.
- •21) Диаграмма состояния сплавов, образующих неограниченные твердые растворы.
- •23) Перитектическая кристаллизация, перитектоидное превращение.
- •22) Диаграмма состояния сплавов, образующих ограниченные твердые растворы.
- •27) Магнитное превращение.
- •24) Количественных расчет по диаграммам состояния. Правило отрезков.
- •25) Правило Курнакова. Связь между типом диаграммы состояния и свойствами сплавов.
- •26) Полиморфные превращения.
- •28) Особенности мартенситного превращения.
- •29) Распад пересыщенного твердого раствора. Процессы старения.
- •30) Спиноидальный распад.
- •31) Упорядочение атомов.
- •32) Понятие об адсорбции. Физическая адсорбция и хемосорбция.
- •34) Особенности адсорбции из растворов.
- •35) Поверхностно-активные вещества.
- •33) Изотермы адсорбции.
- •36) Явление смачивания.
- •37) Растворы. Парциальные мольные величины.
- •38) Совершенные растворы. Реальные растворы. Активность.
- •39) Равновесие в системе "жидкость - пар". Закон Рауля.
- •40) Закон распределения. Экстракция.
- •41) Теоретические основы процессов дистилляции, сублимации, ректификации металлов и их соединений.
- •42) Физико-химич. Основы зонной плавки.
- •43) Км. Общее понятие и классификация.
- •45) Межфазное взаимодействие в композиционных материалах. Выбор материала матриц и волокон.
23) Перитектическая кристаллизация, перитектоидное превращение.
Перитектическое превращение – процесс взаимодействия кристаллов твердого раствора с жидкостью, происходящий при постоянной температуре и постоянной концентрации фаз, приводящий к образованию кристаллов другого твердого раствора.
Перитектоидное превращение – фазовое превращение в твердом состоянии при охлаждении, заключающееся в образовании одной новой фазы из двух других; полностью обратимо при нагреве.
Некоторые промежуточные фазы образуются в результате взаимодействия двух твердых фаз по реакции, аналогичной перитектической, которая называется перитектоидной .
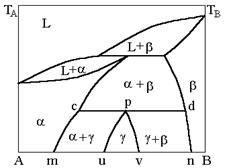 В
рассматриваемом примере промежуточная
фаза g образуется при взаимодействии
граничных твердых растворов: ac + bd --->
gp, превращение, в соответствии с правилом
фаз Гиббса, протекает при постоянной
температуре и неизменных составах всех
фаз.В зависимости от состава сплава
перитектоидная реакция заканчивается
по–разному: с одновременным исчезновением
обеих исходных фаз aс и bd (сплав состава
точки р) или только одной из этих фаз
В
рассматриваемом примере промежуточная
фаза g образуется при взаимодействии
граничных твердых растворов: ac + bd --->
gp, превращение, в соответствии с правилом
фаз Гиббса, протекает при постоянной
температуре и неизменных составах всех
фаз.В зависимости от состава сплава
перитектоидная реакция заканчивается
по–разному: с одновременным исчезновением
обеих исходных фаз aс и bd (сплав состава
точки р) или только одной из этих фаз
22) Диаграмма состояния сплавов, образующих ограниченные твердые растворы.
На рис. 1. точка d характеризует предельную растворимость компонентаβ в компонентеα , а точка с компонентаα в компонентаβ. Сплав, соответствующий точке 3, затвердевает при постоянной температуре Т4. При температуре несколько ниже жидкий сплав оказывается насыщенным по отношению к обеим фазам (α и β- твердым растворам), так как точка 3 принадлежит сразу двум ветвям ликвидуса. Поэтому из жидкости состава 3 при температуре Т4 одновременно выделяются предельно насыщенные кристаллы твердого раствора αd и βc, образующие механическую смесь.
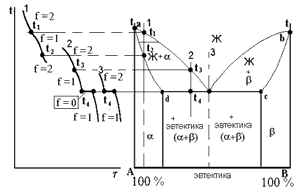
Сплавы, в которых происходит одновременная кристаллизация α и β фаз при постоянной и самой низкой для данной системы сплавов температуре, называют эвтектическими. Структура, состоящая из механической смеси двух (или более) твердых фаз, одновременно кристаллизовавшихся из жидкого сплава, называется эвтектикой. В переводе с греческого - “легкоплавящаяся”. Сплавы, располагающиеся влево от эвтектического состава и имеющие концентрацию в пределах точек d b 3, называются доэвтектическими, а справа в пределах концентрации точек 3 и с - заэвтектическими. При кристаллизации эвтектик сначала зарождаются и растут кристаллы α твердого раствора, богатого компонентом А. Жидкость, окружающая этот кристалл, обогащается вторым компонентом В, и в результате этого происходит выделение кристалликов α и β- твердого раствора. Жидкость, прилегающая к образовавшимся кристалликам β фазы, в свою очередь, обогащается металлом А, и поэтому вновь выделяются кристаллики α- фазы, богатые компонентом А. В результате переменного пересыщения жидкости по отношению кα иβ - фазам образуется эвтектическая колония.
Процесс кристаллизации эвтектики протекает при постоянной температуре, так как согласно правилу фаз при одновременном существовании трех фаз постоянного состава система безвариантна. На кривой охлаждения образуется площадка. Одновременно кристаллизуются две фазы. После затвердевания сплав состоит из кристаллов эвтектики.
