
- •Внутренняя энергия и энтальпия. 1 закон термодинамики. Термодинамические расчеты.
- •2) Энтропия, ее изменения при фазовых переходах и химических процессах. 2 и 3 законы термодинамики.
- •3) Энергия Гиббса. Термодинамическая оценка возможности реакций.
- •4) Понятия о химическом потенциале. Направление протекания процессов.
- •5) Химическое в гомогенных системах.
- •6) Константа равновесия. Зависимость константы равновесия от температуры.
- •7) Равновесие в гетерогенных системах.
- •8) Понятие скорости реакции.
- •9) Зависимость скорости реакции от концентрации реагентов. Закон действующих масс.
- •10) Температурная зависимость константы скорости.
- •11) Теория переходного состояния. Энергия активации. Суть теории переходного состояния (активированного комплекса):
- •13) Диффузия. Законы Фика.
- •12) Механизм и кинетика взаимодействия компонентов в гомогенных газообразных средах. Молекулярность и порядок реакций.
- •14) Особенности диффузионных процессов в твердых телах.
- •15) Влияние дефектов структуры на процесс диффузии. Кристаллизация сплавов. Процессы образования и роста зародышей новой фазы.
- •17) Правило фаз Гиббса.
- •19) Виды взаимодей-я компонентов в сплавах.
- •18) Условия равновесия фаз. Виды фазовых превращений.
- •21) Диаграмма состояния сплавов, образующих неограниченные твердые растворы.
- •23) Перитектическая кристаллизация, перитектоидное превращение.
- •22) Диаграмма состояния сплавов, образующих ограниченные твердые растворы.
- •27) Магнитное превращение.
- •24) Количественных расчет по диаграммам состояния. Правило отрезков.
- •25) Правило Курнакова. Связь между типом диаграммы состояния и свойствами сплавов.
- •26) Полиморфные превращения.
- •28) Особенности мартенситного превращения.
- •29) Распад пересыщенного твердого раствора. Процессы старения.
- •30) Спиноидальный распад.
- •31) Упорядочение атомов.
- •32) Понятие об адсорбции. Физическая адсорбция и хемосорбция.
- •34) Особенности адсорбции из растворов.
- •35) Поверхностно-активные вещества.
- •33) Изотермы адсорбции.
- •36) Явление смачивания.
- •37) Растворы. Парциальные мольные величины.
- •38) Совершенные растворы. Реальные растворы. Активность.
- •39) Равновесие в системе "жидкость - пар". Закон Рауля.
- •40) Закон распределения. Экстракция.
- •41) Теоретические основы процессов дистилляции, сублимации, ректификации металлов и их соединений.
- •42) Физико-химич. Основы зонной плавки.
- •43) Км. Общее понятие и классификация.
- •45) Межфазное взаимодействие в композиционных материалах. Выбор материала матриц и волокон.
38) Совершенные растворы. Реальные растворы. Активность.
Свойства совершенных ионных растворов: а) раствор состоит только из ионов; б) одноименно заряженные ионы равноценны по размерам и заряду; в) ближайшие соседи любого иона имеют противоположный заряд, т.е. анионы могут меняться местами только с анионами, а катионы - только с катионами:
Таким образом, совершенный раствор, как и обычный идеальный раствор, характеризуется равномерным распределением частиц, но отличается от него дополнительным порядком расположения ионов, обусловленным их зарядом. Поскольку на местах одних катионов становятся энергетически равноценные им другие катионы, а на местах одних анионов - эквивалентные им по взаимодействию другие анионы, теплоты смешения при образовании совершенного ионного раствора из компонентов принимается равной нулю.
В случае идеальных растворов из измерения одного из свойств (давление пара) можно рассчитать все другие свойства. Решение было предложено Льюисом, который ввел в теорию растворов так называемые т/д активности в качаестве ф-ии, связывающей свойства равствора друг с другом и заменил концентрацию в реальных растворах. Подставляя т/д активность в место концентрации, в т/д уравнение, полученное для идеальных растворов делает последнее пригодным и для реальных растворов. Т.о. активностью называется величина, подставляя которую вместо концентрации в т/д уравнение делает последнее применимым для реальных растворов, а – активность.
Активность
должна быть введена таким образом чтобы
в идеальных растворах она совпадала с
концентрацией, а в реальных растворах
она должна характеризовать отклонение
их от идеальных. По Льюису активность
выражается соотношением давление пара
данного компонента над реальным
раствором к давлению пара этого
компонента в некотором стандартном
состоянии ![]()
39) Равновесие в системе "жидкость - пар". Закон Рауля.
Имеется р-р (гомогенная система перменного состава, состоящая из нескольких компонентов. Закон Рауля: упругость пара над рас-ром всегда ниже, чем над чистым растворителем, причем относит-е ↓ упругости пара равно мольной доле растворенного вещ-ва.
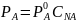
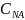 -
мольная доля компонента А.
-
мольная доля компонента А.
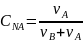
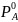 – упругость
пара над чистым компонентом
– упругость
пара над чистым компонентом
Если 2 компонента:
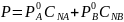 (1)
(1)
рис
Cоот. (1) справедливо только для идеаль. р-ров
В реаль. р-рах всегда набл-ся отклоненик от закона Рауля (положит. и отриц отклонения)
40) Закон распределения. Экстракция.
Рассм. сист. состоящую из 2-х нераств. друг в друге жид-тей. Третий компонент раств-ся в этих жидкостях. Распределение концентрации комп-та в 2-х этих фазах величина постоянная
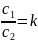
это рав-во соблюдается при условии, что молярная масса компонентов одинаковы в обеих жидкостях и комп-ы не влияют на взаимную растворимость жидкостей.
На этом законе основан метод ЭКСТРАКЦИИ – метод выделения вещ-ва из раствора путем добавления какого-то рас-ля, нерастворяющегося в исх. рас-ре, при этом раствор-ть выделяемого вещ-ва в новом раств-ле должна быть выше чем в исходном.
