- •1. Органическая химия: определение, задачи
- •2. Классификация органических сединений
- •3. Теория строения Бутлерова
- •4. Взаимное влияние атомов в молекуле и её природа
- •5. Эффекты сопряжения и сверхсопряжения
- •6. Предельные углеводороды
- •7. Химические свойства предельных углеводородов
- •1.Радикальное галогенирование
- •2. Нитрование
- •3.Сульфирование, сульфоокисление, сульфохлорирование
- •4.Окисление
- •5.Крекинг углеводородов при высоких температурах
- •8. Этиленовые углеводороды
- •9. Общая характеристика алкенов
- •10. Ацетиленовые углеводороды
- •11. Химические свойства ацетиленовых углеводородов
- •2.Галогенирование
- •3.Гидрогалогенирование
- •9. Полимеризация
- •12.Типы диеновых углеводородов
- •1.Гидрирование
- •2.Галогенирование
- •13. Алициклические углеводороды
- •14. Современные представления об устойчивости циклов
- •15. Ароматические углеводороды
- •16. Строение бензола
- •17. Химические свойства ароматических углеводородов
- •1.Реакции присоединения
- •2.Реакции окисления
- •3.Реакции замещения
- •18. Механизм электрофильного замещения в ряду бензола
- •19. Правила ориентации в ряду бензола
- •20. Галогенопроизводные углеводородов
- •21. Химические свойства галогенопроизводных
- •2.Реакции замещения
- •3.Реакции по бензольному кольцу
- •22. Нитросоединения
- •23. Амины
- •24. Спирты и фенолы
- •25. Карбонильные соединения
- •26. Общие и отличительные свойства альдегидов и кетонов
- •27. Карбоновые кислоты
- •28. Химические свойства карбоновых кислот
- •29. Гетероциклические соединения
- •30. Липиды
- •31. Простые липиды
- •32. Углеводы
- •33. Моносахариды
- •34. Дисахариды
- •35. Высокомолекулярные полисахариды
- •36.Аминокислоты
- •37. Пептиды
- •38. Белки
- •39. Способы получения оксикислот
- •40. Способы получения оксокислот
- •Способы получения
- •Химические особенности
9. Общая характеристика алкенов
10. Ацетиленовые углеводороды
Алкинами называют углеводороды, содержащие кроме σ-связей две π-связи (тройную связь) у одной пары углеродных атомов. Общая формула гомологического ряда ацетиленовых углеводородов СnH2n-2. Родоначальником этого ряда является ацетилен.
Изомерия и номенклатура
Ацетиленовые углеводороды по номенклатуре ИЮПАК называют, пользуясь теми же правилами, что и в случае предельных углеводородов, но суффикс «ан» заменяется суффиксом «ин». Главная цепь выбирается так, чтобы в нее попала тройная связь, а нумеруется с того конца, к которому ближе тройная связь.
Простейшие ацетиленовые углеводороды часто называют как алкилзамещенные ацетилена, т.е. по рациональной номенклатуре:

4-метил-1-пентин 4-метил-2-пентин
Изобутилацетилен метилизопропилацетилен
Изомерия ацетиленовых углеводородов определяется как строением углеродного скелета, так и положением тройной связи.
Способы получения.
Ацетиленовые углеводороды получают либо алкилированием ацетилена, либо отщеплением галогеноводородов или галогенов от полигалогенопроизводных.
1. Ацетилен можно получить при высокотемпературном крекинге метана:
![]()
а также при гидролизе карбида кальция:
СаС2 + 2Н2О → СН≡СН + Са(ОН)2
2. Алкилирование ацетилена осуществляют, превращая ацетилен в металлоорганические соединения:
СН≡СН +NaNH2 → CH≡C–Na + NH3
ацетиленид натрия
CH≡C–Na + СH3J → CH≡C–СH3 + NaJ
пропин
3. Ацетиленовые углеводороды образуются при действии спиртовой щелочи на дигалогенопроизводные предельных углеводородов, содержащих галогены у одного или соседних атомов углерода:
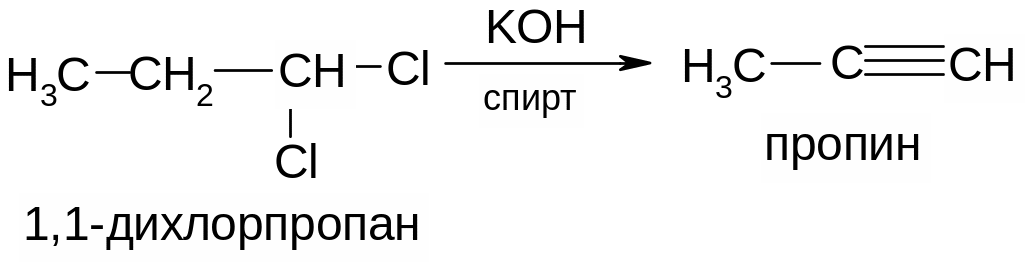

11. Химические свойства ацетиленовых углеводородов
При рассмотрении химических свойств алкинов следует учитывать особенности тройной связи: по сравнению с алкенами алкины несколько менее активны в реакциях электрофильного присоединения и более активны в реакциях с нуклеофилами (вода, алкоголяты, амины). Эти особенности ацетиленовой группировки объясняются ее строением. Оба углеродных атома в ацетилене находятся в sp-гибридном состоянии. Между тем, чем больше доля s-орбитали в гибридном состоянии, тем ближе электроны находятся к ядру и, следовательно, тем труднее эти электроны вовлекаются в химические превращения с участием электрофилов.
1.Гидрирование
Водород присоединяется по месту тройной связи в присутствии тех же катализаторов, что и по месту двойной связи: