
- •1. Органическая химия: определение, задачи
- •2. Классификация органических сединений
- •3. Теория строения Бутлерова
- •4. Взаимное влияние атомов в молекуле и её природа
- •5. Эффекты сопряжения и сверхсопряжения
- •6. Предельные углеводороды
- •7. Химические свойства предельных углеводородов
- •1.Радикальное галогенирование
- •2. Нитрование
- •3.Сульфирование, сульфоокисление, сульфохлорирование
- •4.Окисление
- •5.Крекинг углеводородов при высоких температурах
- •8. Этиленовые углеводороды
- •9. Общая характеристика алкенов
- •10. Ацетиленовые углеводороды
- •11. Химические свойства ацетиленовых углеводородов
- •2.Галогенирование
- •3.Гидрогалогенирование
- •9. Полимеризация
- •12.Типы диеновых углеводородов
- •1.Гидрирование
- •2.Галогенирование
- •13. Алициклические углеводороды
- •14. Современные представления об устойчивости циклов
- •15. Ароматические углеводороды
- •16. Строение бензола
- •17. Химические свойства ароматических углеводородов
- •1.Реакции присоединения
- •2.Реакции окисления
- •3.Реакции замещения
- •18. Механизм электрофильного замещения в ряду бензола
- •19. Правила ориентации в ряду бензола
- •20. Галогенопроизводные углеводородов
- •21. Химические свойства галогенопроизводных
- •2.Реакции замещения
- •3.Реакции по бензольному кольцу
- •22. Нитросоединения
- •23. Амины
- •24. Спирты и фенолы
- •25. Карбонильные соединения
- •26. Общие и отличительные свойства альдегидов и кетонов
- •27. Карбоновые кислоты
- •28. Химические свойства карбоновых кислот
- •29. Гетероциклические соединения
- •30. Липиды
- •31. Простые липиды
- •32. Углеводы
- •33. Моносахариды
- •34. Дисахариды
- •35. Высокомолекулярные полисахариды
- •36.Аминокислоты
- •37. Пептиды
- •38. Белки
- •39. Способы получения оксикислот
- •40. Способы получения оксокислот
- •Способы получения
- •Химические особенности
17. Химические свойства ароматических углеводородов
Ароматические углеводороды обладают большей склонностью к реакциям замещения, чем к реакциям присоединения. Характерна также большая устойчивость бензольного кольца к окислителям.
1.Реакции присоединения
Реакции присоединения протекают обычно по трем кратным связям бензольного кольца одновременно.
1. Гидрирование бензола и его гомологов происходит в присутствии катализаторов (Ni, Pt, Pd) при повышенной температуре:
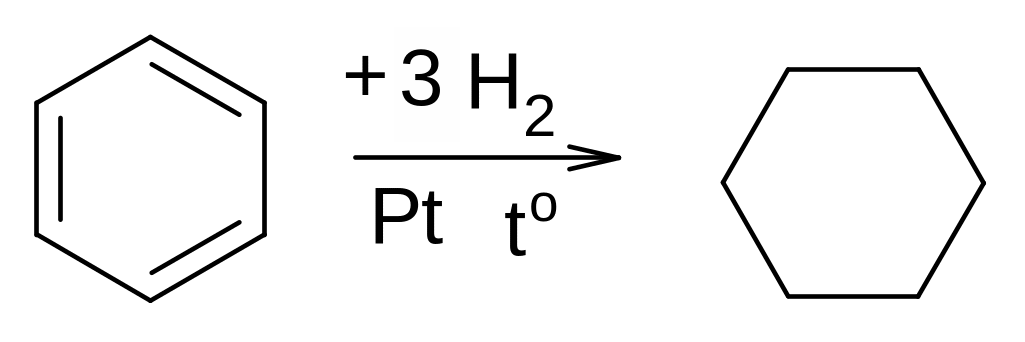
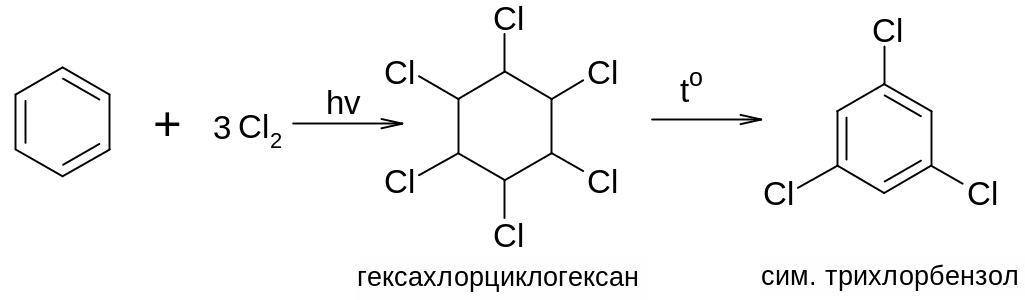
2. Если раствор хлора или брома в бензоле подвергнуть действию солнечного света или ультрафиолетовых лучей, то происходит быстрое присоединение трех молекул галогена. Продукты присоединения при нагревании теряют три молекулы галогеноводорода и дают тригалогенбензол:
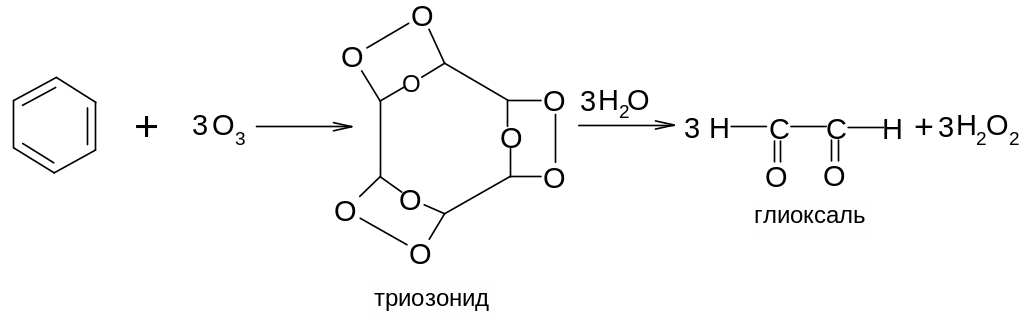
3. Бензол и его гомологи присоединяют озон с образованием чрезвычайно взрывоопасных триозонидов, которые разлагаются на карбонильные соединения под действие воды. Эта реакция используется для доказательства строения ароматических соединений:
2.Реакции окисления
Бензольное кольцо устойчиво к действию окислителей. Такие окислители как перманганат калия, оксид хрома (+6), азотная кислота на бензол не действуют.
1. При окислении бензола кислородом воздуха на оксиде ванадия (+5) образуется малеиновый ангидрид:
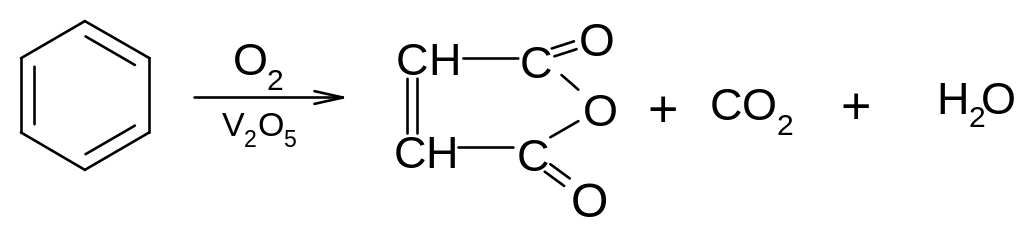
малеиновый ангидрид
2. При окислении гомологов бензола кислородом воздуха образуются гидропероксиды. В реакции принимает участие углеродный атом в α-положении к бензольному кольцу:
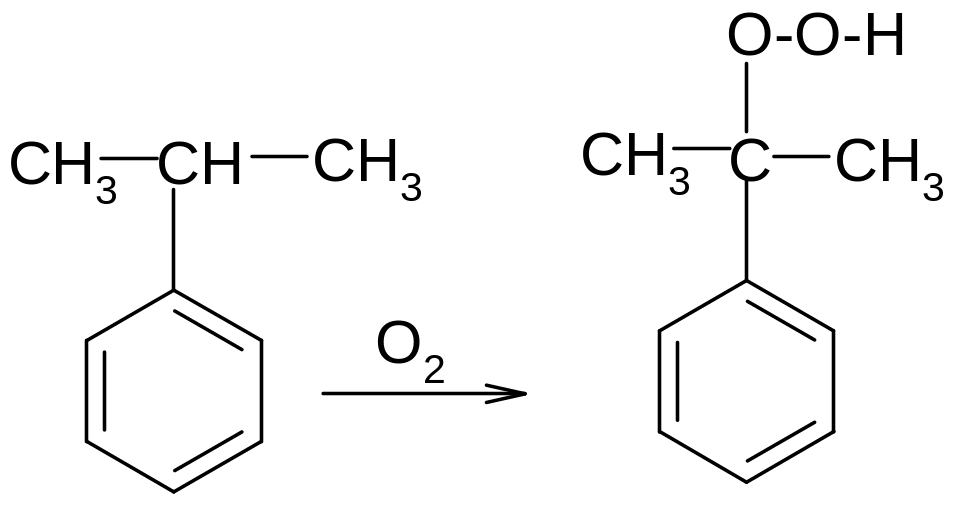
кумол гидроперекись кумола
3. При действии окислителей на гомологи бензола окисляется боковая цепь. Независимо от длины боковой цепи она дает карбоксильную группу:

толуол бензойная кислота
Следует отметить, что третичные алкильные группы, связанные с бензольным кольцом, устойчивы к окислению; бензольное кольцо окисляется легче, чем эти группы.
3.Реакции замещения
1. В присутствии катализаторов (FeCl3, AlCl3) хлор и бром не присоединяются к бензолу, но замещают атомы водорода в его молекуле:
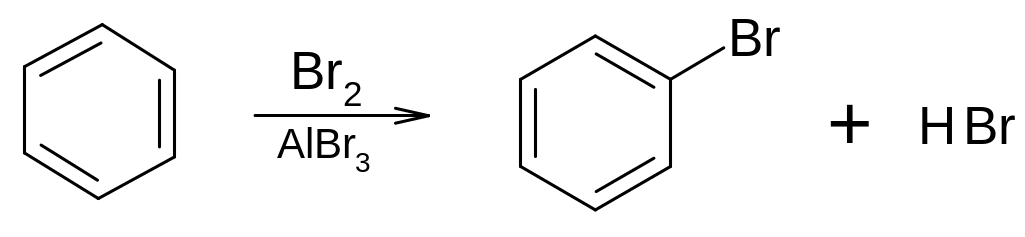
бромбензол
2. Концентрированная серная кислота не вызывает полимеризации бензола, как это происходит в случае алкенов и алкадиенов, а приводит к образованию бензолсульфокислоты:
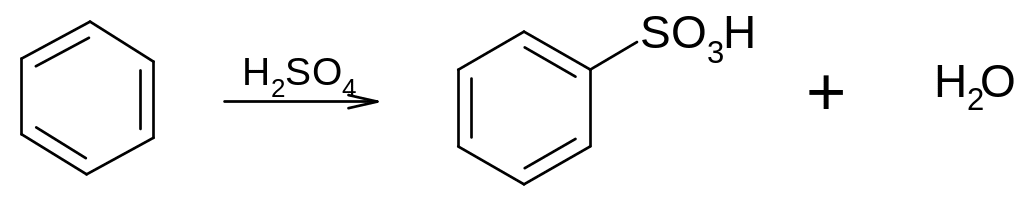
Бензолсульфокислота
3. При действии нитрующей смеси (концентрированная азотная и серная кислоты) происходит нитрование ядра:
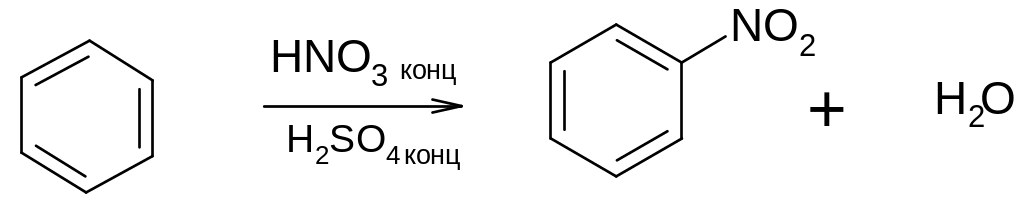
нитробензол
Механизм этих реакций электрофильный. Он осуществляется и при протекании реакций алкилирования, ацилирования, азосочетания.
Механизм электрофильного замещения в бензольном кольце разберем на примере реакции галогенирования.
Под действием катализатора образуется активная форма электрофильного реагента:
![]()
Стадией, определяющей скорость реакции, является образование σ-комплекса:
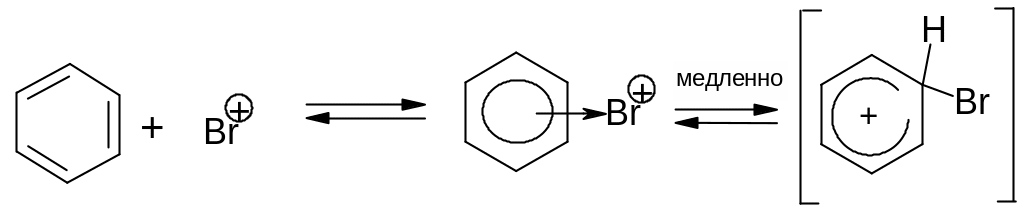
π-комплекс σ-комплекс
π-Комплекс – это промежуточное состояние, в котором реагирующие частицы сориентировались относительно друг друга.
