- •Маркеры в-клеток
- •Леточный иммунный ответ. Гуморальный иммунный ответ. Защитные функции иммуноглобулинов ( антител ).
- •Гуморальный иммунный ответ
- •Механизм действия
- •Формирование и размножение цитотоксических т-лимфоцитов
- •8. Выброс продуктов деградации.
- •Антигенпрезентирующие клетки (апк)
- •Компоненты системы комплемента
- •Основные этапы активации системы комплемента.
- •Биологические функции
- •Классический путь
- •Альтернативный путь
- •Лектиновый (маннозный) путь активации системы комплемента
- •Роль системы комплемента при болезнях
- •Агаммаглобулинемия
- •Селективный IgA-дефицит
- •Вторичные иммунодефициты
- •Причины
- •Классификация
- •Стадии инфекционного процесса
- •Антитела к вич
- •Клинические стадии, классификация вич/спид
- •Клиническая классификация вич-инфекции в рф
- •Система ab0
- •Система Rh (резус-система)
- •Резус-фактор
- •Номенклатура Rh
- •Технология
- •Аллергия лекарственная : ложно-аллергические реакции
- •Ложная аллергия (псевдоаллергия)
- •Иммуноконфликтная беременность. Механизмы развития гемолитической болезни плода
- •Этиология и патогенез
- •Клиника
- •Лечение
- •Реакции гиперчувствительности третьего типа ( III типа ). Иммунокомплексный тип реакций. Феномен Артюса.
- •Реакции гиперчувствительности четвертого типа ( IV типа ). Гиперчувствительность замедленного типа. Реакции гиперчувствительности замедленного типа.
- •Классы hla
- •Отторжение трансплантанта. Реакция отторжения трансплантата. Клеточные реакции отторжения трансплантата. Аллоантитела. Типирование антигенов ( Аг ).
- •Клеточные реакции отторжения трансплантата
- •Аллоантитела
- •Типирование антигенов ( Аг )
- •Подбор тканей в системе «донор-реципиент»
- •Реакция трансплантат против хозяина. Кожные проявления реакции трансплантат против хозяина.
- •Механизм действия
- •Иммунологический надзор: преодоление его опухолевыми клетками
- •Опухолевые клетки и иммунитет: введение
- •Иммунный ответ противоопухолевый
- •Опухолеассоциированные антигены и иммунный ответ: введение
- •Натуральные киллеры: роль в иммунологическом надзоре
- •Ранняя диагностика
- •Возможные причины
- •Механизм развития
- •Прямая реакция Кумбса
- •Непрямая реакция
- •Реимущества
- •Иммунология
- •Сущность и классификация
- •Оценка иммунорегуляторного звена. Показатели иммунорегуляторного звена иммунитета
- •Методика определения групп крови
- •При работе с 3-я сыворотками групп о(I), а(II), в(III) возможны 4 комбинации реакций:
- •Определение резус-принадлежности крови
- •Клиническое значение определения циркулирующих иммунных комплексов (цик)
- •Кожные пробы
Прямая реакция Кумбса
Антитела, находящиеся на поверхности эритроцитов, могут быть как в статичном, так и в свободном состоянии в плазме крови. В зависимости от состояния антител проводится прямая или непрямая реакция Кумбса. Если есть основания для предположения, что антитела зафиксированы на поверхности эритроцитов, проводится прямой тест Кумбса. В этом случае тест проходит в один этап — добавляется антиглобулиновая сыворотка. Если на поверхности эритроцитов присутствуют неполные антитела, происходит агглютинация эритроцитов.
Непрямая реакция
Непрямая реакция Кумбса протекает в 2 этапа. Сначала необходимо искусственно осуществить сенсибилизацию эритроцитов. Для этого эритроциты и исследуемую сыворотку крови инкубируют, что вызывает фиксацию антител на поверхности эритроцитов. После чего проводится второй этап теста Кумбса — добавление антиглобулиновой сыворотки.
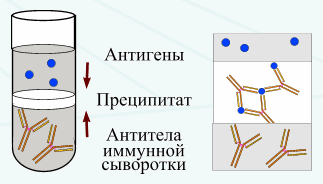
Реакция преципитации - РП (от лат praecipilo осаждать) - это формирование и осаждение комплекса растворимого молекулярного антигена с антителами в виде помутнения, называемого преципитатом. Он образуется при смешивании антигенов и антител в эквивалентных количествах, избыток одного из них снижает уровень образования иммунного комплекса. Реакцию преципитации ставят в пробирках (реакция кольцепреципитации), в гелях, питательных средах и др. Широкое распространение получили разновидности реакции преципитации в полужидком геле агара или агарозы двойная иммунодиффузия по Оухтерлони, радиапьная иммунодиффузия, иммуноэпектрофорез и др.
Реакция кольцепреципитации. Реакцию проводят в узких преципитационных пробирках: на иммунную сыворотку наслаивают растворимый антиген. При оптимальном соотношении антигена и антител на границе этих двух растворов образуется непрозрачное кольцо преципитата. Если в качестве антигенов в реакции используют прокипяченные и профильтрованные экстракты тканей, то такая реакция называется I реакцией-термопреципитации (реакция, при которой выявляют сибиреязвенный гаптен). |
|
Реакция двойной иммунодиффузии по Оухтерлони. Для постановки реакции растопленный агаровый гель тонким слоем выливают на стеклянную пластинку и после затвердевания в нем вырезают лунки. В лунки геля раздельно помещают антигены и иммунные сыворотки, которые диффундируют навстречу друг другу. В месте встречи в эквивалентных соотношениях они образуют преципитат в виде белой полосы. У многокомпонентных систем между лунками с антигенами и антителами появляется несколько линий преципитата; у идентичных АГ линии преципитата сливаются; у неидентичных АГ - пересекаются. |
|
Реакция радиальной иммунодиффузии. Иммунную сыворотку с расплавленным агаровым гелем равномерно наливают на стекло. После застывания в геле делают лунки, в которые помещают антиген в различных разведениях. Антиген, диффундируя в гель, образует с антителами кольцевые зоны преципитации вокруг лунок. Диаметр кольца преципитации пропорционален концентрации антигена. Реакцию используют для определения в сыворотке крови иммуноглобулинов различных классов, компонентов системы комплемента и др. |
|
Иммуноэлектрофорез - сочетание метода электрофореза и иммунопреципитации: смесь антигенов вносится в лунки геля и разделяется в геле с помощью электрофореза, затем в канавку параллельно зонам электрофореза вносят иммуннук сыворотку, антитела которой диффундируют в гель и образуют в месте "встречи" с антигеном линии преципитации. |
|
Реакция флоккуляции (по Рамону) (от лат . f1оecus - хлопья шерсти) - появление опалесценции или хлопьевидной массы (иммунопреципитации) в пробирке при реакции токсин - антитоксин или анатоксин - антитоксин. Ее применяют для определения активности антитоксической сыворотки или анатоксина. |
|
HLA типирование - исследование главного комплекса гистосовместимости человека - HLA комплекса. Это образование включает в себя область генов на 6-й хромосоме, которые кодируют HLA-антигены, участвующие в различных реакциях иммунного ответа.
Задачи при HLA типировании могут стоять самые разные - биологическая идентификация (HLA-тип наследуется вместе с родительскими генами), определение предрасположенности к различным заболеваниям, подбор доноров для пересадки органов - при этом производится сравнение результатов HLA типирования тканей донора и реципиента. С помощью HLA типирования определяют, и насколько супруги сходны или различимы по антигенам тканевой совместимости, чтобы диагностировать случаи бесплодия.
HLA типирование предполагает анализ полиморфизма HLA и проводится двумя методами - серологическим и молекулярно-генетическим. Классический серологический метод HLA типирования основан на микролимфоцитотоксическом тесте, а молекулярный метод использует проведение ПЦР (полимеразную цепную реакцию).
Серологическое HLA типирование проводится на выделенных клеточных популяциях. Антигены главного комплекса гистосовместимости несут на себе в основном лимфоциты. Поэтому суспензию Т лимфоцитов используют в качестве основных носителей антигенов I класса, и суспензию В лимфоцитов для определения антигенов HLA II класса. Для выделения необходимых клеточных популяций из цельной крови используют либо центрифугирование, либо иммуномагнитную сепарацию. Считается, что первый способ может привести к ложноположительным данным, так как при этом происходит гибель части клеток. Второй способ признан более специфичным - при этом более 95% клеток остаются жизнеспособными.
Но основой постановки лимфоцитотоксического теста HLA типирования является специфическая сыворотка, содержащая антитела к различным аллельным вариантам антигенов HLA I и II классов. Серологический тест позволяет определить HLA-тип путем изучения того, какие из сывороток реагируют с лимфоцитами, а какие - нет.
Если между клетками и сывороткой происходит реакция, в результате на поверхности клетки образуется комплекс антиген-антитело. После добавления раствора, содержащего комплемент, происходит лизис и гибель клетки. Оценивают серологический тест HLA типирования с помощью флуоресцентной микроскопии по оценке позитивной (красная флуоресценция) и негативной (зеленая флуоресценция) реакций, или фазово-контрастной микроскопии по окраске ядер погибших клеток. Результат HLA типирования выводят с учетом специфичности прореагировавших сывороток и перекрестно реагирующих групп антигенов, интенсивности реакции цитотоксичности.
Недостатками серологического HLA типирования являются наличие перекрестных реакций, слабое сродство антител или низкая экспрессия HLA-антигенов, отсутствие белковых продуктов у ряда HLA-генов.
Более современные, молекулярные методы HLA типирования используют уже стандартизованные синтетические образцы, которые реагируют не с антигенами на поверхности лейкоцитов, а с ДНК и прямо указывают на то, какие антигены присутствуют в пробе. Молекулярные методы не требуют живых лейкоцитов, любая человеческая клетка может быть подвержена изучению, и для работы достаточно несколько микролитров крови или можно ограничиться соскобом со слизистой оболочки рта.
Молекулярно-генетическое HLA типирование использует метод ПЦР, первым этапом которой является получение чистой геномной ДНК (из цельной крови, лейкоцитарной суспензии, тканей).
Затем образец ДНК копируется - амплифицируется в пробирке с использованием праймеров (коротких одноцепочечных ДНК), специфичных к определенному HLA -локусу. Концы каждого из пары праймеров должны быть строго комплементарны уникальной последовательности, соответствующей конкретному аллелю, в противном случае амплификация не осуществляется.
После ПЦР, в ходе многократного копирования, получается большое количество фрагментов ДНК, которое можно оценить визуально. Для этого реакционные смеси подвергают электролизу или гибридизации, и определяют, произошла ли специфическая амплификация, при помощи программы или таблицы. Результат HLA типирования представляется в форме всестороннего отчета на генном и аллельном уровнях. Из-за стандартизованности используемых образцов, молекулярное HLA типирование точнее серологического. Кроме того, оно дает больше информации (больше новых аллелей ДНК) и более высокий уровень ее детализации, поскольку позволяет идентифицировать не только антигены, но и сами аллели, обуславливающие, какой именно антиген присутствует на клетке.
Реакция иммунного лизиса. В основе реакции лежит способность специфических антител образовывать иммунные комплексы с клетками, в том числе с эритроцитами, бактериями, что приводит к активации системы комплемента по классическому пути и лизису клеток. Из реакций иммунного лизиса чаще других применяется реакция гемолиза и редко - реакция бактериолиза (главным образом при дифференциации Холерных и холероподобных вибрионов).
Реакция гемолиза. Под влиянием реакции с антителами в присутствии комплемента мутная взвесь эритроцитов превращается в ярко-красную прозрачную жидкость - «лаковую кровь» вследствие выхода гемоглобина. При постановке диагностической реакции связывания комплемента (РСК) реакция гемолиза используется как индикаторная: для тестирования присутствия или отсутствия (связывания) свободного комплемента.
Реакция локального гемолиза в геле (реакция Ерне) является одним из вариантов реакции гемолиза. Она позволяет определить число антителообразующих клеток. Количество клеток, секретирую-щих антитела - гемолизины, определяют по числу бляшек гемолиза, возникающих в агаровом геле, содержащем эритроциты, суспензию клеток исследуемой лимфоидной ткани и комплемент.
Иммунофлюоресцентный метод
(РИФ, реакция иммунофлюоресценции) - метод выявления специфических Аг (Ат) с помощью Ат (Аг), конъюгированных с флюорохромом. Обладает высокой чувствительностью и специфичностью. Применяется для экспресс-д-ки инфекц. заболеваний (идентификация возбудителя в иссл. материале), а также для определения Ат и поверхностных рецепторов и маркеров лейкоцитов (иммунофенотипирование) и др. клеток. Прямой И. м. состоит в обработке среза ткани или мазка из патологического материала или микробной к-ры с-кой, содержащей специфические Ат, конъюгированные с флюорохромом; препарат промывают для освобождения от несвязанных Ат и рассматривают в люминесцентный микроскоп. В положительных случаях по периферии объекта появляется светящийся иммунный комплекс. Необходим контроль для исключения неспецифического свечения. При непрямом. И. м. на первом этапе срез ткани или мазок обрабатывают нефлюоресцирующей специфической с-кой, на втором -люминесцирующей с-кой против-глобулинов того животного, с-ка к-рого была применена на первом этапе. В положительном случае образуется светящийся комплекс, состоящий из Аг, Ат к нему и Ат против Ат (сэндвич-метод). Кроме люминесцентного микроскопа для учета РИФ при фенотипировании клеток применяют лазерный сортировщик клеток.
Проточная цитометрия — метод оптического измерения параметров клетки, ее органелл и происходящих в ней процессов.
Методика заключается в выявлении рассеяния света лазерного луча при прохождении через него клетки в струе жидкости, причём, степень световой дисперсии позволяет получить представление о размерах и структуре клетки. Кроме того, в ходе анализа учитывается уровень флуоресценции химических соединений, входящих в состав клетки (аутофлуоресценция) или внесённых в образец перед проведением проточной цитометрии.
Клеточная суспензия, предварительно меченная флюоресцирующими моноклональными антителами или флуоресцентными красителями, попадает в поток жидкости, проходящий через проточную ячейку. Условия подобраны таким образом, что клетки выстраиваются друг за другом за счет т. н. гидродинамического фокусирования струи в струе. В момент пересечения клеткой лазерного луча детекторы фиксируют:
рассеяние света под малыми углами (от 1° до 10°) (данная характеристика используется для определения размеров клеток).
рассеяние света под углом 90° (позволяет судить о соотношении ядро/цитоплазма, а также о неоднородности и гранулярности клеток).
интенсивность флуоресценции по нескольким каналам флуоресцентности (от 2 до 18-20)- позволяет определить субпопуляционный состав клеточной суспензии и др.