
- •Химическое отделение вятский государственный гуманитарный университет
- •М. А. Зайцев основы биохимии
- •Часть 2
- •6. Нуклеиновые кислоты
- •6.1. Химический состав нуклеиновых кислот
- •6.2. Молекулярная масса нуклеиновых кислот
- •6.3. Локализация в клетке днк и рнк. Виды днк и рнк
- •6.4. Строение структурных элементов нуклеиновых кислот
- •6.5.1. Первичная структура днк
- •Генетический код
- •6.5.2. Вторичная структура днк
- •6.5.3. Третичная структура днк
- •6.5.4. Свойства днк
- •6.5.4.1. Репликация (редупликация, самоудвоение) днк
- •6.5.4.2. Транскрипция (синтез рнк)
- •6.6.1. Первичная структура рнк
- •6.6.2. Вторичная структура рнк
- •6.6.3. Третичная структура рнк
- •6.6.4. Классы рнк
- •6.6.5. Синтез белка (трансляция)
- •7. Общие понятия об обмене веществ и энергии в организме
- •7.1. Основные этапы обмена веществ
- •1 Этап. Подготовительный
- •2 Этап. Превращение строительных блоков (мономеров) в более простые соединения
- •3 Этап. Цикл Кребса (цикл ди- и трикарбоновых кислот, цтк)
- •4 Этап. Окислительная цепь ферментов (дыхательная цепь)
- •7.2. Обмен энергии. Макроэргические соединения
- •8. Биологическое окисление
- •8.1. Функции биологического окисления
- •8.2. Типы биологического окисления
- •II. Окисление, сопряженное с фосфорилированием адф
- •6 Железосерных белков
- •9. Обмен углеводов
- •9.1. Переваривание и всасывание углеводов
- •9.2. Синтез гликогена
- •9.3. Распад гликогена и освобождение глюкозы (глюкогенез)
- •9.4. Превращения моносахаридов
- •9.4.1. Дихотомический путь распада глюкозы. Гликолиз
- •1. Фосфорилирование:
- •9.4.2. Обмен пировиноградной кислоты
- •9.4.3. Цикл три- и дикарбоновых кислот (цикл Кребса)
- •9.4.4. Энергетический эффект гликолитического расщепления 1 молекулы глюкозы и последующего окисления пвк до со2 и н2о
- •9.4.5. Апотомический путь распада глюкозо-6-фосфата (пентозный, или пентозофосфатный цикл окисления углеводов)
- •9.5. Общая схема распада углеводов
- •9.6. Синтез углеводов
- •10. Обмен белков
- •10.1. Переваривание белков
- •10.2. Превращения аминокислот в организме
- •10.2.1. Процессы гниения белков в кишечнике
- •10.2.2. Судьба всосавшихся аминокислот
- •10.2.3. Конечные продукты распада аминокислот
- •10.3. Новообразование аминокислот
- •11. Обмен липидов
- •11.1. Переваривание и всасывание липидов
- •11.2. Окисление жирных кислот
- •11.3. Распад глицерина
- •11.4. Биосинтез липидов
- •11.4.1. Синтез высших жирных кислот
- •11.4.2. Биосинтез триглицеридов
- •12. Взаимосвязь процессов обмена веществ
- •12.1. Взаимосвязь обменов нуклеиновых кислот и белков
- •12.2. Взаимосвязь обменов нуклеиновых кислот и углеводов
- •12.3. Взаимосвязь обмена белков и углеводов
- •12.4. Взаимосвязь обмена белков и липидов
- •12.5. Взаимосвязь обмена углеводов и липидов
- •13. Регуляция обмена веществ
- •I. Метаболитный уровень регуляции
- •II. Оперонный уровень регуляции
- •III. Клеточный уровень регуляции
- •IV. Организменный уровень регуляции
- •V. Уровень регуляции метаболизма в экосистемах (популяционный)
10.2.3. Конечные продукты распада аминокислот
В результате распада аминокислот возникают СО2, NН3, амины, кетокислоты и другие сложные органические вещества. Все они (кроме СО2 и NH3) подвергаются дальнейшей деструкции.
Амины путем окислительного дезаминирования превращаются в карбоновые кислоты:
R–CH2–NH2 + H2O + CO2 R–CHO + NH3 + H2O2 (фермент моноаминооксидаза)
R–CHO + H2O + НАД R–СООН + НАДН2 (фермент альдегиддегидрогеназа).
Аналогично идет реакция окислительного дезаминирования диаминов при посредстве диаминоксидаз.
Кетокислоты и карбоновые кислоты постепенно окисляются до СО2 и Н2О (см. обмен липидов).
Таким образом, конечными продуктами распада аминокислот являются Н2О, СО2 и NН3. Вода поступает в общий метаболический фонд, углекислый газ выводится из организма.
Аммиак является высокотоксичным соединением, поэтому концентрация его в организме должна сохраняться на низком уровне (1–2 мг/л в крови; концентрация 50 мг/л является летальной).
Поэтому аммиак должен подвергаться связыванию в тканях с образованием нетоксичных соединений, легко выделяемых с мочой.
Пути устранения аммиака в организме
Аммиак в организме может устраняться следующими путями:
1. Образование аммонийных солей: 2NH3 + H2O + CO2 (NH4)2CO3 (у некоторых обитателей гидросферы – пиявок, крабов, раков и др.).
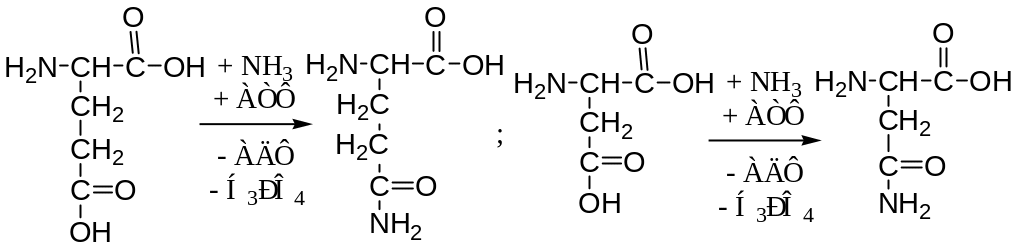
2. Биосинтез глутамина (и аспарагина). Это происходит в мозге, сетчатке, почках, печени и мышцах. Амиды выполняют транспортную функцию.
Синтез амидов требует энергии АТФ и присутствия глу или асп, свободного аммиака и катализируется глутамин- и аспарагинсинтетазами:
3. Основным механизмом обезвреживания аммиака в организме является биосинтез мочевины. Образующаяся мочевина выводится с мочой, на долю ее приходится до 80–85% всего азота мочи. Синтез мочевины локализован в печени. Механизм синтеза мочевины – орнитиновый цикл мочевинообразования – описал Х. А. Кребс в 1932 г.
Образование мочевины начинается с синтеза макроэргического соединения карбамилфосфорной кислоты (карбамилфосфата) из СО2 и NH3 (или глн в качестве донора аммиака) (фермент карбамоилфосфатсинтаза):
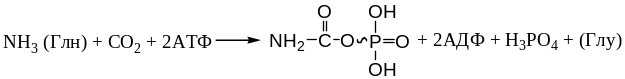
Образовавшийся карбамилфосфат включается в специфический цикл, в котором в качестве регенерируемого компонента («катализатора») принимает участие аминокислота орн, которая не относится к числу аминокислот, формирующих белки, но является важным компонентом азотного обмена. Орн легко возникает при гидролизе арг.
Реакции цикла мочевины:
1. Конденсация карбамилфосфата и орн с образованием цитруллина. Фермент – орнитин-карбамилтрансфераза.
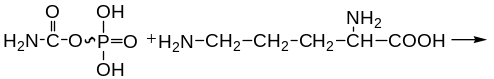
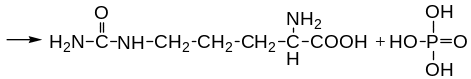
2. Взаимодействие цитруллина с асп с образованием аргининянтарной кислоты (аргининсукцината) Реакция сопряжена с гидролизом АТФ. Фермент – аргининсукцинатсинтетаза.
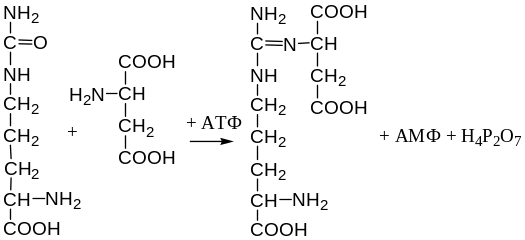
3. Отщепление фумаровой кислоты от аргининянтарной, катализируемое аргининсукцинатлиазой.
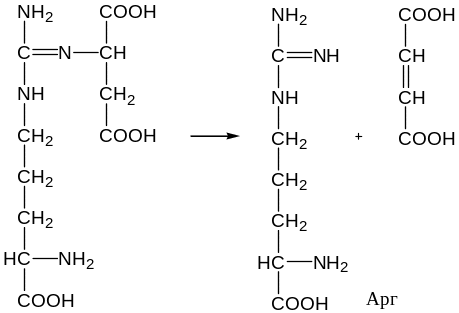
4. Гидролиз аргинина с помощью фермента аргиназы.
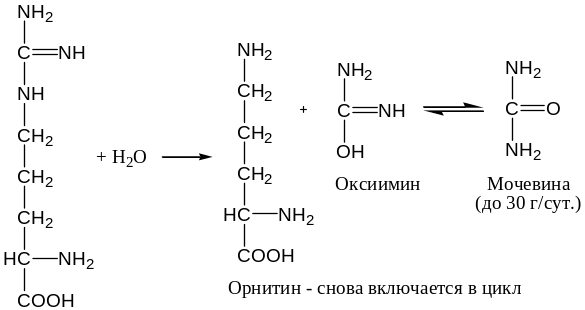
Суммарное уравнение синтеза мочевины:
СО2 + NH3 + 3АТФ + 2Н2О + асп
Н2N–CO–NH2 + 2АДФ + АМФ + фумарат + 2Н3РО4 + Н4Р2О7; -
