
- •Химическое отделение вятский государственный гуманитарный университет
- •М. А. Зайцев основы биохимии
- •Часть 2
- •6. Нуклеиновые кислоты
- •6.1. Химический состав нуклеиновых кислот
- •6.2. Молекулярная масса нуклеиновых кислот
- •6.3. Локализация в клетке днк и рнк. Виды днк и рнк
- •6.4. Строение структурных элементов нуклеиновых кислот
- •6.5.1. Первичная структура днк
- •Генетический код
- •6.5.2. Вторичная структура днк
- •6.5.3. Третичная структура днк
- •6.5.4. Свойства днк
- •6.5.4.1. Репликация (редупликация, самоудвоение) днк
- •6.5.4.2. Транскрипция (синтез рнк)
- •6.6.1. Первичная структура рнк
- •6.6.2. Вторичная структура рнк
- •6.6.3. Третичная структура рнк
- •6.6.4. Классы рнк
- •6.6.5. Синтез белка (трансляция)
- •7. Общие понятия об обмене веществ и энергии в организме
- •7.1. Основные этапы обмена веществ
- •1 Этап. Подготовительный
- •2 Этап. Превращение строительных блоков (мономеров) в более простые соединения
- •3 Этап. Цикл Кребса (цикл ди- и трикарбоновых кислот, цтк)
- •4 Этап. Окислительная цепь ферментов (дыхательная цепь)
- •7.2. Обмен энергии. Макроэргические соединения
- •8. Биологическое окисление
- •8.1. Функции биологического окисления
- •8.2. Типы биологического окисления
- •II. Окисление, сопряженное с фосфорилированием адф
- •6 Железосерных белков
- •9. Обмен углеводов
- •9.1. Переваривание и всасывание углеводов
- •9.2. Синтез гликогена
- •9.3. Распад гликогена и освобождение глюкозы (глюкогенез)
- •9.4. Превращения моносахаридов
- •9.4.1. Дихотомический путь распада глюкозы. Гликолиз
- •1. Фосфорилирование:
- •9.4.2. Обмен пировиноградной кислоты
- •9.4.3. Цикл три- и дикарбоновых кислот (цикл Кребса)
- •9.4.4. Энергетический эффект гликолитического расщепления 1 молекулы глюкозы и последующего окисления пвк до со2 и н2о
- •9.4.5. Апотомический путь распада глюкозо-6-фосфата (пентозный, или пентозофосфатный цикл окисления углеводов)
- •9.5. Общая схема распада углеводов
- •9.6. Синтез углеводов
- •10. Обмен белков
- •10.1. Переваривание белков
- •10.2. Превращения аминокислот в организме
- •10.2.1. Процессы гниения белков в кишечнике
- •10.2.2. Судьба всосавшихся аминокислот
- •10.2.3. Конечные продукты распада аминокислот
- •10.3. Новообразование аминокислот
- •11. Обмен липидов
- •11.1. Переваривание и всасывание липидов
- •11.2. Окисление жирных кислот
- •11.3. Распад глицерина
- •11.4. Биосинтез липидов
- •11.4.1. Синтез высших жирных кислот
- •11.4.2. Биосинтез триглицеридов
- •12. Взаимосвязь процессов обмена веществ
- •12.1. Взаимосвязь обменов нуклеиновых кислот и белков
- •12.2. Взаимосвязь обменов нуклеиновых кислот и углеводов
- •12.3. Взаимосвязь обмена белков и углеводов
- •12.4. Взаимосвязь обмена белков и липидов
- •12.5. Взаимосвязь обмена углеводов и липидов
- •13. Регуляция обмена веществ
- •I. Метаболитный уровень регуляции
- •II. Оперонный уровень регуляции
- •III. Клеточный уровень регуляции
- •IV. Организменный уровень регуляции
- •V. Уровень регуляции метаболизма в экосистемах (популяционный)
6.6.5. Синтез белка (трансляция)
Из современных гипотез наиболее распространена матричная теория. Она предусматривает:
1. Перенос информации из ядра (от ДНК) в цитоплазму к рибосомам в виде нуклеотидной последовательности матричной (информационной) РНК в процессе транскрипции.
2. Активацию аминокислот и перенос активированных аминокислот на полисомы (рибосомы) с помощью транспортных РНК (тРНК).
3. Синтез пептидных связей – трансляцию.
Синтезированная в процессе транскрипции цепь иРНК копирует по своей нуклеотидной последовательности одну из двух цепей ДНК на основе принципа комплементарности. «Переписанные сочетания» нуклеотидов в цепи иРНК в виде кодонов определяет расстановку соответствующих кодируемых ими аминокислот в цепи белковой молекулы.
Таким образом, в иРНК содержится код белкового синтеза в виде сочетаний уникальных для каждой аминокислоты триплетов. ДНК в этом процессе не расходуется и не изменяется, сохраняется в прежнем виде и является готовой для переписывания с нее неограниченного количества иРНК.
Синтез пептидной цепи из свободных аминокислот протекает с поглощением энергии около 3000 кал/моль.
Сущность активирования аминокислот состоит в их взаимодействии с АТФ с образованием аминоациладенилатов, богатых энергией.
На первой стадии АТФ связывается с ферментов аминоацил-тРНК-синетазой, на второй стадии АТФ взаимодействует с аминокислотой:
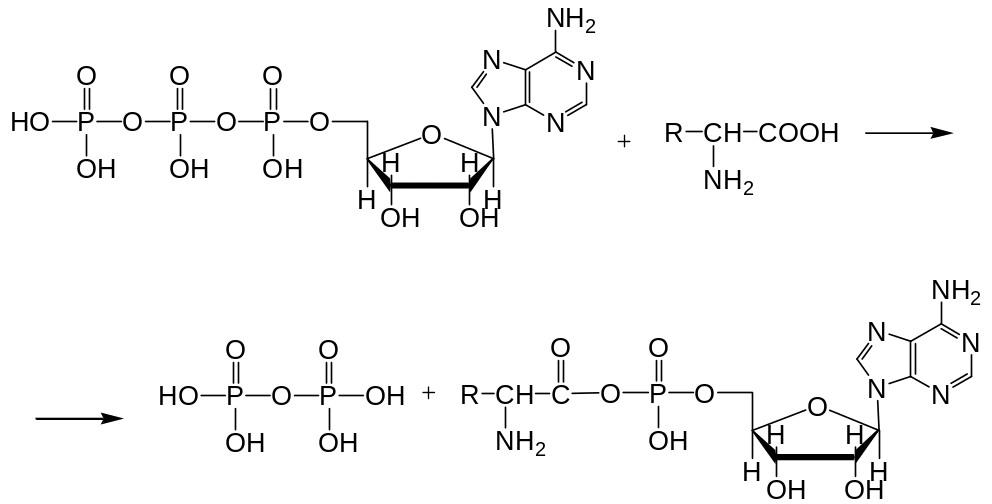
Затем активированные аминокислоты переносятся к тРНК и присоединяются на ЦЦА–ОН (3):
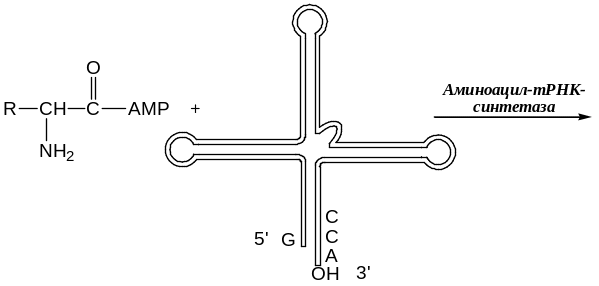
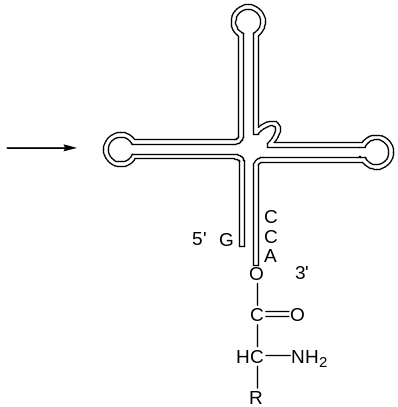
Этапы синтеза белка
1. Инициация. Начало трансляции – медленный процесс. Рибосома разомкнута. иРНК связывается с малой субчастицей. Точка присоединения к субчастице расположена рядом с 5'-концом РНК, так как «чтение» программы РНК идет в направлении 5'3'.
В пределах субчастицы умещаются только два кодона иРНК. Первым кодоном иРНК у 5'-конца является АУГ или ГУГ. Это инициирующие кодоны, с них всегда начинается трансляция в рибосомах. Им соответствует антикодон метионил-тРНК, где NH2-группа блокируется формильной группой. Есть факторы инициации (IF1, IF2, IF3) и ГТФ. Факторы облегчают связывание иРНК с малой субчастицей и ГТФ с образованием инициаторного комплекса (рис. 20).
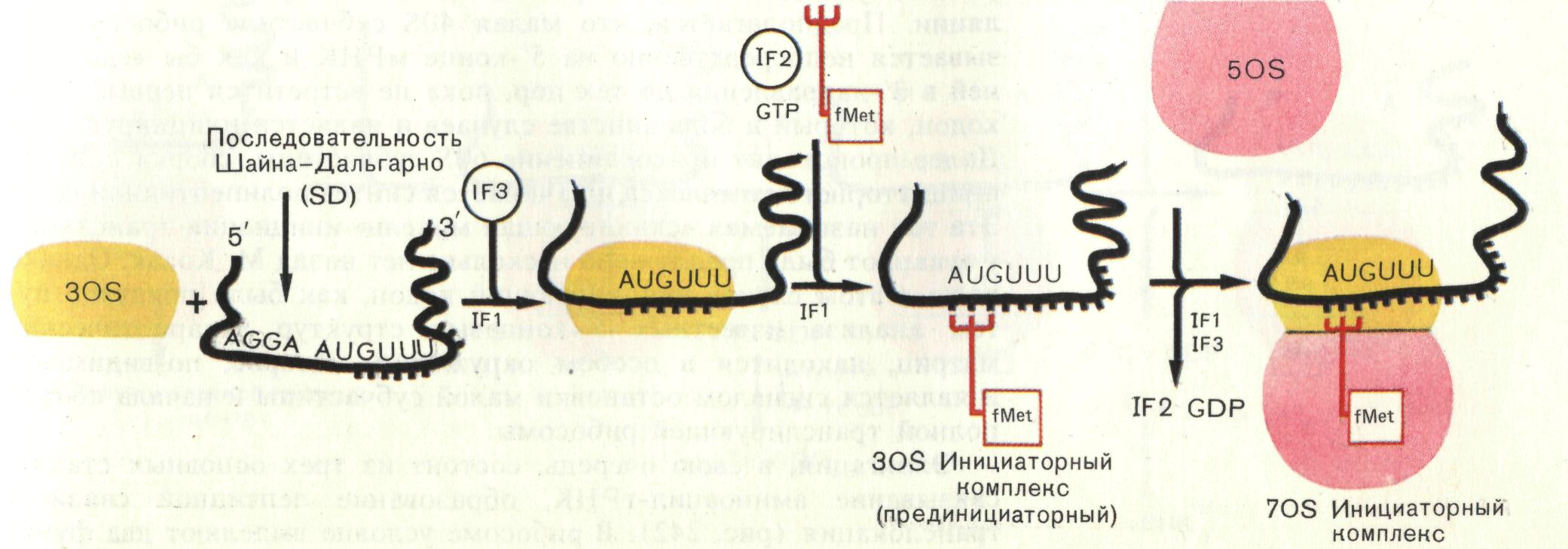
Рис. 20. Образование инициаторного комплекса у прокариот
После этого факторы IF1, IF2, IF3 удаляются. Энергия берется из ГТФ.
Метионил-тРНК антикодоном спаривается с кодоном АУГ иРНК, т. е. как бы подвешивается на водородных связях к иРНК, а акцепторный конец, где находится аминокислота, прикрепляется к большой субчастице рибосомы.
2. Элонгация. Синтез начинается от N-конца и заканчивается С-концом. Здесь три шага:
1. Связывание аминоацил-тРНК в аминоацильном центре.
2. Перенос пептида в пептидилтрансферазный центр.
3. Перемещение иРНК на один триплет.
Первый шаг. В рибосомах (как показано на рис. 21) слева находится тРНК, которая антикодоном связана с кодоном иРНК, а акцепторный конец «связан» с растущим пептидом.
Этот пептид, входящий в пептидил-тРНК, связан с пептидилтрансферазным (пептидильным, Р) центром, который в виде белковой ниши находится на большой субъединице. В момент первого шага второй кодон иРНК свободен. С ним спаривается своим антикодоном поступающая в рибосому аминоацил-тРНК. Аминоацильный конец этой тРНК связывается с аминоацильным центром (А) большой субъединицы. На этом первый шаг, то есть связывание, заканчивается.
Второй шаг. Происходит переброс пептида с левой тРНК на аминогруппу аминоацил-тРНК. При этом образуется пептидная связь. Катализируют образование пептидной связи белки рибосом, которые обладают активным действием.
Третий шаг. Состоит в размыкании субчастиц рибосом, на что расходуется энергия одной молекулы ГТФ. Пептидил-тРНК, несущая уже трипептид, перемещается с А-участка вместе с иРНК, с которой она спарена, в Р-участок на один триплет и выталкивает свободную тРНК из рибосомы. Для синтеза одной пептидной связи (или удлинения пептида на одну аминокислоту) затрачивается энергия двух молекул ГТФ.

Рис. 21. Стадия элонгации. Синтез первой пептидной связи:
1 – EF-Tu-зависимое связывание аминоацил-тРНК с А-участком рибосомы;
2 – пептидилтрансферазная реакция; 3 – EF-G-зависимая транслокация
3. Терминация – окончание трансляции, зависит от присутствия в иРНК терминирующих кодонов, или стоп-сигналов (УАА, УГА, УАГ), и белковых факторов (рис. 22). С этими кодонами не может связываться ни одна тРНК, так как нет тРНК с соответствующими антикодонами. Присоединение белковых факторов терминации к иРНК стимулирует пептидилэстеразную активность рибосомальных белков, вследствие чего гидролизуется сложноэфирная связь между новообразованным полипептидом и тРНК.
В результате синтезированный белок отделяется от нее, одновременно освобождается тРНК и иРНК, а рибосома 70S распадается на субчастицы 30 и 50S.
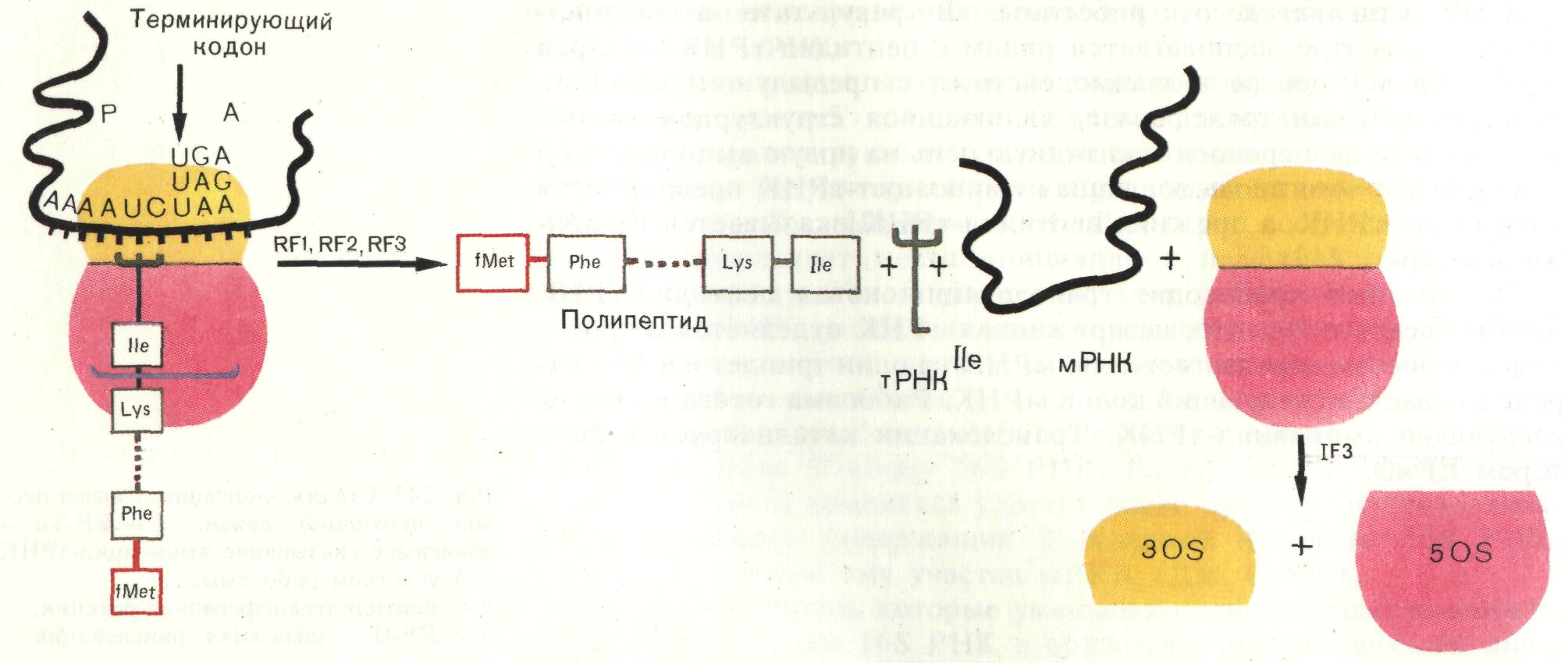
Рис. 22. Терминация синтеза белка
