
- •Химическое отделение вятский государственный гуманитарный университет
- •М. А. Зайцев основы биохимии
- •Часть 2
- •6. Нуклеиновые кислоты
- •6.1. Химический состав нуклеиновых кислот
- •6.2. Молекулярная масса нуклеиновых кислот
- •6.3. Локализация в клетке днк и рнк. Виды днк и рнк
- •6.4. Строение структурных элементов нуклеиновых кислот
- •6.5.1. Первичная структура днк
- •Генетический код
- •6.5.2. Вторичная структура днк
- •6.5.3. Третичная структура днк
- •6.5.4. Свойства днк
- •6.5.4.1. Репликация (редупликация, самоудвоение) днк
- •6.5.4.2. Транскрипция (синтез рнк)
- •6.6.1. Первичная структура рнк
- •6.6.2. Вторичная структура рнк
- •6.6.3. Третичная структура рнк
- •6.6.4. Классы рнк
- •6.6.5. Синтез белка (трансляция)
- •7. Общие понятия об обмене веществ и энергии в организме
- •7.1. Основные этапы обмена веществ
- •1 Этап. Подготовительный
- •2 Этап. Превращение строительных блоков (мономеров) в более простые соединения
- •3 Этап. Цикл Кребса (цикл ди- и трикарбоновых кислот, цтк)
- •4 Этап. Окислительная цепь ферментов (дыхательная цепь)
- •7.2. Обмен энергии. Макроэргические соединения
- •8. Биологическое окисление
- •8.1. Функции биологического окисления
- •8.2. Типы биологического окисления
- •II. Окисление, сопряженное с фосфорилированием адф
- •6 Железосерных белков
- •9. Обмен углеводов
- •9.1. Переваривание и всасывание углеводов
- •9.2. Синтез гликогена
- •9.3. Распад гликогена и освобождение глюкозы (глюкогенез)
- •9.4. Превращения моносахаридов
- •9.4.1. Дихотомический путь распада глюкозы. Гликолиз
- •1. Фосфорилирование:
- •9.4.2. Обмен пировиноградной кислоты
- •9.4.3. Цикл три- и дикарбоновых кислот (цикл Кребса)
- •9.4.4. Энергетический эффект гликолитического расщепления 1 молекулы глюкозы и последующего окисления пвк до со2 и н2о
- •9.4.5. Апотомический путь распада глюкозо-6-фосфата (пентозный, или пентозофосфатный цикл окисления углеводов)
- •9.5. Общая схема распада углеводов
- •9.6. Синтез углеводов
- •10. Обмен белков
- •10.1. Переваривание белков
- •10.2. Превращения аминокислот в организме
- •10.2.1. Процессы гниения белков в кишечнике
- •10.2.2. Судьба всосавшихся аминокислот
- •10.2.3. Конечные продукты распада аминокислот
- •10.3. Новообразование аминокислот
- •11. Обмен липидов
- •11.1. Переваривание и всасывание липидов
- •11.2. Окисление жирных кислот
- •11.3. Распад глицерина
- •11.4. Биосинтез липидов
- •11.4.1. Синтез высших жирных кислот
- •11.4.2. Биосинтез триглицеридов
- •12. Взаимосвязь процессов обмена веществ
- •12.1. Взаимосвязь обменов нуклеиновых кислот и белков
- •12.2. Взаимосвязь обменов нуклеиновых кислот и углеводов
- •12.3. Взаимосвязь обмена белков и углеводов
- •12.4. Взаимосвязь обмена белков и липидов
- •12.5. Взаимосвязь обмена углеводов и липидов
- •13. Регуляция обмена веществ
- •I. Метаболитный уровень регуляции
- •II. Оперонный уровень регуляции
- •III. Клеточный уровень регуляции
- •IV. Организменный уровень регуляции
- •V. Уровень регуляции метаболизма в экосистемах (популяционный)
8. Биологическое окисление
Совокупность окислительных реакций, происходящих в биологических объектах и обеспечивающих их энергией и метаболитами для осуществления процессов жизнедеятельности, называется биологическим окислением.
8.1. Функции биологического окисления
Энергетическое обеспечение: поддержания температуры тела; биолюминесценции (свечения); химических синтезов; осмотических явлений; электрических процессов; механической работы.
Синтез важнейших (ключевых) метаболитов.
Регуляция обмена веществ.
Устранение вредных для клетки продуктов обмена (шлаков).
Детоксикация проникших в организм чуждых соединений – ксенобиотиков (пестицидов, препаратов бытовой химии, лекарственных средств, промышленных загрязнений и т. п.).
Разнообразные реакции биологического окисления ускоряются многочисленными ферментами оксидоредуктазами, которые, как правило, встроены в биологические мембраны, причем очень часто в виде ансамблей.
Существуют 2 типа биологического окисления.
8.2. Типы биологического окисления
I. Свободное окисление – окисление, не сопряженное с фосфорилированием АДФ и не сопровождающееся трансформацией энергии, выделяющейся при окислении, в энергию макроэргических связей. При свободном окислении высвобождающаяся энергия переходит в тепловую и рассеивается.
Реакции свободного окисления органических соединений в живой природе и ускоряющие их ферментные системы многообразны. Этим путем непосредственно окисляются не только многочисленные природные и неприродные субстраты, но и восстановленные коферменты (НАДН, НАДФН, ФАД·Н2 и др.), образовавшиеся при действии первичных и вторичных дегидрогеназ.
Реакции свободного окисления протекают в цитозоле, на мембранах различных субклеточных структур, в ядерном аппарате клетки. Основным средоточием их являются мембраны эндоплазматической сети (ЭПС).
Так как мембраны ЭПС при гомогенизации клеток и фракционировании субклеточных частиц гомогената дают фракцию микросом, то реакции окисления на мембранах ЭПС называются микросомальным окислением.
Особенности микросомальной дыхательной цепи
1). Несмотря на наличие ферментов цепи переноса электронов, ни в одном пункте этой цепи не происходит сопряжения с фосфорилированием АДФ.
2). Своеобразие структуры и функциональной активности цитохромов b5 и Р–450, входящих в ее состав. Так цитохром Р–450 (гемопротеин) обладает множеством форм, возникающих в ответ на введение в организм ксенобиотиков (подобно тому, как антитела синтезируются в ответ на присутствие антигенов); поэтому цитохром Р–450 считают своего рода «мембранным иммуноглобулином».
3). Высокое сродство терминальной оксидазы микросомальных цепей к кислороду, позволяющее ей конкурировать за кислород с митохондриальной цитохромоксидазой.
Наиболее своеобразными являются реакции свободного окисления, идущие при участии оксигеназ. Этот подкласс оксидоредуктаз содержит ферменты, ускоряющие включение в окисляемый субстрат либо двух (диоксигеназы), либо одного (монооксигеназы) атома молекулярного кислорода.
Примеры диоксигеназных реакций:
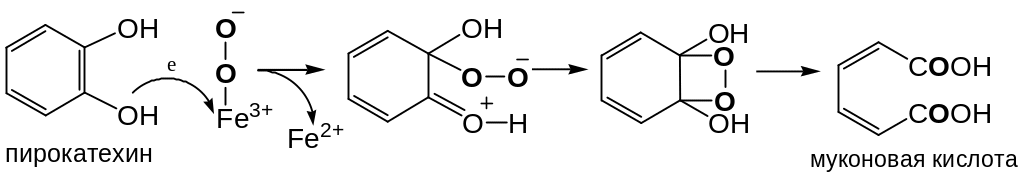
– Действие пирокатехазы (катехол: кислород-1,2-оксидоредуктазы дециклизующей). Этот фермент содержит в активном центре 2 прочно связанных атома железа, которые соединяются с молекулярным кислородом в комплекс, где кислород далее активируется: Fe2+ + О2 → Fе2+О2 → Fе3+О2–.
Затем в активном центре пирокатехазы после присоединения субстрата возникает тройной комплекс, преобразование которого приводит к включению кислорода (О2) в пирокатехин:
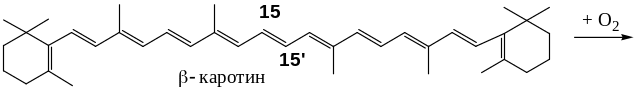
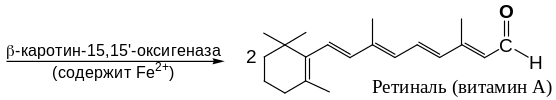
– Превращение -каротина в витамин А:
Свободное окисление при участии монооксигеназ. Монооксигеназы, как правило, не содержат в своем составе ионы тяжелых металлов, а содержат коферменты флавиновой природы. Кроме того, многие из них требуют участия в реакции монооксигенирования парного донора, от которого поступают атомы водорода на один из атомов молекулярного кислорода, а второй атом кислорода внедряется в окисляемый субстрат.
Простейший представитель монооксигеназ – фенолгидроксилаза (фенол-2-монооксигеназа):

Монооксигеназы принимают участие в окислении аминокислот, оксикислот, полиизопреноидных соединений. Механизм действия монооксигеназ выяснен недостаточно.
